
题目列表(包括答案和解析)
1.成熟的神经细胞在兴奋时,下列几种酶中活跃的是
A.RNA聚合酶 B.DNA解旋酶
C.蛋白酶、脂肪酶 D.与ATP和ADP相互转化有关的酶
32.[生物--现代生物科技专题](10分)
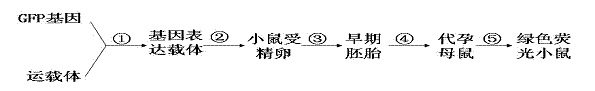 2008年诺贝尔化学奖授予了三位在研究绿色荧光蛋白(GFP)方面做出突出贡献的科学家。绿色荧光蛋白能在蓝光或紫外光的激发下发出荧光,这样借助GFP发出的荧光就可以跟踪蛋白质在细胞内部的移动情况,帮助推断蛋白质的功能。GFP基因可作为目的基因用于培育绿色荧光小鼠,下图表示培育绿色荧光小鼠的基本流程:
2008年诺贝尔化学奖授予了三位在研究绿色荧光蛋白(GFP)方面做出突出贡献的科学家。绿色荧光蛋白能在蓝光或紫外光的激发下发出荧光,这样借助GFP发出的荧光就可以跟踪蛋白质在细胞内部的移动情况,帮助推断蛋白质的功能。GFP基因可作为目的基因用于培育绿色荧光小鼠,下图表示培育绿色荧光小鼠的基本流程:
请根据上述材料回答下列问题:
(1)过程①必需用到的工具酶是 。
(2)过程②将基因表达载体导入小鼠受精卵时,采用最多也最有效的方法是 。然后还可以通过 技术来检测绿色荧光蛋白基因是否已导入成功。
(3)在进行过程④前,利用 技术可以获得数目更多且基因型相同的绿色荧光小鼠。
(4)GFP基因与目的基因一起构建到载体上不影响目的基因的表达,也不影响由目的基因控制合成的蛋白质的结构与功能,且对细胞无毒性作用,因此GFP基因可以运用作为基因表达载体上的 。
福建宁德四县市一中2010届高三第一次联考
31.[化学选考----有机化学](13分)
根据图示填空
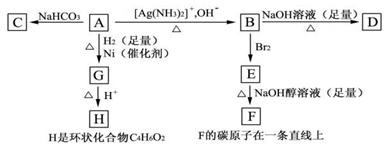
(1)化合物A含有的官能团是_________________________。
(2)B在酸性条件下与Br2反应得到E,E在足量的氢氧化钠醇溶液作用下转变成F,由E转变成F时发生两种反应,其反应类型分别是_____________、____________。
(3)D的结构简式是______________________。
(4)1 mol A与2 mol H2 反应生成1 mol G,其反应方程式是_____________________。
(5)与A具有相同的官能团的A的同分异构体的结构简式是_____________________
30.[化学选考-----物质结构与性质](13分)
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
 (1)A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
(1)A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
|
电离能(kJ/mol) |
I1 |
I2 |
I3 |
I4 |
|
A |
932 |
1821 |
15390 |
21771 |
|
B |
738 |
1451 |
7733 |
10540 |
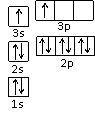
某同学根据上述信息,推断B的核外电子排布如右图所示,该同学所画的核外电子排布式违背了 原理
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。
(3)氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
①写出铬原子的基态电子排布式_________________________________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有____________(填元素符号)。
②CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是__________(填“极性”或“非极性”)分子。
29.[物理选修--3-5](本题有两小题,每小题6分共12分。每小题只有一个选项符合题意。)
(1)下列说法正确的是______
①γ射线在电场和磁场中都不会发生偏转
②β射线比α射线更容易使气体电离
③太阳辐射的能量主要来源于重核裂变
④核反应堆产生的能量来自轻核聚变
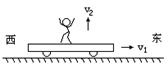 (2)
如图所示,质量为m的人立于平板车上,人与车的总质量为M,人与车以速度v1在光滑水平面上向东运动。当此人相对于车以速度v2竖直跳起时,车向东的速度大小为__________
(2)
如图所示,质量为m的人立于平板车上,人与车的总质量为M,人与车以速度v1在光滑水平面上向东运动。当此人相对于车以速度v2竖直跳起时,车向东的速度大小为__________
①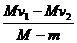 ②
②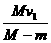 ③
③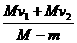 ④V1
④V1
28. [物理选修--3-3](本题有两小题,每小题6分共12分。每小题只有一个选项符合题意。)
(1)下列说法中正确的是 (填选项前的编号)
①常温、常压下,一定质量的理想气体在等温变化过程中,若吸热,则一定对外做功
②温度越高的物体,分子的平均动能越大,内能也越大
③晶体具有规则的几何何形状,在各个方向上的物理性质不同,即表现为各向异性
④布朗运动是悬浮在液体中的固体分子的无规则运动
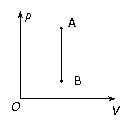 (2)如图所示,为汽缸内密闭的一定质量的气体从状态A变化到状态B的过程中其压强随体积变化的图象。若忽略气体分子之间的分子势能,
(2)如图所示,为汽缸内密闭的一定质量的气体从状态A变化到状态B的过程中其压强随体积变化的图象。若忽略气体分子之间的分子势能,
则下列判断正确的是 (填选项前的编号)
①从状态A到状态B,气体温度升高
②从状态A到状态B,气体吸收热量
③在相同时间内,A、B两状态的气体分子对活塞的冲量相等
④与状态B相比,状态A的气体分子在单位时间内撞击活塞的个数较多
27.(14分)某生物学研究小组观察到某野外四个物种在一天中的平均活动时间(活动时间以%表示):
|
|
休息 |
与其它物种关系 |
进食 |
其它活动 |
|
物种A |
20% |
15%追逐物种B |
55%吃种子 |
10% |
|
物种B |
20% |
25%被物种A追逐 |
45%吃种子 |
10% |
|
物种C |
75% |
|
l5%吃物种A |
10% |
|
物种D |
75% |
|
20%吃物种C |
5% |
(1)根据表中信息,试表示出该生态系统中可能的营养结构关系。

(2)物种A、B之间的关系属于 ,物种C与物种A的关系属于 。从食性角度看,物种C、D一天中进食时间较短而休息时间较长,其可能的原因是
。
(3)组成一个典型的生态系统。除表中涉及的生态系统成分外,还应有 。
(4)碳元素进入该生态系统的生物群落主要是从 开始的,若研究发现一段时期内,进人该生态系统生物群落的碳元素总量与由群落进入无机环境的碳元素总量相等,则说明该项生态系统基本处于 状态。
选考部分
第Ⅱ卷选考部分共5题,共35分。其中,第28、29题为物理题,第30、31题为化学题,考生从两道物理题、两道化学题中各选一题作答,若第28、29题都作答,则按第28题计分,若第30、31题都作答,则按第30题计分;第32题为生物题,是必答题。请将答案都填写在答题卡选答区域的指定位置上。
26.(26分)人体内环境的稳态的维持,依赖于各个器官、系统的协调活动,而信息分子是它们之间的“语言”。分析下图,回答问题:
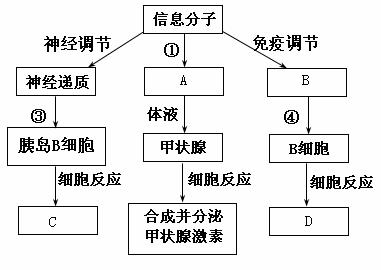 (Ⅰ)写出有关序号或字母所代表的含义或生理过程。
(Ⅰ)写出有关序号或字母所代表的含义或生理过程。
① B D:
(Ⅱ)
(1)神经递质通过 ,在两个神经细胞之间传递,其间信息传递的变化规律是____________________________。接收兴奋性递质刺激的神经细胞,其膜外电位的变化_________________。
(2)在 刺激下,C过程会增强,同时该腺体中的 激素分泌量会减少,以维持内环境的相对稳定。这两类激素间的作用称为_________作用。
(3)图中A的分泌量的多少受到_____________、_____________两种信息分子的调节。
(4)当吃食物过咸时,可导致____________的上升,通过图中的①和________调节可使之恢复正常
25.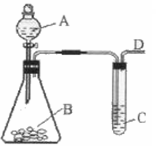 某同学用如图所示的装置来探究SO2的性质及有关实验。
某同学用如图所示的装置来探究SO2的性质及有关实验。
(1)实验前应先检验装置的气密性,方法是
(2)实验室用亚硫酸钠固体与硫酸反应制取SO2气体,写出该反应的化学方程式 。
(3)将制取的SO2气体通入C溶液中,请回答下列问题:
①若C溶液是紫色石蕊试液,通入少量SO2气体后,现象是 ,继续通入过量的SO2气体,现象是 。
②若C溶液是橙色的溴水溶液,通入SO2气体后现象是 ,写出反应的离子方程式 。
③若C溶液是澄清石灰水,缓慢且持续通入SO2气体过程中,观察到的现象是 。写出相应反应的化学方程式 。
24.(15分)自然界中存在的天然纯碱主要来自于碱湖和固体碱矿。工业上以氯化钠为原料生产纯碱。
我国化工专家侯德榜发明的侯氏制碱法的原理是将二氧化碳通入氨水的氯化钠饱和溶液中,使碳酸氢钠从溶液中析出,过滤得到碳酸氢钠晶体。已知氯化钠、碳酸氢钠、碳酸氢铵在20℃下的溶解度分别为:36 g、9.6 g、21.7 g。侯氏制碱法的流程如下图:

⑴请写出制取碳酸氢钠的化学方程式: ,碳酸氢钠能从溶液中析出的原因是: 。
⑵侯氏制碱法的原理是将二氧化碳通入氨水的氯化钠饱和溶液中,能否将其改为“将氨水通入到二氧化碳的氯化钠饱和溶液”呢(选填“能”或“不能”)? 。你选择的理由是: __________________________ __。
⑶将析出的碳酸氢钠晶体煅烧,分解得到碳酸钠。写出该反应的化学方程式: 。
⑷在滤出碳酸氢钠后的母液中加入石灰水并加热,生成的氨可以重新利用,写出发生反应的化学方程式:
。反应的另一产物氯化钙被弃掉,母液中食盐的利用率只有70%。侯德榜先生经过多年的摸索和实践,在过滤出碳酸氢钠后的母液中,不加石灰水,而是在降温到t ℃后加食盐,利用低温下氯化铵比氯化钠溶解度小的特点,加入的食盐在连续循环操作中不断被利用,使食盐的利用率提高到96%。同时,析出的氯化铵又可作为化学肥料。请根据下表所给有关溶解度的数据,结合经济效益推测温度t应在 左右
   溶解度 温度 溶解度 温度物质 |
0 ℃ |
10 ℃ |
20 ℃ |
30 ℃ |
|
NaCl |
35.7 g |
35.8 g |
36.0 g |
36.3 g |
|
NH4Cl |
29.4 g |
33.3 g |
37.2 g |
41.4 g |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com