
题目列表(包括答案和解析)
1.2009年度诺贝尔化学奖授予英国科学家拉玛克里斯南、美国科学家斯泰茨、以色列科学家约纳什因,以表彰他们在核糖体结构和功能研究中的贡献,以下对核糖体的叙述正确的是
A.所有生物都含有核糖体
B.核糖体不含膜结构,因此不含有磷元素
C.核糖体是细胞内水和ATP形成的重要场所之一
D.核仁与核糖体的形成有关
14.B 15.D 16.A 17.AD 18.C 19.AB 20.C 21.BC

(3)导体棒匀速运动时,速度大小为 ………… 1分
………… 1分
则力F的作用时间t应满足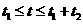 ,即
,即 (2分)
(2分)

34.(11分) 白花三叶草有叶片内含氰(有剧毒)和不含氰的两个稳定遗传的品种,已知白花三叶草叶片内氰化物是经下列途径产生的(如下图)。

(1)若某一品系基因突变后,叶片内不含氰,但含氰糖苷较多,发生突变的基因是__________。
(2)若两个不含氰的品种杂交,F1全部含氰,F1自交得到F2。写出亲代的基因型_________ ; F2个体的表现型及其比例是______ ____;F2含氰个体中能稳定遗传的个体所占的比例是______ ____。
(3)现有HhDd个体,怎样快速培育出含氰且能稳定遗传的个体?简要写出培育过程
①______ _ ___;
②______ ___;
③_______ .
2009-2010学年第二次四校联考物理试题答案
33.(11分)玉米种子在黑暗中萌发,测定胚芽鞘与幼根中各部分生长素含量,结果如图A所示。请据图分析回答:

(1)从图中观察玉米种子萌发过程中,合成生长素旺盛的部位是_______和_______。
(2)调节根尖伸长区细胞伸长的生长素来源于根尖的_____ __。
(3)切除玉米胚芽鞘的顶端,然后在其左侧放置含有不同浓度生长素的琼脂块,保持在黑暗中12h。胚芽鞘可能向右弯曲,弯曲角度如图B所示。生长素浓度与弯曲角度关系如图C 所示。实验要在黑暗中进行的原因是_________________。
(4)请分析说明实验结果:_______________ __。
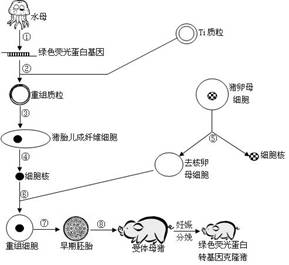
32. (8分)下图为我国首例绿色荧光蛋白转基因克隆猪的培育过程示意图。请据图回答:
⑴过程①和②必需用到的酶是 。绿色荧光蛋白基因在猪体内表达的步骤是 和 。
⑵重组质粒除了带有绿色荧光蛋白基因以外,还必须含有 才能构成一个完整的基因表达载体。
⑶为了获得更多的猪卵母细胞,可通过对母猪注射 的方法来达到目的。
⑷将所采集到的卵母细胞在体外通过显微操作将其 去除并形成重组细胞,然后再通过 技术培养成早期胚胎。
(5)早期胚胎的培养液成分较复杂,除一些无机盐和有机物外,还需添加维生素、激素、氨基酸、核苷酸等营养成分,以及 等物质。
31.(12分)将两株植物放在封闭的玻璃罩内,用全素营养液置于室外进行培养(如下图甲),假定玻璃罩内植物生理状态和自然环境中相同,且空气湿度对植物蒸腾作用的影响、微生物对CO2浓度的影响忽略不计。现用CO2浓度测定仪测定该玻璃罩内一天中CO2浓度的变化情况,绘制成如乙图所示曲线。请据图分析回答:

(1)BC段与AB段相比,曲线上升缓慢,其原因是 。
(2)G点时植物生理活动过程的特点是 。
(3)EF段说明此植物光合速率 (“较快”或“较慢”),由此推断该植物应为 (“C3植物”或者“C4植物”)。
 (4)一天之后,将玻璃罩去掉,仍置于原处培养。一星期后,两培养瓶中的植物均开始生长不正常,其原因可能有①
;②
。
(4)一天之后,将玻璃罩去掉,仍置于原处培养。一星期后,两培养瓶中的植物均开始生长不正常,其原因可能有①
;②
。
30.(共14分)请根据下图作答:

已知:一个碳原子上连有两个羟基时,易发生下列转化:

(1)E中含有的官能团是 。
(2)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1,则B的分子式为 。
(3)反应③的化学方程式 。
(4)F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有多种结构,写出其中一种的结构简式 。
29.(共16分)两组同学利用下列装置(某些可重复使用)和试剂完成某些实验的探究。
①18.4mol/L硫酸;②2mol/L稀硫酸;③KClO3固体;④碱石灰;⑤4mol/L NaOH溶液;⑥浓氨水;⑦MnO2固体;⑧生石灰;⑨2mol/L稀盐酸;⑩Na2SO3固体;
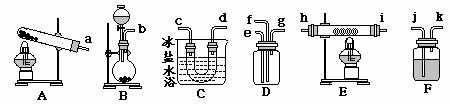
[Ⅰ] 甲小组同学在D中加入浓硫酸,E中选择V2O5催化,欲摸拟工业上SO2的氧化反应。
(1)所选装置用橡胶管连接,其接口连接顺序:{ 其中a确定接e } 为:
( )←→(f)←→(g)←→( )←→( )←→( )←→( )←→( )
(2)证明生成SO3生成的实验依据是________________________________。
(3)相关该实验中下列分析正确的是___________。
①加热E装置既可以提高反应速率又可以提高SO2的转化率。
②D瓶在实验中既可以用于干燥气体又可以用于混合气体,还可以观察气流的流速;
③实验中一段时间后E装置无需持续加热,反应依然可以进行;
④工业上与E对应的生产设备称为接触室;
⑤工业吸收塔中常用2mol/L稀硫酸吸收SO3效果最好。
[Ⅱ] 乙小组采用在D中不加入试剂,E中放入铂铑合金网,欲用上述装置和某些试剂完成工业生产中常见X气体的催化氧化。最终观察到E中产生红棕色气体且在C中颜色逐渐变浅,底部有少量液体产生。
(4)E装置可能发生的反应的化学方程式为_______________;____________。
(5)若用B装置,则B中所加试剂为__________和_________。
(6)按此设计,实验中E中没明显观察到红棕色气体,其原因可能是(气密性良好)______________________________________________________________________。
28.(共15分)现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型。A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子甲、乙、丙。
(1)元素F在周期表中的位置是________________。
(2)写出元素A、C形成分子C2A4的电子式:________________。
(3)甲、乙、丙三物质沸点由高到低的顺序为(用分子式):________________。
(4)生活中的一种绿色氧化剂由A和D组成,一定条件下也可表现出还原性,试写出表现其还原性的一个离子方程式: 。
(5)某盐X(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性。盐X显酸性原因(用离子方程式表示) 。
27.(共15分)有A、B、C、D、E、F六种物质,它们之间相互转化的关系如下图所示(反应条件及部分产物未标出)。
(1)若A、D、F都是短周期元素非金属单质,常温下,A、D为固体,D单质作为半导体材料,F为气体,则反应①的化学方程式是_________________________。
(2)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,C的溶液为浅绿色,则反应②(在水溶液中进行)的离子方程式:_____ _________________;
已知1 g D与足量F在光照的条件下完全反应生成B时,放出92.3 kJ热量,试写出该反应的热化学方程式:_______________________________________________。
工业上可电解某盐溶液同时制得D和F,写出电解阳极的电极反应式: 。
(3)若A、D为生活中常见金属,工业上用电解C的方法冶炼A,反应③在溶液中进行,则反应③的离子方程式是:_______ _
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com