
题目列表(包括答案和解析)
25、某学生用标准 溶液滴定未知硫酸溶液,根据题目要求回答问题。
溶液滴定未知硫酸溶液,根据题目要求回答问题。
 (1)实验操作如下:
(1)实验操作如下:
A.用酸式滴定管取稀
 ,
,
注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2-3cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下。
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2-3cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管
液面所在刻度。
①滴定操作的正确顺序(用序号填写)_________(2分)
②该滴定操作中应选用的指示剂是_________
③在G操作中如何确定终点?___________
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入滴定管_____(选填“甲”或“乙”中)。
(3) 误差分析(填“偏小”、“偏大”或“无影响”)
① 碱式滴管用蒸馏水润洗后,未用标准液润洗导致滴定结果______.
② 碱式滴定管滴定前尖,滴定后气泡消失_________
③ 观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值________.
24、(8分)下图是 -
- 原电池的示意图,试根据图示回答有关问题:
原电池的示意图,试根据图示回答有关问题:

(1)锌极是 极,电极反应式是 ,发生 反应;
(2)铜极是 极,电极反应式是 ,发生 反应;
(3)电池的总反应式是 ,若锌电极质量变化了3.25g,则电路中转移的电子的物质的量为 mol。
23.(12分)已知X是由两种元素组成的黑色固体,可溶于盐酸,白色固体Y即可溶于硫酸,又可溶于NaOH溶液,C为棕红色气体,D可使用品红溶液褪色,B、E是金属单质,他们之间有下列变化(其反应条件均略去):


(1) 写出化学式:X_________;D____________;
(2) 固体C中阳离子的检验方法__________________________;
(3)写出B与 溶液的化学方程式
;
溶液的化学方程式
;
(4)写出Y溶于 溶液的离子方程式
;
溶液的离子方程式
;
(5)写出B与C反应的化学方程式 ;
(6)写出C与稀硫酸反应的化学方程式 。
22.(11分)(1)在一定条件下反应:2A+B→2C,达到平衡
①若升高温度,平衡向做移动,则正反应是____(放、吸)热反应;
②增加或减少B时,平衡不移动,则B是______态;
③若A、B、C都是气体,增加压强,平衡向_____(左、右)移动。
(2)盐类水解的实质是____________________________________________;
在25℃时电离出的H+和OH-浓度为____,其离子浓度乘积为_____,此温度下PH=12的NaOH溶液中由水电离出的c(OH-)=___;FeCl3稀溶液呈(填“酸性”或“碱性”),原因是(用离子方程式表示)_________
在配置Al2(SO4)3溶液时,为了防止发生水解,可以加入少量的______,盐碱地(含较多的NaCl、Na2CO3)不利于作物生长产生碱性的原因是(用离子方程式表示)______
21.(5分)黑火药爆炸时,发生的反应是:S+KNO3+C→K2S+N2,配平时的化学计量系数依次是____ ____ ____=_____ _____ ____,反应中的氧化剂是____;_____元素被氧化,每生成1 mol CO2转移_____mol电子。
20、将 的
的 与
与 的
的 溶液等体积混合后,所得的混合溶液中,下列关系式正确的是( )
溶液等体积混合后,所得的混合溶液中,下列关系式正确的是( )
A.
B.
C.
D.
19、某 溶液中含
溶液中含 的
的 、
、 的
的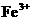 ,加入
,加入 的铁粉,待
的铁粉,待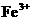 完全还原后,溶液中的
完全还原后,溶液中的 的物质的量浓度为( )
的物质的量浓度为( )
A. B.
B. C.
C. D.
D.
18、 A、B、C、D、E是含有一种相同元素的五种物质,在一定条件
A、B、C、D、E是含有一种相同元素的五种物质,在一定条件
下可发生如图所示的转化,其中A是由非极性分子构成的气体
单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化
物,则A可能是( )
A. B.
B. C.
C.
 D.
D.
17、某无色透明溶液能与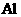 反应放出
反应放出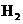 ,则此溶液中可能大量存在的离子是( )
,则此溶液中可能大量存在的离子是( )
A. 、
、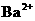 、
、 、
、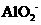 B.
B. 、
、 、
、 、
、
C. 、
、 、
、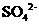 、
、 D.
D. 、
、 、
、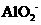 、
、
16、在一定温度下的固定容积的密闭容器中,反应

 ,达到平衡的标志是( )
,达到平衡的标志是( )
A.单位时间内生成
 ,同时生成
,同时生成

B.容器内的总压强、密度和平均相对分子质量均不随时间变化
C.容器内 、
、 、
、 的物质的量之比
的物质的量之比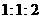
D.单位时间内生成
 的同时生成
的同时生成

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com