
题目列表(包括答案和解析)
17、( )右表为元素周期表短周期的一部分,有关元素X、Y、Z、M的说
法不正确的是
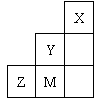 A X晶体的结构微粒是原子,故属于原子晶体
A X晶体的结构微粒是原子,故属于原子晶体
B Y的氢化物沸点比M的氢化物的沸点高
C 原子半径:Z>M>Y
D Z离子的结构示意图可表示为: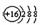
16、( )下列说法中正确的是
A 非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B 非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C 最外层有2个电子的原子都是金属原子
D 最外层有5个电子的原子都是非金属原子
15、( )A、B、C、D、E是同一周期的五种主族元素,A与B的最高氧化物对应的水化物呈碱
性,且碱性B>A;C和D的气态氢化物稳定性为C>D;E是这五种元素中原子半径最
小的元素,则它们的原子序数由小到大的的顺序为
A ABCDE B CDABE C BADCE D ECDBA
14、( )X、Y、Z三种主族元素的离子具有相同的电子层结构。X的离子半径大于Y的离子
半径,Y可与Z形成ZY2型的离子化合物,则三种元素原子序数的关系是
A X>Y>Z B Z>X>Y C Z>Y>X D Y>X>Z
13、( )根据中学化学教材所附元素周期表判断,下列叙述正确的是
A 同周期ⅡA和ⅢA族元素原子序数的差值可能为1、11、24
B L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C 原子最外层有1或2个电子的元素一定在ⅠA或ⅡA族
D 所含元素种数最多的族是第Ⅷ族
12、( )某元素R的含氧酸根离子符号是RO3-,能发生如下反应:RO3-+6I-+6H+=R-+3I2+3H2O
则该元素R的气态氢化物的化学式是
A HR B H2R C RH3 D 不能确定
11、( )下列说法中正确的是
A 原子晶体和分子晶体中一定只含有共价键
B 非极性分子中一定含有非极性键
C 只由极性键构成的分子一定是极性分子
D 由极性键构成的双原子分子一定是极性分子
10、( )只含极性键的非极性分子是①BF3(平面正三角型分子) ②CCl4 ③NH3 ④H2O
⑤CH3Cl ⑥CS2 ⑦SiO2 ⑧N2
A ①②⑥ B ①②⑥⑦ C ②⑤③ D ①②③⑥
9、( )下列各项中表达正确的是
A
F-的结构示意图: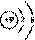 B CO2的分子模型示意图:
B CO2的分子模型示意图:
C
CaCl2的电子式:Ca2+[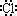 ]-2
D N2的结构式:︰N≡N︰
]-2
D N2的结构式:︰N≡N︰
8、( )下列物质中,含有非极性键的离子化合物是
A H2S B MgCl2 C CaC2 D Ca(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com