
题目列表(包括答案和解析)
36.[化学--选修化学与技术](15分)
海水中溶解了大量的气体物质和各种盐类。人类在陆地上发现的100多种元素,在海水中可以找到80多种。海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景。回答下列问题:
⑴ 蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但由于使用大量燃煤,因此能耗多、排污量大。为克服蒸馏法海水淡化的缺陷,请你对蒸馏法淡化海水的工艺提出一条改进建议 。
⑵ 使用离子交换树脂与水中的离子进行交换也是常用的水处理技术。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式 .。
⑶ 空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):

① 反应②的离子方程式为 ; ② 从反应③后的四氯化碳溶液中分离出单质溴的方法是 。
⑷ 苦卤中含有NaCl、MgCl2、KCl、MgSO4。用简要的文字说明如何测定苦卤中MgCl2的含量
35. [物理--选修3-5](15分)
(1)(5分)下列说法中错误的是( )
A.卢瑟福通过实验发现了质子的核反应方程为He+N→O+H
B.铀核裂变的核反应是:U→Ba+Kr+2n
C.质子、中子、α粒子的质量分别为m1、m2、m3,质子和中子结合成一个α粒子,释放的能量是(2m1+2m2-m3)c2
D.原子从a能级状态跃迁到b能级状态时发射波长为λ1的光子;原子从b能级状态跃迁到c能级状态时吸收波长为λ2的光子,已知λ1>λ2,那么原子从a能级状态跃迁到c能级状态时将要吸收波长为的光子
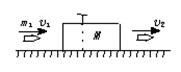 ⑵(10分)质量为M=2 kg的木板若固定在光滑的水平地面上,质量为m=0.04
kg的子弹以速度v1=500 m/s射入,射出时子弹
⑵(10分)质量为M=2 kg的木板若固定在光滑的水平地面上,质量为m=0.04
kg的子弹以速度v1=500 m/s射入,射出时子弹
速度v2=300 m/s,如图所示,今将钉子拔掉,
子弹穿出木块后的速度多大?
(设前后两次子弹和木块的作用力相同)
34. [物理--选修3-4](15分)
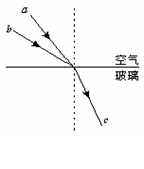
(1)(5分)如图所示,两束单色光a、b自空气射向玻璃,
经折射后形成复合光束c.下列说法中正确的是( )
A.从玻璃射向空气,a光的临界角小于b光的临界角
B.玻璃对a光的折射率小于玻璃对b光的折射率
C.经同一双缝所得干涉条纹,a光条纹宽度小于b光条纹宽度
D.在玻璃中,a光的速度等于b光的速度
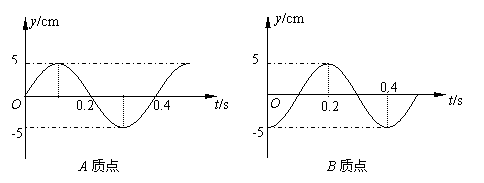 (2)(10分)如图所示是一列横波上A、B两质点的振动图象,该波由A传向B,两质点沿波的传播方向上的距离Δx=4.0m,波长大于3.0m,求这列波的波速.
(2)(10分)如图所示是一列横波上A、B两质点的振动图象,该波由A传向B,两质点沿波的传播方向上的距离Δx=4.0m,波长大于3.0m,求这列波的波速.
33. [物理--选修3-3](15分)
(1)(5分)下列说法中正确的是________
A.液体表面层分子间距离大于液体内部分子间距离,液体表面存在张力
B.扩散运动就是布朗运动
C.大颗粒的盐磨成细盐,就变成了非晶体
D.第二类永动机虽然不违反能量守恒定律,但它是制造不出来的
(2)(10分)图中A、B气缸的长度和截面积均为30cm和20cm2, C是可在气缸内无摩擦滑动的、体积不计的活塞,D为阀门。整个装置均由导热材料制成。起初阀门关闭,A内有压强PA=2.0×105帕的氮气。B内有压强PB=1.0×105帕的氧气。阀门打开后,活塞C向右移动,最后达到平衡。求:
①活塞C移动的距离及平衡后B中气体的压强;
②活塞C移动过程中A中气体是吸热还是放热(简要说明理由)。(假定氧气和氮气均为理想气体,连接气缸的管道体积可忽略)

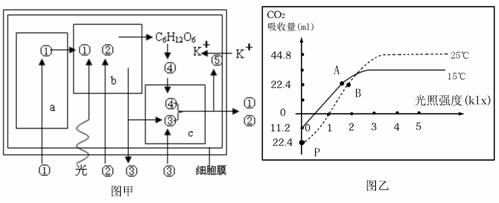
32.(11分)下图甲是某植物细胞代谢过程示意图(图中数字代表物质,a、b、c代表细胞器),图乙是该植物置于密闭容器内1小时CO2的变化曲线图(标准状况)。
 根据图中所给信息回答:
根据图中所给信息回答:
 (1)图甲中细胞器a是
,物质④是 。
(1)图甲中细胞器a是
,物质④是 。
(2)图甲中细胞器b、c增大膜面积的方式分别是
。
(3)根据图乙分析,在15℃、lklx光照条件下,
该植物5小时内光合作用固定CO2 mL;
A点总光合作用强度 B点(填大于、
小于或等于);P点为曲线在纵轴上的交点,
它上下移动的主要影响因素是 。
(4)在条件不变的情况下,若以O2吸收量为观测指标,在图丙中画出该植物在密闭容器内15℃条件下1小时O2的变化曲线图 。
(5)将叶绿体置于pH为4的酸性溶液中,直到基质的pH也达到4,然后将其取出,再置于pH为8的溶液中,这时发现叶绿体中开始合成ATP。联系所学知识解释上述实验现象。 (2分)
(二)选考题。33~40是选考题。请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题作答,并将答题纸上所选题目后的方框“涂黑”( )。注意所答题目的题号必须与所选题目题号相同,并且在解答过程中写清每问的小题号。如果多做,则每学科按所做第一题计分。
31.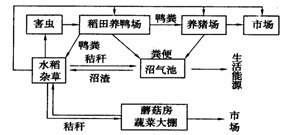 (8分)下图是我国南方开始尝试的农业生态系统的结构模式图,它利用雏鸭旺盛的杂食性,吃掉稻田里的杂草和害虫,用作物养猪、养鸭,用秸秆培育蘑菇、生产沼气,猪鸭粪、沼渣肥田。请据图回答:
(8分)下图是我国南方开始尝试的农业生态系统的结构模式图,它利用雏鸭旺盛的杂食性,吃掉稻田里的杂草和害虫,用作物养猪、养鸭,用秸秆培育蘑菇、生产沼气,猪鸭粪、沼渣肥田。请据图回答:
(1)该生态系统的能量最终来源是 。鸭子与作物害虫之间的关系是 。
(2)下列对该生态系统功能的描述中不正确的是(多选)
A.这种设计比传统农业生产模式提高了能量利用率
B.这种设计使能量持续高效流向对人类最有益的部分
C.图示表明,能量在一些环节可以循环利用
D.产甲烷杆菌与蘑菇的主要区别是前者是分解者,后者是生产者
E.猪和鸭子既是竞争关系又是捕食关系
F.蘑菇和大棚蔬菜之间具有种间互助的特征
(3)在生态系统中,基本组成元素能在生物群落和无机环境中不断循环,为什么还要往农田中不断施加氮肥?
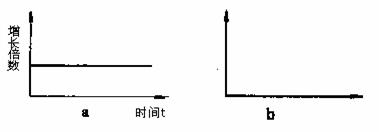
(4)下图a是某段时间内沼气池中产甲烷杆菌的种群增长率曲线,请在下图b中画出这段时间的种群数量变化曲线。
30.(11分)请回答下列关于下丘脑对人体部分生理活动调节过程的问题。图中甲、乙、丙表示内分泌腺,字母表示激素,数字表示生理活动。其中激素C的分泌受H的调节。(括号内填字母、数字与甲、乙、丙,横线上写文字)。
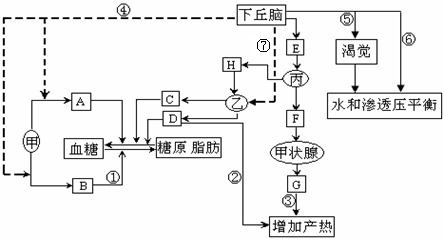
(1)寒冷刺激时,以神经调节为主的生理活动是[ ]。
(2)在寒冷环境下人体直接参与产热调节的激素有[ ] 与[ ] 。E可能是 。
(3)甲状腺能参与体温调节,是因为 。
(4)若高盐饮食后不喝水,机体通过⑥的调节过程是:___________________。
(5)图中显示促进血糖升高的激素是[ ]。B除了图示的作用外,还可以通过促进_________________作用调节血糖平衡。
(6)为验证胰岛素能降血糖,某同学给几只健康的小鼠腹腔注射一定剂量的胰岛素溶液(用酸性生理盐水配制),观察现象,若出现惊厥,则达到目的。为了使该实验更加严密,需要完善的是(多选题)
A.为使反应出现得较快且明显,实验前应将小鼠饥饿处理,以消耗肝糖原。
B.应设置注射等量酸性生理盐水的对照组,且注射的部位、方法同实验组。
C.应设置口服胰岛素的实验组,对照组灌喂等量的清水。
D.出现惊厥现象后,还应对其中的一半注射葡萄糖液抢救,另一半不予抢救。
29.回答下列有关遗传学的问题。(共9分)
I.人类遗传病发病率逐年增高,相关遗传学研究备受关注。根据以下信息回答问题:

(1)上图为两种遗传病系谱图,甲病基因用F、f表示,乙病基因用B、b表示,Ⅱ-4无致病基因。甲病的遗传方式为 ,乙病的遗传方式为 。
(2)Ⅱ-2的基因型为 ,Ⅲ-1的基因型为 ,如果Ⅲ-2与Ⅲ-3婚配,生出正常孩子的概率为 。
(3)采取____措施,可估计遗传病的再发风险率并提出预防措施。
II.下图表示人体部分代谢途径,基因为ABC时,代谢可正常进行,否则会引起相应的疾病;请回答:
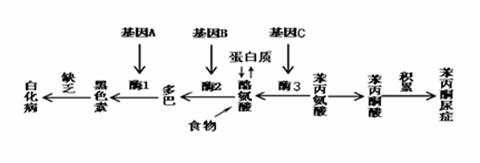
(1)某人基因型为AABBCc,其细胞内基因C突变为c,但其只患苯丙酮尿症却没患白化病,原因是: 。
(2)若已知酶3的氨基酸序列,能否精确推知编码酶3的基因C的具体的碱基序列? 。理由是: 。
28. (14分) 环境问题备受世界关注。化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素。
 (1)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白,反应方程式可表示为:CO+Hb·O2
O2+Hb·CO
(1)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白,反应方程式可表示为:CO+Hb·O2
O2+Hb·CO
实验表明,c(Hb·CO)即使只有c(Hb·O2)的 1/50,也可造成人的智力损伤。
已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol·L-1,若使c(Hb·CO)小于c(Hb·O2)的 1/50,则吸入肺部CO的浓度不能超过_________mol·L-1。
(2)汽车尾气治理的方法之一是在汽车的排气管上安装一个“催化转化器”。
 已知反应2NO(g) + 2CO(g) N2(g)
+ 2CO2(g) △H=-113kJ·mol-1
已知反应2NO(g) + 2CO(g) N2(g)
+ 2CO2(g) △H=-113kJ·mol-1
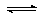
①为了模拟催化转化器的工作原理,在t℃时,将2 molNO与1 mol CO充入lL反应容器中,反应过程中NO(g)、CO(g)、N2(g)物质的量浓度变化如右下图所示。反应进行到15min时,NO的平均反应速率为 ,
 ②观察在20 min~30 min内N2(g)发生变化的曲线图,判断引起该变化的条件可能是
;
②观察在20 min~30 min内N2(g)发生变化的曲线图,判断引起该变化的条件可能是
;
a.加入催化剂
b.降低体系温度
c.缩小容器体积为0.5L
d.增加CO2的物质的量
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。
 已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
830 |
1000 |
|
平衡常数K |
10 |
9 |
1 |
0.6 |
试回答下列问题
①上述正向反应是: 反应(填“放热”、“吸热”)。
②某温度下上述反应平衡时,恒容、升高温度,正反应速率 (填“增大”、“减小”或“不变”),容器内混合气体的压强 (填“增大”、“减小”或“不变”)。
③在830℃发生上述反应,以下表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D)。
|
|
A |
B |
C |
D |
|
n(CO2) |
3 |
1 |
0 |
1 |
|
n(H2) |
2 |
1 |
0 |
1 |
|
n(CO) |
1 |
2 |
3 |
0.5 |
|
n(H2O) |
5 |
2 |
3 |
2 |
27.(15分)某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为____________________________;
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去;①说明乙二酸具有_____________(填“氧化性”、“还原性”或“酸性”);②请配平该反应的离子方程式:
____ MnO4– + ___ H2C2O4 + ____ H+ = ____ Mn2+ + ___ CO2↑ + ____H2O
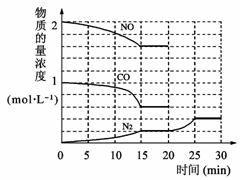
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:
①上述装置中,D的作用是__________________,
②乙二酸分解的化学方程式为_____________________________________;
(4)该小组同学将2.52 g草酸晶体(H2C2O4·2H2O)加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是___________________________________(用文字简单表述),该溶液中各离子的浓度由大到小的顺序为:___________________(用离子符号表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com