
题目列表(包括答案和解析)
3.比较5个SO2分子和5个CO2分子,含量一样的是( )。
A.氧分子 B.氧原子 C.氧元素 D.氧气
2.下列计算错误的是( )。
A.Mg(OH)2的相对分子质量:24 +(16 + 1)×2 = 58
B.SO2中硫元素与氧元素的质量比:1:1
C.NH4NO3中氮元素的质量分数: ×100% = 17.5%
×100% = 17.5%
D.18 g水(H2O)中含氢元素的质量:18 g×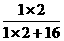 = 2 g
= 2 g
1.2CO2表示( )。
A.2个二氧化碳分子 B.2个碳原子和4个氧原子
C.2个碳原子和2个氧分子 D.2个碳原子和2个氧原子
15、

 解释:根据纯度等于纯物质的质量与该物质的质量之比再乘100%,首先要算出钙片中葡萄糖酸钙的质量,葡萄糖酸钙的质量可以根据补充钙质0.5g计算。
解释:根据纯度等于纯物质的质量与该物质的质量之比再乘100%,首先要算出钙片中葡萄糖酸钙的质量,葡萄糖酸钙的质量可以根据补充钙质0.5g计算。


 答案:(C6H11O7)2Ca中钙元素的质量分数:
答案:(C6H11O7)2Ca中钙元素的质量分数: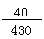
 ×100%≈9.3%。
×100%≈9.3%。


 则补充钙质0.5g需要(C6H11O7)2Ca的质量:
则补充钙质0.5g需要(C6H11O7)2Ca的质量: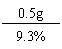
 ≈5.376g。
≈5.376g。


 所以钙片中葡萄糖酸钙的质量分数:
所以钙片中葡萄糖酸钙的质量分数: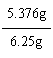
 ×100%≈86.0%。
×100%≈86.0%。









14、

 解释:C20H12的相对分子质量=碳的相对原子质量×碳的原子个数+氢的相对原子质量×氢的原子个数=12×20+1×12=252;
解释:C20H12的相对分子质量=碳的相对原子质量×碳的原子个数+氢的相对原子质量×氢的原子个数=12×20+1×12=252;


 C20H12中碳元素的质量分数为:
C20H12中碳元素的质量分数为:
 ×100%=
×100%=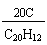
 ×100%=
×100%=



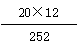
 ×100%=95.2% ;
×100%=95.2% ;


 C20H12中碳氢元素的质量比为:(碳的相对分子质量×碳的原子个数) :(氢的相对分子质量×氢的原子个数)=20C :12H =(12×20) :(1×12)=20 :1
C20H12中碳氢元素的质量比为:(碳的相对分子质量×碳的原子个数) :(氢的相对分子质量×氢的原子个数)=20C :12H =(12×20) :(1×12)=20 :1


 答案:(1)C20H12的相对分子质量=12×20+1×12=252;
答案:(1)C20H12的相对分子质量=12×20+1×12=252;


 (2)C20H12中碳元素的质量分数为:
(2)C20H12中碳元素的质量分数为: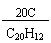
 ×100%=
×100%=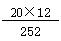
 ×100%=95.2% ;
×100%=95.2% ;


 (3)C20H12中碳氢元素的质量比为:20C :12H =(20×12) :(12×1)=20 :1
(3)C20H12中碳氢元素的质量比为:20C :12H =(20×12) :(12×1)=20 :1


 点拨:根据化学式计算物质的相对分子质量、某元素的质量分数和各元素的质量比是根据化学式进行计算的基本题型,一定要掌握计算方法。
点拨:根据化学式计算物质的相对分子质量、某元素的质量分数和各元素的质量比是根据化学式进行计算的基本题型,一定要掌握计算方法。
13、

 解释:因为该物质是有机物,所以还含有的另一种元素是碳元素;因为有5个氧原子,氧元素的质量分数约为46.0%,那么该有机物的相对分子质量为:(16×5)÷46.0%==174;因为,氢元素质量分数约为5.75%,所以氢的原子个数为:(174×5.75%)÷1==10,碳的原子个数为:[174-(16×5)-(10×1)] ÷12==7,所以该有机物的化学式为:C7H10O5。
解释:因为该物质是有机物,所以还含有的另一种元素是碳元素;因为有5个氧原子,氧元素的质量分数约为46.0%,那么该有机物的相对分子质量为:(16×5)÷46.0%==174;因为,氢元素质量分数约为5.75%,所以氢的原子个数为:(174×5.75%)÷1==10,碳的原子个数为:[174-(16×5)-(10×1)] ÷12==7,所以该有机物的化学式为:C7H10O5。


 答案为:(1)碳 (2)174 (3)C7H10O5
答案为:(1)碳 (2)174 (3)C7H10O5
12、

 解释:元素符号可以表示一个原子,三个氧原子是在氧的元素符号前面加上数字3;化学式的微观意义就可以表示一个该分子,一个氯化氢分子就可用氯化氢的化学式表示;磷元素用磷的元素符号表示就可以了;三个碳酸根离子就是在碳酸根离子符号前面加上数字3。
解释:元素符号可以表示一个原子,三个氧原子是在氧的元素符号前面加上数字3;化学式的微观意义就可以表示一个该分子,一个氯化氢分子就可用氯化氢的化学式表示;磷元素用磷的元素符号表示就可以了;三个碳酸根离子就是在碳酸根离子符号前面加上数字3。


 答案:(1)3O;(2)HCl;(3)P; (4)3CO32-
答案:(1)3O;(2)HCl;(3)P; (4)3CO32-
11、

 答案:②④⑥⑦⑧。解释:氧气不是由原子构成的它的元素符号不能表示氧气,②错;因为Al为+3价O为-2价,根据化合物中各元素的化合价代数和为零氧化铝的化学式为Al2O3,④错;锰酸钾的化学式为K2MnO4
,⑥错;在化合物中表示原子个数的小写数字要标在相应元素的右下角,⑦⑧错。
答案:②④⑥⑦⑧。解释:氧气不是由原子构成的它的元素符号不能表示氧气,②错;因为Al为+3价O为-2价,根据化合物中各元素的化合价代数和为零氧化铝的化学式为Al2O3,④错;锰酸钾的化学式为K2MnO4
,⑥错;在化合物中表示原子个数的小写数字要标在相应元素的右下角,⑦⑧错。


 点拨:单质:金属、稀有气体和固态非金属它们是由原子直接构成的,用元素符号表示;非金属气体在元素符号右下角写上表示份子中所含原子数的数字。
点拨:单质:金属、稀有气体和固态非金属它们是由原子直接构成的,用元素符号表示;非金属气体在元素符号右下角写上表示份子中所含原子数的数字。


 化合物:氧化物的化学式一般是金属元素写在右方,另一种元素写在左方;金属元素与非金属元素组成的化合物,一般是金属元素写在符号左边,非金属元素写在右边。
化合物:氧化物的化学式一般是金属元素写在右方,另一种元素写在左方;金属元素与非金属元素组成的化合物,一般是金属元素写在符号左边,非金属元素写在右边。
10、
 C,解释:从宏观上看,偏二甲肼是由碳、氢、氧三种元素组成的。从微观上分析,偏二甲肼是由分子构成的,偏二甲肼分子是由碳原子、氢原子和氮原子构成,且1个偏二甲肼分子中含有2个碳原子、8个氢原子和2个氮原子。偏二甲肼中碳、氢、氧三种元素的质量之比为6 :2 :7,原子个数比才是1 :4 :1。
C,解释:从宏观上看,偏二甲肼是由碳、氢、氧三种元素组成的。从微观上分析,偏二甲肼是由分子构成的,偏二甲肼分子是由碳原子、氢原子和氮原子构成,且1个偏二甲肼分子中含有2个碳原子、8个氢原子和2个氮原子。偏二甲肼中碳、氢、氧三种元素的质量之比为6 :2 :7,原子个数比才是1 :4 :1。
9、
 A,解释:B中表示的是2个氢原子,B错;C中表示的是1个氮分子,C错;D中表示的是2个氧离子,D错。
A,解释:B中表示的是2个氢原子,B错;C中表示的是1个氮分子,C错;D中表示的是2个氧离子,D错。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com