
题目列表(包括答案和解析)
2、


 A 解析:当氢与氧气完全反应时,生成18g水,由水的质量可以求出参加反应的氢气和氧气的的质量分别是2g和16g,即其质量比为1:8。
A 解析:当氢与氧气完全反应时,生成18g水,由水的质量可以求出参加反应的氢气和氧气的的质量分别是2g和16g,即其质量比为1:8。
1、


 C 解析:利用化学方程式可以计算出NH3和CO2的质量比为17 :44,列出比例式即可计算出生成4.4gCO2时,同时生成NH3的质量为1.7g。
C 解析:利用化学方程式可以计算出NH3和CO2的质量比为17 :44,列出比例式即可计算出生成4.4gCO2时,同时生成NH3的质量为1.7g。



 点拨:44是二氧化碳的相对分子质量,4.4是因为44的1/10,口算即可得出生成的氨气质量的数值为氨气相对分子质量17的1/10,即1.7g。在利用化学方程式的计算中,有很多类似的计算,利用其倍数关系,可快速得出答案。
点拨:44是二氧化碳的相对分子质量,4.4是因为44的1/10,口算即可得出生成的氨气质量的数值为氨气相对分子质量17的1/10,即1.7g。在利用化学方程式的计算中,有很多类似的计算,利用其倍数关系,可快速得出答案。
15、


 我国又迎来了一个航天高峰,继“神舟六号”宇宙飞船成功发射之后,“神舟七号”又发射在即。“神舟六号”携带了50kg的氧气,供宇航员呼吸之用,同时还有一套完整的系统用来吸收二氧化碳。有些宇宙飞船内是通过盛有氢氧化锂的过滤网来除去舱内所含的二氧化碳,反应的化学方程式如下:
我国又迎来了一个航天高峰,继“神舟六号”宇宙飞船成功发射之后,“神舟七号”又发射在即。“神舟六号”携带了50kg的氧气,供宇航员呼吸之用,同时还有一套完整的系统用来吸收二氧化碳。有些宇宙飞船内是通过盛有氢氧化锂的过滤网来除去舱内所含的二氧化碳,反应的化学方程式如下:



 2LiOH+CO2===
Li2CO3+H2O
2LiOH+CO2===
Li2CO3+H2O



 (1)试计算1g氢氧化锂所能吸收二氧化碳的质量。
(1)试计算1g氢氧化锂所能吸收二氧化碳的质量。



 (2)若用氢氧化钾来代替氢氧化锂,试计算1g氢氧化钾所能吸收的二氧化碳的质量。
(2)若用氢氧化钾来代替氢氧化锂,试计算1g氢氧化钾所能吸收的二氧化碳的质量。



 (反应的化学方程式为2KOH+CO2===K2CO2+H2O)
(反应的化学方程式为2KOH+CO2===K2CO2+H2O)



 (3)利用(1)和(2)所得的结果,试解释为什么宇宙飞船选用氢氧化锂来吸收二氧化碳比用氢氧化钾更好?
(3)利用(1)和(2)所得的结果,试解释为什么宇宙飞船选用氢氧化锂来吸收二氧化碳比用氢氧化钾更好?



 (4)若每位宇航员每天所呼出的二氧化碳平均是502:,现有4位宇航员在进行一项为期7天的太空任务,试计算在宇宙飞船上应携带氢氧化锂的质量。(在宇宙飞船内的温度和气压下,二氧化碳气体的密度为1.833g/L)
(4)若每位宇航员每天所呼出的二氧化碳平均是502:,现有4位宇航员在进行一项为期7天的太空任务,试计算在宇宙飞船上应携带氢氧化锂的质量。(在宇宙飞船内的温度和气压下,二氧化碳气体的密度为1.833g/L)











 紧跟教材训练答案
紧跟教材训练答案
14、


 解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8 g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:




|
小柯:实验测定法
|
    小妍:计算法 小妍:计算法 |
小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300mL。                |
解:高锰酸钾中氧元素的质量分数        = = ×100% ×100%        = =     氧气的质量为:15.8g×40.5%=6.4g 氧气的质量为:15.8g×40.5%=6.4g    答:15.8g高锰酸钾完全分解产生氧气6.4g。 答:15.8g高锰酸钾完全分解产生氧气6.4g。 |



 请回答:
请回答:



 (1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出
(1)在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出



 15.8 g高锰酸钾分解后所产生的氧气质量为--g(结果保留一位小数)。
15.8 g高锰酸钾分解后所产生的氧气质量为--g(结果保留一位小数)。



 (2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质
(2)大家经过讨论,认为小妍的计算方法明显错误,本题不能采用该方法计算氧气质



 量的一项理由是( )。
量的一项理由是( )。



 A.高锰酸钾中含氧元素
A.高锰酸钾中含氧元素



 B.锰酸钾和二氧化锰中含氧元素
B.锰酸钾和二氧化锰中含氧元素



 C.氧气中含氧元素
C.氧气中含氧元素



 (3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。
(3)请计算15.8 g高锰酸钾完全分解所产生的氧气质量为____________________g。



 (4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,



 请提出一种合理的猜测:_______________________________。
请提出一种合理的猜测:_______________________________。
13、


 在一密闭容器内盛有20g H2、O2、N2的混合气体,在实验室中某同学误加热此容器,混合气体发生了爆炸,冷却后,测知生成的H2O为18g,请帮助该同学判断一下,剩余气体是
。
在一密闭容器内盛有20g H2、O2、N2的混合气体,在实验室中某同学误加热此容器,混合气体发生了爆炸,冷却后,测知生成的H2O为18g,请帮助该同学判断一下,剩余气体是
。
12、


 水通电分解的化学方程式为 。如果电解3.6g水,则生成氢气的质量为
g,生成氧气的质量为 g。
水通电分解的化学方程式为 。如果电解3.6g水,则生成氢气的质量为
g,生成氧气的质量为 g。
11、


 在C+O2
在C+O2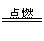
 CO2的反应中, 份质量的碳与
份质量的氧气反应生成
CO2的反应中, 份质量的碳与
份质量的氧气反应生成



 份质量的二氧化碳。
份质量的二氧化碳。




10、



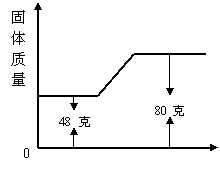
 镁在空气中燃烧,生成氧化镁,其固体质量变化可用图表示,则(80-48)克表示的质量为:
镁在空气中燃烧,生成氧化镁,其固体质量变化可用图表示,则(80-48)克表示的质量为:








|























 A.
生成物MgO的质量
B. 参加反应O2的质量
A.
生成物MgO的质量
B. 参加反应O2的质量



 C. 参加反应的镁的质量
D. 生成物MgO与参加反应的O2的质量和
C. 参加反应的镁的质量
D. 生成物MgO与参加反应的O2的质量和
9、


 A、B、C三种物质各15 g,它们化合时只能生成30 g新物质D。若增加10 g A,则反应停止后,原反应物中只余C。根据上述条件推断下列说法中正确的是( )
A、B、C三种物质各15 g,它们化合时只能生成30 g新物质D。若增加10 g A,则反应停止后,原反应物中只余C。根据上述条件推断下列说法中正确的是( )



 A.第一次反应停止后,B剩余9 g
B.第二次反应后,D的质量为50 g
A.第一次反应停止后,B剩余9 g
B.第二次反应后,D的质量为50 g




 C.反应中A和B的质量比是3∶2
D.反应中A和C的质量比是5∶2
C.反应中A和B的质量比是3∶2
D.反应中A和C的质量比是5∶2
8、


 一定质量的铜粉和碳粉的混合物,在空气中充分灼烧后其固体与原混合物的质量不变,则原混合物中铜粉和碳粉的质量比为( )
一定质量的铜粉和碳粉的混合物,在空气中充分灼烧后其固体与原混合物的质量不变,则原混合物中铜粉和碳粉的质量比为( )



 A、4:1
B、2:1 C、3:2 D、1:1
A、4:1
B、2:1 C、3:2 D、1:1




湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com