
题目列表(包括答案和解析)
13、


 (09河南)
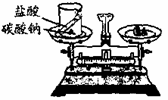
(2分)某同学按右图装置对质量守恒定律进行实验
(09河南)
(2分)某同学按右图装置对质量守恒定律进行实验


 探究,结果观察到反应后天平不平衡,由此得出这个化学反应
探究,结果观察到反应后天平不平衡,由此得出这个化学反应


 不遵守质量守恒定律的结论。这个结论是否正确?为什么?
不遵守质量守恒定律的结论。这个结论是否正确?为什么?


 关键词:质量守恒定律的应用
关键词:质量守恒定律的应用


 答案:(2分)不正确。(1分) 因为参加反应的碳酸钠和盐酸的质量总和等于反应后生成的氯化钠、水和二氧化碳的质量总和,因此这个化学反应遵守质量守恒定律。 (或由于生成的二氧化碳气体逸出,使反应后天平不平衡等。)(1分)
答案:(2分)不正确。(1分) 因为参加反应的碳酸钠和盐酸的质量总和等于反应后生成的氯化钠、水和二氧化碳的质量总和,因此这个化学反应遵守质量守恒定律。 (或由于生成的二氧化碳气体逸出,使反应后天平不平衡等。)(1分)
12.

 (09湖北黄石市)在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9:22,若2.6gA与B完全反应,生成8.8gD,则在此反应中B与D的质量比为
(09湖北黄石市)在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9:22,若2.6gA与B完全反应,生成8.8gD,则在此反应中B与D的质量比为


 A.4:9
B.8:1
C.10:11
D.31:44
A.4:9
B.8:1
C.10:11
D.31:44


 关键词: 质量守恒定律
关键词: 质量守恒定律


 答案:C
答案:C


 简答和填空
简答和填空
11.

 (09山东德州)2008年4月8日安徽省阜南县一所小学又发生一起误把亚硝酸钠当食盐的中毒事件,确保食品安全的警钟再次敲响,亚硝酸钠(NaNO2)外观与食盐极相似,有咸味,区别它们的有效方法是隔绝空气加热,没有明显变化的是食盐,能分解放出刺激性气味气体的是亚硝酸钠,此气体可能是
(09山东德州)2008年4月8日安徽省阜南县一所小学又发生一起误把亚硝酸钠当食盐的中毒事件,确保食品安全的警钟再次敲响,亚硝酸钠(NaNO2)外观与食盐极相似,有咸味,区别它们的有效方法是隔绝空气加热,没有明显变化的是食盐,能分解放出刺激性气味气体的是亚硝酸钠,此气体可能是


 A、SO2
B、NH3
C、N2
D、NO2
A、SO2
B、NH3
C、N2
D、NO2


 关键词: 质量守恒定律的内容
关键词: 质量守恒定律的内容


 答案: D
答案: D
10.

 (09江苏徐州)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是
(09江苏徐州)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是
|
物质 |
M |
N |
Q |
P |
|
反应前质量(g) |
18 |
1 |
2 |
32 |
|
反应后质量(g) |
X |
26 |
2 |
12 |
A.该变化的基本反应类型是分解反应 B.反应后物质M的质量为l3g


 C.反应中N、P的质量比为5:4 D.物质Q可能是该反应的催化剂
C.反应中N、P的质量比为5:4 D.物质Q可能是该反应的催化剂


 关键词: 质量守恒定律的计算 质量守恒定律的应用
关键词: 质量守恒定律的计算 质量守恒定律的应用


 答案: A
答案: A
9.

 (09江苏徐州)科学的假设与猜想是科学探究的先导和价值所在。在下列假设(猜想)引导下的探究肯定没有意义的选项是
(09江苏徐州)科学的假设与猜想是科学探究的先导和价值所在。在下列假设(猜想)引导下的探究肯定没有意义的选项是


 A.探究二氧化硫和水反应可能有硫酸生成
A.探究二氧化硫和水反应可能有硫酸生成


 B.探究钠与水的反应产生的气体可能是氧气
B.探究钠与水的反应产生的气体可能是氧气


 C.探究镁条表面灰黑色的物质可能只是氧化镁
C.探究镁条表面灰黑色的物质可能只是氧化镁


 D.探究铜在灼烧时出现的黑色物质可能是炭黑
D.探究铜在灼烧时出现的黑色物质可能是炭黑


 关键词: 质量守恒定律的内容
关键词: 质量守恒定律的内容


 答案: D
答案: D
8.


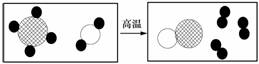 (09山东烟台)下图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子。下列说法不正确的是
(09山东烟台)下图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子。下列说法不正确的是


 (A)图中能表示氢分子的是“
(A)图中能表示氢分子的是“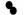 ”
”


 (B)反应前后,原子的种类、数目不变
(B)反应前后,原子的种类、数目不变


 (C)该反应中共涉及两种单质和三种化合物
(C)该反应中共涉及两种单质和三种化合物


 (D)该反应中参加反应的两种分子的个数比为1
:1
(D)该反应中参加反应的两种分子的个数比为1
:1


 关键词: 质量守恒定律的内容
关键词: 质量守恒定律的内容


 答案: C
答案: C
7、

 (2009·重庆)根据化学方程式A+NaOH =B十H2O推断,B、A的相对分子质量相差 ( )
(2009·重庆)根据化学方程式A+NaOH =B十H2O推断,B、A的相对分子质量相差 ( )


 A.
12 B. 18
C.22 D.40
A.
12 B. 18
C.22 D.40


 关键词:质量守恒定律
关键词:质量守恒定律


 思路分析:根据质量守恒定律,A的相对分子质量+40=B的相对分子质量+18.
思路分析:根据质量守恒定律,A的相对分子质量+40=B的相对分子质量+18.


 答案:C
答案:C
6、

 (2009兰州) 关于化学反应A+B=C+D,下列说法中正确的是 C
(2009兰州) 关于化学反应A+B=C+D,下列说法中正确的是 C


 A.若生成物C和D分别是盐和水,则反应物一定是酸和碱
A.若生成物C和D分别是盐和水,则反应物一定是酸和碱


 B.若C是单质、D为化合物,则A和B中一定有一种是单质,一种是化合物
B.若C是单质、D为化合物,则A和B中一定有一种是单质,一种是化合物


 C.若B是酸,则C和D一定有一种是盐
C.若B是酸,则C和D一定有一种是盐


 D.若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g
D.若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g


 关键词:化学反应
关键词:化学反应


 思路分析:A金属氧化物和酸、非金属氧化物和碱反应都可以生成盐和水;B一氧化碳还原氧化铜;C中酸和金属、金属氧化物、碱或盐的反应中生成物都有盐;AB不是恰好完全反应,则生成的CD质量总和小于20g.
思路分析:A金属氧化物和酸、非金属氧化物和碱反应都可以生成盐和水;B一氧化碳还原氧化铜;C中酸和金属、金属氧化物、碱或盐的反应中生成物都有盐;AB不是恰好完全反应,则生成的CD质量总和小于20g.
5.

 将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X。测得反应前后物质的质量如下表:
将一定量的乙醇和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知物X。测得反应前后物质的质量如下表:
|
物 质 |
 乙醇 乙醇 |
氧气 |
二氧化碳 |
水 |
X |
|
反应前质量/g |
4.6 |
8 |
0 |
0 |
0 |
|
反应后质量/g |
0 |
0 |
4.4 |
5.4 |
m |
下列判断正确的是


 A.表中m的值为2.8
A.表中m的值为2.8


 B.X可能是该反应的催化剂
B.X可能是该反应的催化剂


 C.增加氧气的量可以减少X的生成
C.增加氧气的量可以减少X的生成


 D.物质X一定含有碳元素,可能含有氢元素
D.物质X一定含有碳元素,可能含有氢元素


 关键词: 质量守恒定律的应用
关键词: 质量守恒定律的应用


 答案:AC
答案:AC
4.

 用酸性高锰酸钾溶液可以测定室内空气的污染物甲醛的含量是否超标。相关反应的化学方程式是4KMnO4+5CH2O+6H2SO4=2K2SO4+4MnSO4+5X+11H2O,其中X的化学式为
用酸性高锰酸钾溶液可以测定室内空气的污染物甲醛的含量是否超标。相关反应的化学方程式是4KMnO4+5CH2O+6H2SO4=2K2SO4+4MnSO4+5X+11H2O,其中X的化学式为


 A.CO
B.CO2
C. H2CO3 D.K2CO3
A.CO
B.CO2
C. H2CO3 D.K2CO3


 关键词: 质量守恒定律的应用
关键词: 质量守恒定律的应用


 答案:B
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com