
题目列表(包括答案和解析)
15.如图所示,在水平匀强电场中,一端固定的丝线下方悬挂一个带正电的小球,小球带电量为q、质量为m,小球从最低点由静止释放,己知丝线能够摆过的最大角与竖直方向成60°,则下列说法正确的是
 A、电场强度的大小为E=
A、电场强度的大小为E=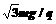
B、电场强度的大小为E=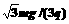
C、小球从最低点摆向最大偏角过程中,机械能增加
D、小球从最低点摆向最大偏角过程中,电势能增加
14.下列说法中不正确的是
A、布朗运动是液体分子对悬浮颗粒的碰撞作用不平衡造成的
B、容器中的气体对器壁的压强是由于大量气体分子频繁撞击器壁而产生的
C、用打气筒给自行车打气时,越向下压缩活塞越费劲,这时气体分子斥力的缘故。
D、用N表示阿伏德罗常数,M表示铜的摩尔质量,ρ表示铜的密度,那么一个铜原子所占空间的体积可表示为ρ/(MN)
13.将铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
|
编号 |
① |
② |
③ |
④ |
|
稀硝酸体积/mL |
100 |
200 |
300 |
400 |
|
剩余金属质量/g |
18.0 |
9.6 |
0 |
0 |
|
NO体积/mL |
2240 |
4480 |
6720 |
V |
下列计算结果正确的是
A、硝酸的浓度为4mol/L B、①中溶解了5.6gFe
C、②中溶解了9.6gCu D、④中V=6720mL
12.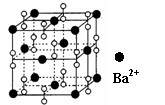 钡在氧气中燃烧时的得到一种钡的氧化物晶体,其晶体结构如下图所示,有关说法正确的是
钡在氧气中燃烧时的得到一种钡的氧化物晶体,其晶体结构如下图所示,有关说法正确的是
A、该晶体属于离子晶体
B、晶体的化学式为Ba2O2
C、该晶体晶胞结构与CsCl相似
D、与每个Ba2+距离相等且最近的Ba2+共有8个
11.下列各项操作中,不发生“先沉淀后溶解”现象的是
① 向饱和Na2CO3溶液中通入过量的CO2;
② 向Fe(OH)3胶体中逐滴滴入过量的稀H2SO4;
③ 向AgI胶体中逐滴加入过量的稀盐酸;
④ 向石灰水中通入过量的CO2; ⑤向硅酸钠溶液中逐滴加入过量的盐酸。
A、①②③ B、②③⑤ C、①②③⑤ D、①③⑤
10.对于密闭容器中的反应:N2(g)+3H2(g)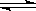 2NH3(g);△H<0,在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g);△H<0,在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
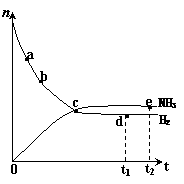 A、点a的反应速率比点b的小
A、点a的反应速率比点b的小
B、点 c处的正反应速率比逆反应速率大
C、点d (t1时刻) 的n(N2)比点 e (t2时刻) 处的n(N2)大
D、其他条件不变,773K下反应至t1时刻,此时画出
的两根平行线间的距离将一定会变大
9.在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中,加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,完全反应后,离子数目没有变化的是
A、Fe3+ B、Fe2+ C、Al3+ D、NH4+
8.金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式
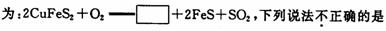
A、方框中的物质应为 Cu2S
B、O2只作氧化剂
C、SO2 既是氧化产物又是还原产物
D、若有 1 molSO2生成,则反应中有4 mol 电子转移
7.下列实验中,仪器的下端必须插入液面下的是
① 制备氢气的简易装置中用来加入稀硫酸的长颈漏斗
② 实验室用 MnO2和浓盐酸制备氯气装置中的分液漏斗
③ 用新制的FeSO4溶液和NaOH 溶液制备 Fe ( OH )2操作中的胶头滴管
④ 将氯气溶于水制取氯水时的导气管
⑤ 蒸馏石油时的温度计
A、③ ⑤ B、① ③ ④ C、② ④ ⑤ D、全部
6.氢氧燃料电池以H2为还原剂,O2为氧化剂,电极为多孔镍,电解液为30%的KOH溶
液,下列有关叙述正确的是
①负极反应为4OH--4e- =O2↑+2H2O
②负极反应H2+2OH- - 2e- =2H2O
③工作时正极区PH升高,负极区PH降低
④工作时溶液中阴离子移向正极
A、③④ B、②③ C、②④ D、①④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com