
题目列表(包括答案和解析)
15.在均匀的介质中,各质点的平衡位置在同一直线上,相邻两个质点的距离均为a ,如图甲所示,振动从质点13 开始并向左传播,其振动初速度方向竖直向下,经过时间t ,图中13 个质点第一次形成的波形图如图乙所示,则该波的周期T 和波速v 分别是
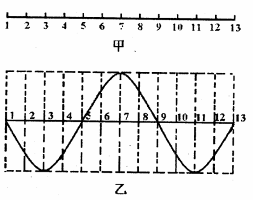 A.T=,v=16
A.T=,v=16
B.T=t,v=
C.T=,v=12
D.T=,v=
14.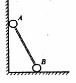 如图所示,两个质量都是,的小球 A 、 B 用轻杆连接后斜靠在墙上处于平衡状态,已知墙面光滑,水平地面粗糙,现将 A 球向上移动一小段距离,两球再次达到平衡,那么将移动后的平衡状态和原来的平衡状态比较,地面对 B 球的支持力 F .和摩擦力凡的大小变化情况是
如图所示,两个质量都是,的小球 A 、 B 用轻杆连接后斜靠在墙上处于平衡状态,已知墙面光滑,水平地面粗糙,现将 A 球向上移动一小段距离,两球再次达到平衡,那么将移动后的平衡状态和原来的平衡状态比较,地面对 B 球的支持力 F .和摩擦力凡的大小变化情况是
A.F1不变, F2增大
B.F1不变, F2减小
C.F1增大, F2 增大
D.Fl 增大, F2减小
13.已知 25 ℃ 时, AgI饱和溶液中 c ( Ag十)为 1.22×l0一8 mol / L , AgCl 的饱和溶液中 c ( Ag + )为 1.25×l0一 5 mol / L 。若在 5mL 含有 KCl 和 KI 各为 0 .01mol / L 的溶液中,加人 8mL0.01mol / L AgNO3 溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
A.c ( K+ ) > c ( NO3-)> c ( Ag + ) = c ( Cl一)+ c ( I一)
B.c ( K+ ) > c ( NO3-)> c ( Ag + ) > c ( Cl一)+ c ( I一)
C.c ( NO3-)>c ( K+ ) > c ( Ag + ) > c ( Cl一)+ c ( I一)
D.c ( K+ ) > c ( NO3-)>c ( Cl一)> c ( Ag + ) > + c ( I一)
12.短周期元素 X 、 Y 可以形成化合物 XY2。下列有关叙述正确的是
A.若 XY2是离子化合物,则 X 与 Y 的原子序数不可能相差 8
B.若 XY2是共价化合物,则 X 与 Y 的原子序数不可能相差 1
C.若 X 与 Y 的原子序数相差 5 ,则离子化合物 XY2不溶于水
D.若 X 与 Y 的原子序数相差 6 ,则共价化合物 XY2不溶于强碱溶液
11.我国首创的海水电池以铝为负极,铂网为正极,海水为电解质溶液。空气中的氧气与铝反应产生电流,电池总反应为: 4Al + 3O2+ 6HZO=4Al (OH )3 ,下列说法正确的是 A.电池工作时,电流由铝电极沿导线流向铂电极
B.以网状的铂为正极,可增大与氧气的接触面积
C.为了增加海水的导电性,向海水中加人大量食盐
D.负极反应:O2+ 2HZO=4OH一-4e-
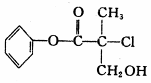
10.某有机物A 是农药生产中的一种中间体,其结构简式如右:下列有关叙述中正确的是
A.有机物A 属于芳香烃、
B.有机物A 可以和Br2的CCl4溶液发生加成反应 C.有机物A 和浓硫酸混合加热,可以发生消去反应
D.l mo1A 和足量的NaOH 溶液反应,最多可以消耗3mol NaOH
9.密度为dg/cm3的溶液VmL ,含有相对分子质量为M 的溶质mg ,其物质的量浓度为cmol / L ,溶质的质量分数为w%,下列表示式不正确的是
A.c = B.m=
 C.d =
D.w=
C.d =
D.w=
8.在等温等容条件下的反应:2A ( g ) +2B ( g )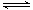 C(g ) + 3D ( g)。现分别从两条途径建立平衡:( I ) A 和B 的起始浓度均为2mol
/ L ; (II) C 和D 的起始浓度分别为2mol
/ L 和6mol / L 。下列叙述正确的是
A.I 和II 两途径最终达到平衡时,体系内混合气体的各物质的量相同
B.达到平衡时,I 途径混合气体密度为II
途径混合气体密度的2 倍
C.I 和II 两途径最终达到平衡时,体系内同种气体的体积分数相同
D.达到平衡时,I 途径的反应速率VA等于II 途径的反应速率VB
C(g ) + 3D ( g)。现分别从两条途径建立平衡:( I ) A 和B 的起始浓度均为2mol
/ L ; (II) C 和D 的起始浓度分别为2mol
/ L 和6mol / L 。下列叙述正确的是
A.I 和II 两途径最终达到平衡时,体系内混合气体的各物质的量相同
B.达到平衡时,I 途径混合气体密度为II
途径混合气体密度的2 倍
C.I 和II 两途径最终达到平衡时,体系内同种气体的体积分数相同
D.达到平衡时,I 途径的反应速率VA等于II 途径的反应速率VB
7.在0.lmol / L 的NaHSO3溶液中有如下关系: c ( Na + ) > c ( HSO3-)> c ( SO32-)> c ( H2SO3 ) 向该NaHSO3 溶液中慢慢地加人少量的NaOH 溶液,发生的主要反应的离子方程式为
A.SO32-+H2O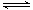 HSO3-十OH-
B.HSO3-十H2O
HSO3-十OH-
B.HSO3-十H2O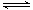 H2SO3
+ OH-
C.HSO3-十OH-
H2SO3
+ OH-
C.HSO3-十OH-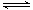 SO32-十H2O
D . H2SO3 + OH-
SO32-十H2O
D . H2SO3 + OH-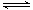 HSO3-十H2O
HSO3-十H2O
6.下列实验事实,可用同一反应原理解释的是 A.乙醇和水都能与钠反应放出氢气 B.烧碱和纯碱的溶液都呈碱性 C.C2H4和SO2 都能使溴水褪色 D.苯酚溶液和AgNO3 溶液遇溴水都产生沉淀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com