
题目列表(包括答案和解析)
2、竖直向上抛出一个小球,4S后落回出发点,则小球在2S内的位移(不计空气阻力)是A、10m B、20m ( )
C、0m D、40m
1、有两个物体的质量之比是1:3,两物体所在位置的高度之比是2:1,它们各自做自由落体运动,则( )
A、落地时的速度之比是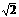 :1
:1
B、落地时的速度之比是1:1
C、下落过程中的加速度之比是1:2
D、下落时间是2:1
31.(20分)下图表示氮循环与动物体内有机物部分代谢途径,请分析回答:

(1)完成①、②过程的微生物分别是_______________、________________。
(2)完成③过程的细胞器是_________________。
(3)进行④过程首先要经过_______作用。促进⑤、⑥过程的激素分别是_____________、
____________________。
(4)某些微生物能够完成①过程,关键是由于有_________酶。
假如科学家想利用基因工程的方法,将编码该酶的基因转移到小麦胚细胞中,获取该基因的途径:一是从微生物的DNA分子直接分离,二是_________________________;
假如已经知道组成该酶的氨基酸序列,从理论上讲能不能准确确定其基因编码区的碱基序列?_____________,原因是______________________________________________,这对于生物体的生存有什么意义?_____________________________________________。
 (5)NO3-被吸收进入植物体内后,必须经过下列还原反应,生成NH3才能被植物体利用合成蛋白质:
(5)NO3-被吸收进入植物体内后,必须经过下列还原反应,生成NH3才能被植物体利用合成蛋白质:
①若将水稻幼苗培养在硝酸盐溶液中,则体内生成硝酸还原酶;若将水稻幼苗培养在无硝酸盐的培养液中,硝酸还原酶消失。这种现象说明硝酸还原酶是( )
A.还原酶 B.水解酶 C.组成酶 D.诱导酶
②给你提供两株生长状况相同的植物幼苗及药品、用具,请你设计一个实验,通过可观察现象验证钼是组成硝酸还原酶的必需元素,并预期实验现象。
步骤:
30、.(22分)1999年4月23日,在广州中山医科大学第一附属医院,我国首例试管婴儿出生,该女婴的父母身体健康。女婴的母亲7年前生下一男婴,孩子一岁后发病,最后死于脑出血。5年后,她第二次怀孕,怀孕6个月时,到医院抽羊水及脐带血诊断,发现胎儿是男孩,而且是血友病患者,遂引产。夫妇二人最后来到中山医院大学附属医院做试管婴儿。医生培养了7个可做活体检查的胚胎,并抽取每个胚胎1-2个细胞进行检查后,选择了两个活体胚胎进行移植,最后一个移植成功。据此资料回答下列问题:
(1)试管婴儿技术作为现代生物技术和母亲正常怀孕、生产的过程的相同之处是______________________ ______________________________
不同点在于____________________________ ____。
(2)血友病的遗传方式为___________________________________,如果用B和b表示正常基因和血友病基因,则父、母亲的基因型分别是______ 和______。如果该夫妇再生一男孩,患血友病的概率是_____________。
(3)医生抽取活检胚胎的1或2个细胞后,可通过观察______________判断早期胚胎的性别,你认为医生应选用_________性胚胎进行移植,原因是 。 应用现代生物技术,现在人们已能够选取最理想的胚胎,其基因型应该是_______。自然状态下,出现这样的胚胎的概率是_______。该实例体现了现代科学技术应用于社会和人类生活的重要意义。
29. (12分)
(12分)
由碳、氢、氧三元素组成的化合物M是预防心血管疾病的一种新药。M可发生如下变化:
已知B的蒸气密度是H2的22倍,并可发生银镜反应,M的相对分子质量为174,化合物C
中氧元素质量分数为54.2%,取一定质量的化合物C完全燃烧生成CO2和水的物质的量之比为4:3。试解答下列问题:
(1)写出下列化合物的结构简式:
B:_______;A:_________;E:________。
(2)化合物C分子中碳、氢、氧原子个数之比为N(C):N(H):N(O)=__________。
(3)M的分子式是:_________________________.
(4)写出符合上述框图转化关系的M的可能有的结构简式:________________________
28. (20分)
(20分)
(1)50mL1.0mol·L-1盐酸跟50mL1.1mol·L-1氢氧化钠溶液
在右图装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
①该实验装置有3处明显错误,分别是:
A ,B , C 。
②大小烧杯间如果不填满碎纸屑或塑料泡沫,对求得中和热
的数值有何影响?
A.偏低 B.偏高
C.无影响 D.无法判断
③当实验装置改正好后再做实验。
若改用60mL1.0mol·L-1盐酸跟50mL1.1mol·L-1氢氧化钠溶液进行反应,与上述实验相比,所放出的热量将 ,所求中和热数值将 。
A.偏低 B.偏高 C.相等 D.无法判断
④若用相同浓度和体积的氨水代替上述实验中的氢氧化钠溶液,测得中和热的数值
A.偏低 B.偏高 C.相等 D.无法判断
(2)我国化学家侯德榜,成功地改进了国外纯碱的生产工艺,发明了联合制碱法。用其生产线所生产的纯碱中往往含有少量杂质氯化钠。
①为检验产品Na2CO3中含有杂质氯化钠,可取少量试样溶于水后,再滴加 ;观察到的现象是 。
②若起始时取试样ag,U型管(装有碱石灰)的质量为bg,请你利用下列装置完成纯碱试样中Na2C03的质量分数的测定。
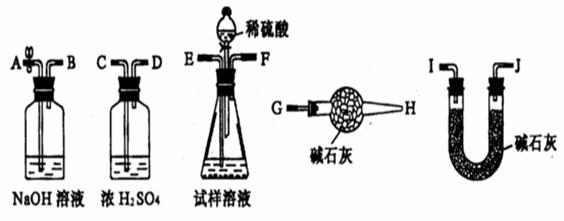
Ⅰ.实验时,各装置管口的连接顺序从左到右依次为A→B→E→F→C→D→1→J→G-→H,其中盛有浓硫酸的装置作用是 ,G→H的干燥管作用是 。
Ⅱ.反应前,先要从A处缓缓鼓人一定量的空气后再连接U型管等仪器,其目的是 ;反应后,若不从A处缓缓鼓人一定量的空气,将导致测试结果______(填“偏大”、“偏小”或“不变”)。
Ⅲ。若反应完全后,最终U型管的质量为:99,则试样中纯碱的质量分数的计算式为 。
25.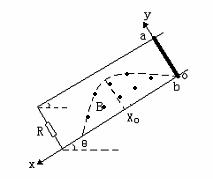 (20分)如图所示,两根不计电阻的倾斜平行导轨与水平面的夹角θ=37o ,底端接电阻R=1.5Ω。金属棒a b的质量为m=0.2kg。电阻r=0.5Ω,垂直搁在导轨上由静止开始下滑,金属棒a b与导轨间的动摩擦因数为μ=0.25,虚线为一曲线方程y=0.8sin(
(20分)如图所示,两根不计电阻的倾斜平行导轨与水平面的夹角θ=37o ,底端接电阻R=1.5Ω。金属棒a b的质量为m=0.2kg。电阻r=0.5Ω,垂直搁在导轨上由静止开始下滑,金属棒a b与导轨间的动摩擦因数为μ=0.25,虚线为一曲线方程y=0.8sin( x)m与x轴所围空间区域存在着匀强磁场,磁感应强度.B=0.5T,方向垂直于导轨平面向上(取g=10m/s2,sin37o=0.6,cos37o=0.8)。求:
x)m与x轴所围空间区域存在着匀强磁场,磁感应强度.B=0.5T,方向垂直于导轨平面向上(取g=10m/s2,sin37o=0.6,cos37o=0.8)。求:
(1).当金属棒a b下滑的速度为 m/s 时,电阻R上消耗的电功率是多少?
m/s 时,电阻R上消耗的电功率是多少?
(2)若金属棒a b从静止开始运动到Xo=6 m处,电路中消耗的电功率为0.8w,在这一过程中,安培力对金属棒a b做了多少功?
26(14分).已知A、C、D、E均为单质气体,G、H均为化合物气体,B、M均为金属单质,常温下W是无色无味的液体。请回答下列问题:

(1)写出下列物质的化学式:
A 、E 、Z 、Y ;
(2)若反应①转移24mole-时,生成还原产物的质量为 g;
(3)写出反应②的化学方程式: ;
(4)写出反应③的离子方程式: ;
(5)把I溶液加热、蒸发、蒸干,再加强热后,得到的固体产物中一定有_________ (填化学式);
(6)某金属与稀硝酸恰好完全反应生成NO,消耗金属和硝酸的物质的量之比为1∶3,则该金属可能是M和B中的 (填化学式)。
27(14分).已知A、B、C是第二周期的非金属元素,其原子序数依次增大,且它们之间可以形成AC和BC以及AC2和BC2分子,D元素是一种短周期元素,它与A、B、C可分别形成电子总数相等的三种分子.
请填空:
(1) 写出A、B、C、D对应的元素符号:A.______、B.______、C.______、D._____.
(2) 写出工业生产中BD3与氧气反应的化学方程式:__________________________.
(3) 你认为B、C、D元素形成的化合物之间能否_____________(填:“能”或“不能”)发生下面的反应BC+BD3→DBC2+D2C,得出上面结论的理由是__________________
Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g) 4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是_____________(用含a的代数式表示);
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是_____________(用含a的代数式表示);
Ⅱ.若维持温度不变,在一个与Ⅰ反应前的起始体积相同容积固定的密闭容器中发生Ⅰ中所述的化学反应,开始时仍向容器中充入AC和BC2各1mol,达平衡时生成AC2和 B2共bmol,将b与Ⅰ中的a进行比较,则a_____b(填“>”、“<”、“=”或“不能确定”
24.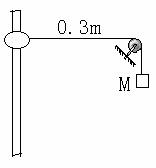 (19分)轻绳一端挂一质量为M的物体,另一端系在质量为m的圆环上,圆环套在竖直固定的细杆上,定滑轮与细杆相距0.3m,如图所示,将环由静止释放,圆环沿杆向下滑动的最大位移为0.4m。若不计一切摩擦阻力,求:
(19分)轻绳一端挂一质量为M的物体,另一端系在质量为m的圆环上,圆环套在竖直固定的细杆上,定滑轮与细杆相距0.3m,如图所示,将环由静止释放,圆环沿杆向下滑动的最大位移为0.4m。若不计一切摩擦阻力,求:
(1)物体与圆环的质量之比;
(2)圆环下落0.3m时的速度大小(g取10m/s2)
23.(16分)2005年10月12日上午9时,“神舟六号”在长征2号F运载火箭的推动下飞向太空,飞船先在距近地点200km、远地点350km的椭圆型轨道上运行5圈后变轨进入到距地面343km的圆形轨道上绕地球飞行。与10月17日凌晨,返回舱顺利着陆。
为使问题简化,现设地球的半径为R,地球表面的重力加速度为g,地球自转周期为T,飞船做圆轨道飞行时距地面高度为H,求:飞船进入圆轨道做匀速圆周运动时的周期为多少?其轨道半径与地球同步卫星轨道半径之比为多少?(用以上字母表示)
22.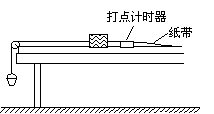 ⑴(6分)测量木块与长木板间的动摩擦因数的实验装置如图所示,长木板处于水平,装砂的小桶通过细线绕过定滑轮与木块连接,细线的长度大于桌面的高度,木块可以拖动纸带运动,打点计时器在纸带上打下一系列的点。
⑴(6分)测量木块与长木板间的动摩擦因数的实验装置如图所示,长木板处于水平,装砂的小桶通过细线绕过定滑轮与木块连接,细线的长度大于桌面的高度,木块可以拖动纸带运动,打点计时器在纸带上打下一系列的点。
实验时接通打点计时器的电源,放手后,装砂小桶带动木块一起运动,小桶与地面接触之后,木块还要在木板上继续运动一段距离后停下,打点计时器在纸带上打下一系列的点,如图所示。纸带的左端与木块相连,并用虚线框标出了A、B两个区域,为了求得木块与长木板间的动摩擦因数,应选取_____区域的数据计算出木块运动的加速度的大小(用a表示),由此计算动摩擦因数的公式是μ=__________。

(2)(11分)为了测定电流表A1的内阻,采用如图所示的电路。其中
 A1是待测电流表,量程为300μA,内组约为100Ω;
A1是待测电流表,量程为300μA,内组约为100Ω;
A2是标准电流表,量程是200μA;
R1是电阻箱,阻值范围0~999.9Ω;
R2是滑动变阻器;
R3是保护电阻;
E是电池组,电动势为4V,内阻不计;
S1是单刀单掷开关,S2是单刀双掷开关。
(1)根据电路图,请在下面实物图中画出连线,将器材连接成实验电路。

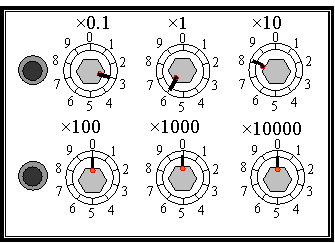
(2)连接好电路,将开关S2扳到接点a处,接通开关S1,调整滑动变阻器R2使电流表A2的读数是150μA;然后将开关S2板到接点b处,保持R2不变,调节电阻箱R1,使A2的读数仍为150μA。若此时电阻箱各旋钮的位置如图3所示,电阻箱R1的阻值是_______Ω,则待测电流表A1的内阻Rg= _______Ω。
(3)上述实验中,无论怎样调整滑动变阻器R2的滑动端位置,都要保证两块电流表的安全。在下面提出来供的四个电阻中,保护电阻R3应选用___________(填写阻值相应的字母)。
A.200kΩ B.30 kΩ C.20 kΩ D.15 kΩ
(4)下面提供最大阻值不同的四个滑动变阻器供选用。既要满足上述实验要求,又要调整方便,滑动变阻器________(填写阻值相应的字母)是最佳选择。
A.25kΩ B.10 kΩ C.5 kΩ D.1 kΩ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com