
题目列表(包括答案和解析)
5.绿色化学又称环境友好化学,它的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”。下列反应符合绿色化学这-特点的是
A.工业冶铁 
B.用生石灰制熟石灰 
C.实验室制二氧化碳 
D.工业上用硫酸除铁锈 
4. 通过下列实验操作,不能达到实验目的的是
通过下列实验操作,不能达到实验目的的是
3.下列实验操作中,正确的是
A.向试管内滴加液体时,将胶头滴管伸入试管内
B.用排水集气法收集二氧化碳
C.将盛有液体药品的烧杯直接放在酒精灯火焰上加热
D.读取量筒内液体药品的体积时,视线与凹液面的底部保持水平
2.在治理城市污染中所采取的措施错误的是
A.就地焚烧秸秆和落叶 B.种花植树美化环境
C.垃圾分类放置,实行垃圾资源化 D.提倡出行尽量以公交车代替私家车
1.我们生活在物质的世界里,而物质在不断地变化。以下变化属于物理变化的是
A.葡萄酿酒 B.冰雪融化
C.菜刀生锈 D.食物腐败
25.(11分)市场上有两种外观类似黄金的Cu-Zn合金和Cu-Ag合金制品,若实验室只提供一瓶稀硫酸和必要仪器。
(1) 你认为能测出 合金中铜的质量分数;
(2) 取上述(1)中的合金粉末20g放入烧杯中,加入50 g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为69.8 g。
求:①产生氢气的质量;
②求出该合金中铜的质量分数;
③稀硫酸中溶质的质量分数。


|
|
|
填涂卡号 |
|
|
|
姓名 |
|
|
|
班级 |
|
|
|
试室 |
金中南校2009-2010学年度第一学期第三次月考
24.(6分)锌是人体生长发育、维持器官正常功能的微量元素,人体缺锌会引起多种疾病,因此缺锌者可通过服用葡萄糖酸锌等保健品来补锌。已知葡萄糖锌的化学式为C12H22O14Zn。请回答:
(1)葡萄糖酸锌是由____种元素组成的,葡萄糖酸锌的相对分子质量是 ;
(2)葡萄糖酸锌中所含锌元素的质量分数为__________(结果保留至0.1%);
(3)现有一支20mL的葡萄糖酸锌口服液,其中含锌6.5mg,那么该口服液中葡萄糖酸锌的质量是_________ mg。
23.(13分)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应,NaOH溶液与稀盐酸发生反应的化学方程式是 。
(1)用pH试纸测定溶液的pH时,正确的操作是:
。
(2)简述强调“测得的pH小于7”的理由: 。
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了。该小组对这种意外现象的原因作了如下猜想:
①可能是酚酞溶液与空气中的氧气反应,使红色消失;
②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失。
(1) 氢氧化钠溶液与二氧化碳反应的化学方程式是 。
(2)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液。实验中“加热”和“滴入植物油”目的分别是 、
。实验结果表明酚酞溶液红色消失与空气中的氧气无关。
(3)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:
结论1:说明Na2CO3溶液呈 性;
结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关。
(4)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象。请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法 ,②观察到的现象 。
22.(14分)化学实验是学习化学的基础,请根据下列装置图回答问题。
 A
B
C
A
B
C
(1)写出仪器a、b的名称_____ __;b_____ __。
(2)写出A图中产生气体的化学方程式____________________________。
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有______ _、______ _和_____ __的性质。这一性质在实际生活中的应用为_____ __。
(4)C图中螺旋状铁丝的末端系一根火柴的作用是___ ___。
(5)小明按C图实验时,集气瓶内发生反应的化学方程式是 ,集气瓶炸裂了,其可能的原因是______ _。
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。请你分析回答:
|
物质 |
镁条 |
含碳0.05%的铁丝 |
含碳0.2%的铁丝 |
含碳0.6%的铁丝 |
|
燃烧时 的现象 |
剧烈燃烧,发出 耀眼白光,无火星 |
剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
(未填) |
①你认为表中未填的实验现象是__________________________。
②根据上表中有关数据及燃烧时的现象,分析造成铁丝在氧气中燃烧时火星四射的主要原因是_____________ ___。
21.(10分)下图是小明配制100g溶质质量分数12%的氯化钠溶液的有关实验操作示意图。
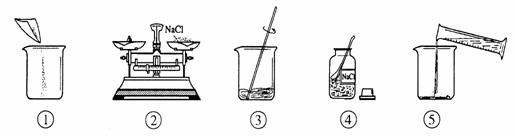
(1) 配制过程中使用的四种玻璃仪器,分别是广口瓶、________、_________、量筒。
(2) 请你指出图中一处错误操作,并分析该操作可能造成的后果。____________________________,________________________。
(3) 图②、图③表示的操作步骤分别是______ __、______ __。
(4) 配制时需称量氯化钠_______g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会__________(填“偏大”或“偏小”);量取水最好选择____________的量筒(填序号①10mL ②50mL ③100mL)。(水的密度为1g/cm3)
(5)在量取蒸馏水体积时,若仰视读数,则会导致氯化钠溶液的溶质质量分数 (填“<”或“>”)12%。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com