
题目列表(包括答案和解析)
5.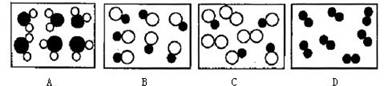 下图是表示气体粒子的示意图,其中“●”和“○”分别表示两种不同元素的原子,那么其中表示混合物的是
下图是表示气体粒子的示意图,其中“●”和“○”分别表示两种不同元素的原子,那么其中表示混合物的是
4.已知一个碳12原子的质量为M㎏,铝的相对原子质量为N,则一个铝原子的质量为
A.12M/N㎏ B.12N/M㎏ C.MN/12㎏ D.12MN㎏
3.下列对有关实验现象的描述正确的是
A.铁丝在空气中燃烧时,火星四射,有黑色物质生成
B.红热木炭放入盛有氧气的集气瓶中,剧烈燃烧,产生白光
C.石蜡在氧气中燃烧时,有水和二氧化碳生成
D.红磷在氧气中燃烧产生白色烟雾
2.下表是市场上销售的一种加碘食盐包装袋上的文字说明,下列说法中错误的是




 配料表 精制海盐、碘酸钾(KIO3) A.碘酸钾是化合物
配料表 精制海盐、碘酸钾(KIO3) A.碘酸钾是化合物
 含碘量 35±15mg/kg
B.碘酸钾不稳定、受热易分解
含碘量 35±15mg/kg
B.碘酸钾不稳定、受热易分解

 储藏方法 通风、防潮
C.碘酸钾是一种氧化物
储藏方法 通风、防潮
C.碘酸钾是一种氧化物

 食用方法 待食物熟后加入碘盐
D.在KIO3中,碘元素化合价为+5价
食用方法 待食物熟后加入碘盐
D.在KIO3中,碘元素化合价为+5价
1.下列变化属于化学变化的是
A.工业上分离液态空气制氧气 B.石油经炼制得到汽油等产品
C.木炭使红墨水褪色 D.用石墨制取人造金刚石
32.(共10分)同学们学习了《金属与矿物》一章后,对金属的有关性质产生了浓厚的兴趣。
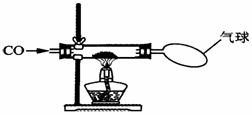 探究一:某小组做了如下图所示的探究实验。实验发现CO与CuO加热后黑色粉末变成红色粉末。请你参与该小组的研究过程并完成相关任务:
探究一:某小组做了如下图所示的探究实验。实验发现CO与CuO加热后黑色粉末变成红色粉末。请你参与该小组的研究过程并完成相关任务:
[研究课题]探究红色粉末的主要成分
[查阅资料]
(1) 有关物质的颜色:
CuO粉末:黑色,Cu2O粉末:红色
(2)CuO和Cu2O都能和稀硫酸发生反应,
化学方程式为:
CuO十H2SO4 = CuSO4+H2O Cu2O+H2SO4 = CuSO4+Cu+H2O
[猜想与实验]
(1)如果硬质玻璃管内红色粉末为一种物质,请猜想它的成分,并设计简单的实验证明你的猜测。
|
猜想 |
简单实验方案 |
现象 |
CO和CuO反应的化学方程式 |
|
粉末为Cu |
|
不反应 |
CuO+CO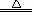 Cu+CO2 Cu+CO2 |
|
|
粉末溶解,溶液变成蓝色,生成红色粉末 |
2CuO+CO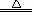 Cu2O+CO2 Cu2O+CO2 |
(2)如果硬质玻璃管内红色粉末为两种物质的混合物,要确定粉末中两种物质的质量分数,还需要通过有关数据计算进行判断。下列数据为计算依据的是 ( )
A.反应前CuO粉末的质量 B.硬质玻璃管中固体物质减少的质量
C.通入CO的质量 D.反应后固体混合物的总质量
探究二:实验室通常利用反应“Zn+H2SO4= ZnSO4+H2↑”可以制氢气。
(1)探究小组发现实验室制氢气常用粗锌(含杂质的锌)而不用纯锌,原因是粗锌跟硫酸反应放出氢气的速率比纯锌快。现将等质量的两份纯锌粉分别加入a,b两个烧杯中,两烧杯中均各盛有相同的过量稀硫酸,同时向a烧杯中加入少量的CuO粉末,充分反应后两烧杯中:
①产生氢气的质量:a b(填“<,>,或=”)
②产生氢气的速率:a b(填“<,>,或=”)
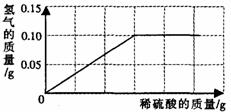 (2)为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如右图所示。试计算:
(2)为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如右图所示。试计算:
①样品中铜的质量分数为: 。
②恰好完全反应时所消耗稀硫酸的质量
为 克。(写出具体计算过程)
2009-2010学年第一学期期末质量检测
31.(7分)某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定。
信息:碱石灰是NaOH和CaO的固体混合物,既能吸收水,也能吸收CO2。
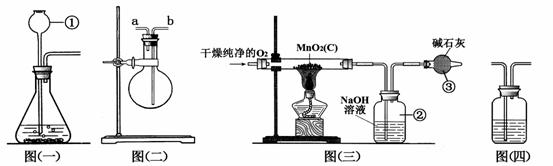
(1)仪器①的名称是 。如果该实验选择图(一)装置来制取氧气,则所反应的化学方程式为 。其中二氧化锰的起到 作用。
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入。
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是____________________________________________________。
(4)为确认图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为__________(填字母)。
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(5)称取5.0 g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1 g,则样品中二氧化锰的质量分数为_______________________(填计算结果)。
30.(3分)人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)现代社会使用大量的钢铁,钢铁与 接触容易生锈造成损失,在钢铁表面采用 方法可以防止钢铁生锈。
(2)波尔多液是由硫酸铜和熟石灰加水配制而成,不能用铁制容器配制的原因是(用化学方程式表示) 。
29.(8分)为改善城市环境,提升生活质量,我市陆续使用天然气,乙醇汽油等清洁能源。
(1)镇江市区家用燃料的更新历程如下:

①下列有关家用燃料更新的理由,正确的是 。
A.天然气是可再生的能源 B.气体燃料的利用率更高
C.减少煤燃烧过程中产生的污染物
②天然气(主要成分是甲烷)和液化石油气(主要成分是丙烷和丁烷)中碳元素的质量分数分别约为75%和82.3%,通过该数据分析:相同条件下,用天然气作燃料比液化石油气更环保的理由 。
③甲烷在空气中完全燃烧的化学方程式为 。
(2)从新疆输送到镇江气门站的天然气需经过除杂、添加无毒臭味剂、减压等处理后才能输送到市民家中。用分子的观点解释天然气减压后体积会膨胀的原因 。在其中添加无毒臭味剂可以起到的作用 。
(3)为进一步提升空气质量,我市将逐步推广乙醇汽油的使用。所谓乙醇汽油是在汽油中加入适量乙醇混合而成的一种燃料。
①乙醇汽油属于_________(选填:“纯净物”或“混合物”)。
②从环境保护的角度看,下列燃料中最理想的是___________ (填写字母编号)。
A.氢气 B.煤 C.乙醇汽油 D.煤气(主要含CO)
(4)为测定原煤中的含碳量需要用纯氧气。但小亮同学在实验室制氧气的过程中发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃。那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装人其总容积10%、20%、30%、40%、50%的水。用排水法收集氧气,恰好把5只集气瓶中的水排去。将带火星的木条依次插入①~⑤号瓶中,记录实验现象。
小亮在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见下表。
|
|
第一组 |
第二组 |
第三组 |
||||||||
|
集气瓶编号 |
① |
② |
③ |
④ |
⑤ |
① |
② |
③ |
④ |
⑤ |
① |
|
瓶中O2占容积的体积分数(%) |
l0 |
20 |
30 |
40 |
50 |
3l |
33 |
35 |
37 |
39 |
34 |
|
带火星木条的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
很亮 |
很亮 |
复燃 |
复燃 |
复燃 |
很亮 |
请根据实验回答下列问题:
①使用带火星的木条验满氧气的方法是否可靠: (填“是”或“否’')。
②收集的氧气占容积的体积分数最低为 %时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数分数是 %(计算结果保留整数)。
(5)鉴于用收集好氧气再进行实验,存在上述不确定因素,因此小亮和同学们决定采用下列装置进行测定(如图):
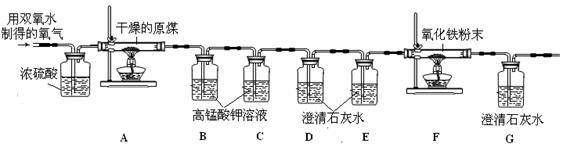
资料:①干燥原煤燃烧产生的气体主要CO2,但同时含有少量SO2和CO。
②SO2能使紫红色高锰酸钾(KMnO4)溶液褪色,也能使澄清石灰水变浑浊;而CO2和CO均不能使紫红色高锰酸钾溶液褪色。
请根据装置图回答
①浓硫酸的作用是 ;
②试写出B装置和C装置(或D装置和E装置)的作用(任选一组,2组兼答不给分):
B装置(或D装置)的作用 ;
C装置(或E装置)的作用 ;
③若将B、C装置和D、E装置对调,测得原煤中碳元素的质量分数 (填“偏大”或“偏小”)
④尾气应如何处理? 。
(6)过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小。为确保实验时,双氧水的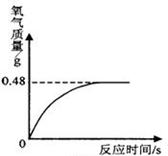 用量。小亮和同学们事先对实验室提供的过氧化氢溶液,进行
用量。小亮和同学们事先对实验室提供的过氧化氢溶液,进行
了溶质质量分数测定。他们取出该溶液51g,加入适量二氧化
锰,生成氧气的质量与反应时间的关系如图所示。
①完全反应后生成氧气的质量为 。
②计算该过氧化氢溶液中溶质的质量分数(写出计算过程)。
28.(6分
 )已知 A、C、D、Y都是氧化物,其中A为黑色固体,D 为红棕色固体,C、Y为无色气体;B、E、G是单质,其中B、E为常见金属, G为气体;反应②是高炉炼铁中的反应原理,X溶液呈蓝色。下图是它们之间的相互转化关系.请回答:
)已知 A、C、D、Y都是氧化物,其中A为黑色固体,D 为红棕色固体,C、Y为无色气体;B、E、G是单质,其中B、E为常见金属, G为气体;反应②是高炉炼铁中的反应原理,X溶液呈蓝色。下图是它们之间的相互转化关系.请回答:
|
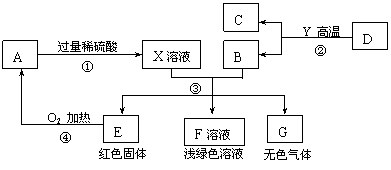
(1)X溶液中所含有的溶质为 ,固体A的化学式为________,F溶液显浅绿色,其中所含有的溶质是________________。
(2)写出反应②的化学方程式 ,
(3)写出反应③中生成无色气体的化学方程式 ,
(4)指出物质G和A在加热条件下发生的化学反应的基本反应类型 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com