
题目列表(包括答案和解析)
28.(3分)根据下图所示水、二氧化碳和氧气的性质实验,请回答以下问题。
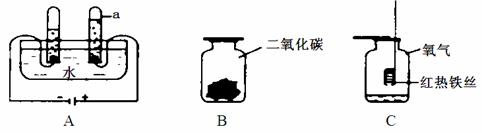
(1)A中负极产生的气体是_______(填化学式).
(2)将白色纸花用紫色石蕊试液喷湿,放入集气瓶B中,观察到的现象是___________.
(3)集气瓶C中的铁丝在氧气中燃烧实验时,集气瓶底部放一些水或细沙的作用是 .
27.(3分)实验室科学研究的重要手段,正确操作是实验获得成功的重要保证。请填空:
(1)给试管内的液体加热时,液体量不可超过试管容积的__________;
(2)实验中氯化钠固体取多了_________(填“能”或“不能”)放回原瓶;
(3)点燃可燃性气体前必须先 .
26.(4分)A-G都是初中化学中常见的物质,已知:B为黑色固体;C是常用于灭火的气体;A与C是组成元素相同的两种氧化物;D为红色固体单质;E为黑色固体单质;F为一种比较活泼的常见金属;G是一种蓝色溶液。它们的转化关系如图所示:
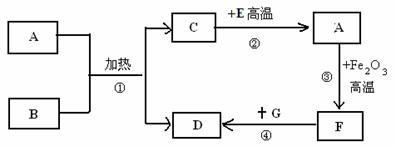
试推断:
⑴物质B的化学式 ;
⑵反应③的化学方程式 ;
⑶反应④的化学方程式 ,反应类型:_______反应。
25.(5分)人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
 (1)下列铁制品的用途中,利用金属导热性的是______________(填字母)。
(1)下列铁制品的用途中,利用金属导热性的是______________(填字母)。
(2)某地区部分居民更换了旧自来水铁质管道,基本解决了管内生锈、饮用水含铁量超标的问题。下列与铁质管道生锈有关的物质是________(填代号)。
①水 ②氧气 ③氮气
(3)防止铁制品生锈的一种方法是________________________________________。
(4)铝制品在空气中有较强的抗腐蚀性,原因是____________________________________。
(5)氮化铝(AlN)因耐高温、抗冲击、导热性好,被广泛用于大规模集成电路生产、陶瓷工业等,工业上是用氧化铝、氮气、单质碳在一定条件下反应生成AlN和另一种可燃性气体氧化物,该反应的化学方程式为: .
24.(5分)水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的运用。
下图为自来水厂净水过程示意图:

(1)上图所加絮凝剂若为明矾,其作用是________________________,吸附池内的活性炭起 ___________作用。
(2)鱼类可在河水中生存,是因为河水中溶有________①氧分子②氧元素(填序号)。
(3)现要测定某段河水的pH:在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量该河水沾在pH
试纸上,把试纸显示的颜色与标准比色卡比较,pH大于7,则说明该水样显________性;
(4)2009年“中国水周”活动的宣传主题为“落实科学发展观,节约保护水资源”。下列生活习惯应该摒弃的是(填序号)_____________。
①用盆接水洗菜 ②用养鱼水浇花草
③使用节水龙头 ④大量使用含磷洗衣粉洗衣服
23.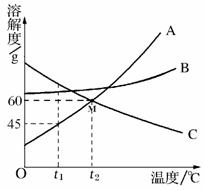 (4分)右图是 A、B、C三种物质的溶解度曲线。请回答:
(4分)右图是 A、B、C三种物质的溶解度曲线。请回答:
⑴t1℃时,A、B、C三种物质的溶解度由大到小的顺序
是 ;
⑵A、C在________℃时溶解度相等;
(3)现有t2℃时160克A的饱和溶液,将其降温到t1℃时,
可析出_________克A晶体;
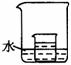 ⑷如右图所示,小烧杯中盛放的是底部有少量固体C的饱和
⑷如右图所示,小烧杯中盛放的是底部有少量固体C的饱和
溶液。 若将少量的下列物质分别小心地加入到大烧杯的
水中,不断搅拌,能使小烧杯C溶液的溶质质量分数增大
的是_______(填字母)。
A.氢氧化钠 B.硝酸铵 C.氧化钙 D.氯化钠
22. (4分)图A是元素周期表的一部分
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
第二 周期 |
3 Li 锂 7 |
4 Be 铍 9 |
5 B 硼 11 |
① |
7 N 氮 14 |
8 O 氧 16 |
9 F 氟 19 |
10 Ne 氖 20 |
|
第三 周期 |
11 Na 钠 23 |
② |
13 Al 铝 27 |
14 Si 硅 28 |
③ |
16 S 硫 32 |
17 Cl 氯 35.5 |
18 Ar 氩 40 |
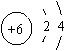

图B 图C
(1)原子序数为8的元素名称为 ;
(2)图B是某元素的原子结构示意图,该原子最外层电子数为___________,该元素在图A中的位置是(填①或②或③) ;
(3)图C是氯元素的原子结构示意图,氯原子在化学反应中易(填“得”或“失”) 电子。
21.(6分)
⑴用适当的符号和数字填空:
①3个氮原子__________;②3个氢分子________;③2个铁离子_________ ;
⑵现有下列三种物质A 氮气 B生石灰 C二氧化碳,试用相关物质的序号填空:
①常用作袋装食品干燥剂的是 ②固态时可用于人工降雨的物质是
③可用于制取氮肥的是___________。
20.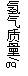
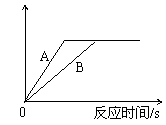 某研究性学习小组的同学为探究实验室制取氢气的方案,分别用等质量的金属A、B跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如下图所示。分析图象得到的下列结论中,正确的是(已知A、B在生成物中均显+2价,A、B的相对原子质量不等)
某研究性学习小组的同学为探究实验室制取氢气的方案,分别用等质量的金属A、B跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如下图所示。分析图象得到的下列结论中,正确的是(已知A、B在生成物中均显+2价,A、B的相对原子质量不等)
A.反应速率A>B
B.金属的活动性A<B
C.可能是A、B两种金属都有剩余,硫酸完全反应
D.可能是A、B两种金属均反应完,硫酸有剩余
19.现有含杂质的铁5.6克,与足量的稀硫酸充分反应后,生成0.19克氢气,则含有的杂质可能是
A.锌 B.镁 C.铝 D.铜
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com