
题目列表(包括答案和解析)
31.[答案]实验步骤:
①取2支试管,分别标记为A、B。(3分)
②分别量取0.3mol/L的葡萄糖溶液、0.3mol/L的甘油溶液各10mL,注入A、B二支试管。(3分)
③分别量取1 mL稀释的羊红细胞悬液注入A、B二支试管中,同时开始记时,记录溶液由不透明到澄清的时间。(3分)
结果及结论:
如果加入葡萄糖液的试管内溶液澄清所用的时间短,说明葡萄糖比甘油进入细胞的速度快;(3分)
如果加入甘油的试管内溶液澄清所用的时间短,说明甘油比葡萄糖进入细胞的速度快;(3分)
如果两支试管内溶液澄清所用的时间相同,说明葡萄糖和甘油进入细胞的速度相同。(3分)
实验思考:
由于葡萄糖和甘油都是细胞选择吸收的物质,所以会逐渐进入细胞,使细胞内的溶液浓度增大,渗透压上升,细胞大量吸水,最终导致细胞胀破。(4分)
[解析]本题属于对实验能力的考查,考查了考生设计简单的对照实验进行科学探究的能力及其对探究结果进行预测和分析的能力。同时此题还考查了细胞膜的功能。
设计简单的对照实验,要遵循单一变量原则,实验中除了葡萄糖和甘油两种溶液的区别外,所加入的量、时间及其浓度都要保持一致,避免无关变量对实验结果造成的误差。对于葡萄糖溶液和甘油溶液谁进入细胞的速度更快是未知的,所以其结果就可能有三种可能性:两者进入细胞内的速度一样快;葡萄糖比甘油进入细胞的速度快;甘油比葡萄糖进入细胞的速度快。葡萄糖和甘油都是生命活动需要的物质,即使是红细胞的等渗溶液,也都会被细胞膜运输吸收进入细胞内,从而是细胞的渗透压增大而吸收水分,最终使红细胞破裂。
30.[答案]:①选择具有抗噬菌体突变的大肠杆菌(2分) 便于识别(鉴别)大肠杆菌的菌落(2分)②异养型(2分) (注:此空如果答“异养需氧型”不能得分) 乳糖 、蛋白胨(2分) 蛋白胨(1分)③寄生(2分) ④支持假设一(2分) A、B两组所有的培养皿中菌落数没有显著差异(2分)
⑤抗噬菌体变异发生时刻的差异(2分) 由于A试管大肠杆菌进行了分装培养,使A组实验中的大肠杆菌营养较为充足,繁殖的代数和DNA复制的次数比B组大肠杆菌多,造成A组实验中大肠杆菌的基因突变机会高于B组,而且这种突变的时间发生在大肠杆菌接触噬菌体之前(3分)。
[解析]本题综合地考查了噬菌体对大肠杆菌的筛选,大肠杆菌的代谢类型和鉴别方法,并考查了有关的实验现象进行综合分析的能力。
①噬菌体能寄生并破坏大肠杆菌,使大肠杆菌菌落消失,因此噬菌体可用于选择不具有抗噬菌体突变的大肠杆菌。伊红一美蓝一般用于便于识别(鉴别)大肠杆菌的菌落。②由于大肠杆菌不能制造有机物,因此同化作用类型是异养型,并可利用乳糖和蛋白胨作为碳源和氮源。③噬菌体只能利用大肠杆菌细胞内的各种成分进行代谢和繁殖,因此它与大肠杆菌之间的关系是寄生。④对图解的分析,不难判断该实验支持假设一,因为如果大肠杆菌的抗噬菌体突变发生在大肠杆菌与噬菌体接触之后,应出现A、B两组所有的培养皿中菌落数没有显著差异,与图中事实不符。⑤根据菌落的多少,可判断抗噬菌体变异发生在何时,从而推断有关的假设是否正确。由于A试管大肠杆菌进行了分装培养,使A组实验中的大肠杆菌营养较为充足,繁殖的代数和DNA复制的次数比B组大肠杆菌多,造成A组实验中大肠杆菌的基因突变机会高于B组,而且这种突变的时间发生在大肠杆菌接触噬菌体之前 。
29.[答案] (1)2 (1分) 3 (1分) 1 (1分)
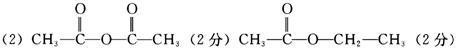
(3)6 (4分)
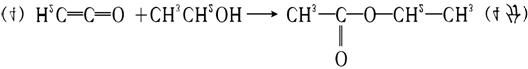
[分析预测及备考建议]本题主要考查了有机化学的反应类型和官能团的性质。
[答题技巧]由题目所给信息及CH3-COOH 的性质可知,A为乙烯酮,反应为:
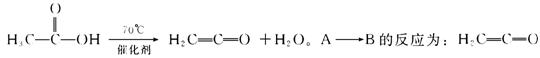
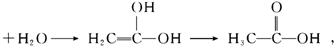 即B乙酸。其他反应分别为:
即B乙酸。其他反应分别为:
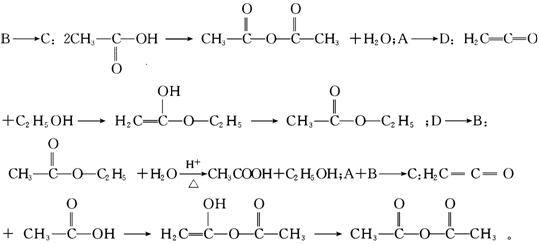
由以上分析可知,取代反应有两个,加成反应有3个,消去反应为1个。由题意可知,所要求的C的同分异构体除一个-OH和四元环外,还有一个碳原子可以甲基或亚甲基形式存在,其结构分别为:
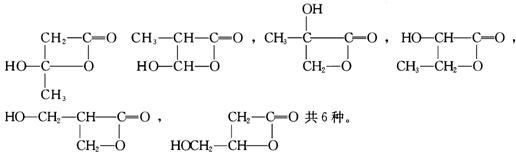
28.[答案](1)CD(2分)
(2)0.06(或6%)(2分) 1.45(2分)
(3)c(NH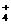 )>c(SO
)>c(SO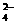 )>c(H+)>c(OH-)(2分)
)>c(H+)>c(OH-)(2分)
[分析预测及备考建议]本题主要考查了硫酸工业和化学平衡的计算,属于综合性较强的题目。因此我们在平时的学习中要注意前后联系和融会贯通。
 [答题技巧] (1)将矿石粉碎和使用催化剂都只与化学反应速率有关,而与化学平衡无关;在接触室中发生的反应是一个气体总体积缩小的放热反应2SO2+O2 2SO3;ΔH<0。从平衡移动的角度来看,应采用较低温度和较高的压强,即C是根据平衡移动选择的条件,增加O2的用量可使上述平衡向正反应方向移动,提高SO2的转化率,符合化学平衡移动原理;用浓H2SO4吸收SO3与吸收速率有关,与化学平衡移动无关,答案为C、D。(2)若保持温度和压强不变,充入1 mol SO3与所给的平衡等效,平衡时SO2的体积分数为
[答题技巧] (1)将矿石粉碎和使用催化剂都只与化学反应速率有关,而与化学平衡无关;在接触室中发生的反应是一个气体总体积缩小的放热反应2SO2+O2 2SO3;ΔH<0。从平衡移动的角度来看,应采用较低温度和较高的压强,即C是根据平衡移动选择的条件,增加O2的用量可使上述平衡向正反应方向移动,提高SO2的转化率,符合化学平衡移动原理;用浓H2SO4吸收SO3与吸收速率有关,与化学平衡移动无关,答案为C、D。(2)若保持温度和压强不变,充入1 mol SO3与所给的平衡等效,平衡时SO2的体积分数为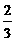 (1-0.91)=0.06。若保持温度和体积不变,充入a mol SO2和b mol O2,a∶b=2∶1,平衡时SO3体积分数仍为0.91,则达平衡时每种物质的物质的量与所给平衡相等,设O2的转化量为x,则:
(1-0.91)=0.06。若保持温度和体积不变,充入a mol SO2和b mol O2,a∶b=2∶1,平衡时SO3体积分数仍为0.91,则达平衡时每种物质的物质的量与所给平衡相等,设O2的转化量为x,则:
2SO2 + O2 2SO3
2SO3
开始: a mol b mol
转化: 2x x 2x
平衡:a mol-2x b mol-x 2x
根据题意得: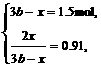
解得:x =0.6825 mol,b=0.7275 mol,
所以a=1.455 mol。
 (3)由(NH4)2SO4的组成可知c(NH
(3)由(NH4)2SO4的组成可知c(NH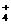 )>c(SO
)>c(SO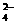 );
);
由NH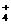 +H2O NH3·H2O+H+ 可知c(H+)>c(OH-),
+H2O NH3·H2O+H+ 可知c(H+)>c(OH-),
所以有c(NH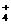 )>c(SO
)>c(SO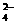 )>c(H+)>c(OH-)。
)>c(H+)>c(OH-)。
27.[答案](1)硫 (1分)
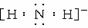 (2)
(2) +H2O
+H2O NH3·H2O+H+ (2分)
NH3·H2O+H+ (2分)
(3) (2分)
(4)①O2 0.8(m-n) 0.2m+0.8n
②NO 0.8m+0.6n 0.2m-0.6n (每空2分,共12分)
[分析预测及备考建议]本题主要考查了元素及其化合物的知识和用理论知识解释化学问题的能力,同时考查思维的严密性和分析能力。
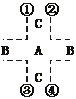 [答题技巧](1)根据题意可知,A、B、C三元素的位置关系有四种可能,如图:
[答题技巧](1)根据题意可知,A、B、C三元素的位置关系有四种可能,如图:
经计算可知,只有当A为氧元素,C为硫元素,B为氮元素时符合题意,又A、B、C、D为短周期元素,D与A、B、C不同周期,也不同主族,所以D只能为氢元素。(2)H4N2O3的离子化合物为NH4NO3,其中 水解呈酸性:
水解呈酸性: +H2O
+H2O NH3·H2O+H+。(3)由于NH3(液态)的电离方式与H2O相似,所以有NH3+NH3
NH3·H2O+H+。(3)由于NH3(液态)的电离方式与H2O相似,所以有NH3+NH3
 +NH
+NH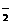 。(4)设NO2的气体体积为x,O2的体积为y,则有x+y=m mL①,若余下的气体为O2,则参加反应的O2为(y-n),根据4NO2+O2+2H2O====4HNO3…A可知,4(y-n)=x②,解①②得:x=0.8(m-n),y=0.2m+0.8n若余下的气体为NO,由3NO2+H2O====2HNO3+NO知经上述反应A余下NO2的体积为3n mL,根据4NO2+O2+2H2O====4HNO3知:4y=(x-3n)③,解①③得:x=0.8m+0.6n,y=0.2m-0.6n。
。(4)设NO2的气体体积为x,O2的体积为y,则有x+y=m mL①,若余下的气体为O2,则参加反应的O2为(y-n),根据4NO2+O2+2H2O====4HNO3…A可知,4(y-n)=x②,解①②得:x=0.8(m-n),y=0.2m+0.8n若余下的气体为NO,由3NO2+H2O====2HNO3+NO知经上述反应A余下NO2的体积为3n mL,根据4NO2+O2+2H2O====4HNO3知:4y=(x-3n)③,解①③得:x=0.8m+0.6n,y=0.2m-0.6n。
26.[答案](1)Ba(NO3)2 (1分) HCl (1分) HNO3(1分) Br2(1分) AgNO3(1分)
(2)SO (1分) SO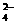 (1分) Cl-(1分)
(1分) Cl-(1分)
(3)BaSO3+2H+====Ba2++SO2↑+H2O(2分)
(4)中和OH-,防止对Cl-的检验产生干扰(2分)
(5)会使SO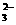 对SO
对SO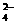 的检验产生干扰,不能确认SO
的检验产生干扰,不能确认SO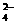 是否存在(2分)
是否存在(2分)
(6)SO2+Br2+2H2O====4H++SO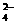 +2Br-(2分)
+2Br-(2分)
[分析预测及备考建议]本题主要考查了阴阳离子的鉴别和离子方程式的书写。
[答题技巧]由所给试剂的性质特点及反应“气体B+试剂④ →溶液褪色”,可知试剂④为溴水,气体B为SO2。又“白色沉淀A+过量试剂② →SO2↑+沉淀B”,则试剂②为盐酸(若为HNO3,则会生成SO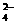 而不能放出气体SO2),且白色沉淀A中含SO
而不能放出气体SO2),且白色沉淀A中含SO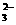 离子。又“原无色溶液+过量试剂① →白色沉淀A+无色溶液A”,则试剂①为Ba(NO3)2(因AgNO3与OH-作用生成棕黑色Ag2O沉淀),白色沉淀A为BaSO4与BaSO3的混合物,白色沉淀B为BaSO4,试剂③可能为HNO3(联想SO
离子。又“原无色溶液+过量试剂① →白色沉淀A+无色溶液A”,则试剂①为Ba(NO3)2(因AgNO3与OH-作用生成棕黑色Ag2O沉淀),白色沉淀A为BaSO4与BaSO3的混合物,白色沉淀B为BaSO4,试剂③可能为HNO3(联想SO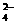 的检验方法)。无色溶液A中含Cl-、OH-,经HNO3酸化除去OH-后,所得溶液B中含Cl-,而“溶液B+试剂⑤→白色沉淀C”,所以试剂⑤为AgNO3,试剂③必为HNO3,C沉淀为AgCl。至此所给试剂和离子全部确定,其他问题便可迎刃而解。
的检验方法)。无色溶液A中含Cl-、OH-,经HNO3酸化除去OH-后,所得溶液B中含Cl-,而“溶液B+试剂⑤→白色沉淀C”,所以试剂⑤为AgNO3,试剂③必为HNO3,C沉淀为AgCl。至此所给试剂和离子全部确定,其他问题便可迎刃而解。
25.[解](1)对卡西尼-惠更斯号飞船由牛顿第二定律和万有引力定律
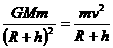 ① (2分)
① (2分)
在土星表面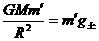 ② (2分)
② (2分)
g土=1.07 g地=10.7m/s2
解得v=2.22×104m/s (2分)
(2)设卡西尼号飞船质量为m
由动量守恒得惠更斯号是向后方分离发射的,则 m v=
m v=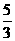 m v-
m v-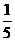 m v1 ③ (4分)
m v1 ③ (4分)
v1=5.18×104m/s (2分)
(3)对卡西尼号由近点到远点机械能守恒
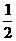 mv12-
mv12-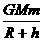 =mv22-
=mv22- 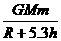 ④ (4分)
④ (4分)
得v2=4.68×104m/s (2分)
[分析预测及备考建议]动量、能量综合应用问题是主干知识点,结合天体运动这方面也较容易出综合题,因此它是高考出题的热点问题。
[答题技巧]动量守恒、能量守恒、动能定理是这类问题的理论依据,解题中关键是正确分析相互作用过程,建立正确的模型,结合动力学的知识顺利解题。
24.[答案](1)T=0.4π s ;l=0.4 m(2)m=0.05㎏(3)vmax=0.283 m/s
[分析预测及备考建议]本题考查单摆振动过程中摆线上的拉力变化情况,单摆的振动周期公式,向心力公式,受力分析,机械能守恒定律。本题是考查能力的一道新题型。
[答题技巧](1)由图可知 T=0.4π s,由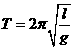 得:
得: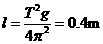 。(4分)
。(4分)
(2)在B点拉力的最大值为Fmax=0.510
N,Fmax-mg=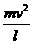 ;在A、C两点Fmin=0.495
N ,Fmin=mgcosθ.由A到B机械能守恒,即
;在A、C两点Fmin=0.495
N ,Fmin=mgcosθ.由A到B机械能守恒,即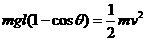 ,解得m=0.05㎏. (6分)
,解得m=0.05㎏. (6分)
(3)vmax=0.283m/s(4分)
23.[解]设运动中受总阻力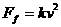 ,炮弹与金属架在磁场和阻力合力作用下加速(2分)
,炮弹与金属架在磁场和阻力合力作用下加速(2分)
根据牛顿第二定律,获得v1速度时,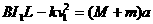 ①(4分)
①(4分)
当炮弹速度最大时,有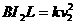 ②(3分)
②(3分)
解得垂直轨道的磁感强度为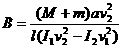 .
(3分)
.
(3分)
[分析预测及备考建议]电磁感应问题几乎是每年都有,主要考查感应电动势问题、受力分析、能量转化等问题,对这种高考热点要真正掌握好。
[答题技巧]抓住力是改变物体运动状态的原因,通过分析受力,结合运动过程,知道加速度和速度的关系,这是这种题的分析思路。结合动量定理、能量守恒就能解决本题。
22.[答案](1)1.33 (2分);负x轴上(3分)
[分析预测及备考建议]光学实验近几年很少出现,属于备考热点,同学们要掌握试验原理。
[答题技巧]根据光的折射定律,得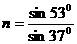 =1.33;玻璃砖绕O点逆时针转过26.50,法线相应的转过26.50,入射光线不动,则入射角变为63.50。因为sinC=
=1.33;玻璃砖绕O点逆时针转过26.50,法线相应的转过26.50,入射光线不动,则入射角变为63.50。因为sinC=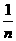 =0.75,而sin63.50>sin600=0.865,说明sin63.50大于临界角C,则发生全反射现象,只能在反射线上插针才能挡住A的象,根据光的反射定律可以知此时反射线正好在负x轴上。
=0.75,而sin63.50>sin600=0.865,说明sin63.50大于临界角C,则发生全反射现象,只能在反射线上插针才能挡住A的象,根据光的反射定律可以知此时反射线正好在负x轴上。
[答案](1) 380 (4分)(2) 最左端(分压为零的一端);向左端闭合;滑动头不动;电阻箱;R (5分)
[分析预测及备考建议]设计性实验是很好的实验题,学生比较难掌握,近几年在高考中这类题目也出现过,是一种热门试题。
[答题技巧]R1分担的最大电压U1=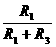 E,流过电表的最大电流为
E,流过电表的最大电流为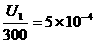 A,即
A,即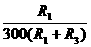 E=5×10-4,可得R3=380Ω。
E=5×10-4,可得R3=380Ω。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com