
题目列表(包括答案和解析)
8.氧气的收集方法有:①____________法;②____________法
思路解析:根据氧气的性质,可以用排水法收集氧气,也可以用向上排空气法收集氧气。
答案:①排水 ②向上排空气
7.以美国为首的北约军队使用一种“油气炸弹”,这种炸弹炸时首先释放出大量可燃性气体,然后可将可燃性气体引燃,这时躺在防护工事里的人即使未被炸死,也会因窒息而死亡,其原因是____________________________________________________________。
思路解析:汽油炸弹在爆炸后大量燃烧消耗空气中的氧气,使得防御工事中的士兵窒息死亡。
答案:汽油炸弹在爆炸后大量燃烧消耗空气中的氧气,使得防御工事中的士兵窒息死亡
6.在实验室制取某种气体时,该气体既能用排水集气法收集,又能用向上排空气法收集。由此可肯定该气体的物理性质中有:
(1)________________________,(2)________________________。
思路解析:排水法收集气体,要求气体在水中的溶解度很小,或者是难溶于水;能用向上排气法收集,要求该气体密度比空气的大。
答案:(1)难溶于水 (2)比空气重
5.实验室除了用加热高锰酸钾的办法制氧气外,还常用以下两种方法制取氧气。
(1)氯酸钾在二氧化锰催化剂和加热的条件下制取氧气。


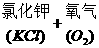
(注:催化剂能改变反应的速率,这里是加快反应速率)
(2)用双氧水在二氧化锰作催化剂的条件下制取氧气。

(注:双氧水是过氧化氢的水溶液,这里用稀溶液)
(3)研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
|
催化剂 温度/℃ 反应程度 |
Fe2O3 |
Al2O3 |
CuO |
MgO |
|
开始反应 |
470 |
515 |
305 |
490 |
|
剧烈反应 |
490 |
540 |
350 |
545 |
实验室用氯酸钾来制取氧气,在以上物质中选用催化剂,最好用( )
A.Fe2O3 B.Al2O3 C.CuO D.MgO
思路解析:本题考查氧气的制备过程中催化剂的作用。催化剂能够改变(一般指加快)化学反应速率,但自身质量不发生变化。根据上述表格得知:选择催化剂最佳依据是在条件最低但催化效果最好。
答案:C
4.某同学用氯酸钾和二氧化锰的混合物加热制取氧气时发生了爆炸,分析其可能的原因是( )
A.管受热不均匀 B.气体发生装置漏气
C.二氧化锰中混有可燃性杂质 D.加热温度太高
思路解析:由于加热时体系温度比较高,且产生了大量氧气,只要有可燃物,就可能发生爆炸。
答案:C
3.(经典回放)小兰同学用下图所示的装置测定空气中氧气的体积分数,实验后发现测定氧气的体积分数低于1/5。针对这一事实,你认为下列做法或想法不可取的是( )
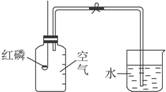
A.查看实验装置是否漏气
B.实验中可能红磷的量不足,没有将瓶内氧气耗尽
C.实验中可能未冷却至室温就打开止水夹,使进入瓶内水的体积减少
D.将红磷改为木炭再重做实验
思路解析:本题旨在探究实验室测定空气中氧气体积的方法。用题给实验方法测定空气中氧气的体积分数若低于1/5,则造成误差的原因可能有三种。一是红磷不足量;二是装置漏气;三是未等瓶内气体冷却就打开了止水夹。这三个方面,无论哪一个方面出问题,所测O2体积分数都会低于1/5。因此,应从这三方面去检查失误原因,切不可用木炭代替红磷再做实验。因木炭燃烧产生的是CO2,CO2填充了所耗O2的体积,瓶内气体压强基本不变,实验目的更难达到。所以用题给实验方法测定空气中氧气体积时,所选可燃物应满足两个条件:①能在空气中燃烧;?②燃烧的产物是固体。
答案:D
2.催化剂在化学反应中所起的作用是( )
A.加快化学反应速率 B.使生成物质量增加
C.改变化学反应速率 D.减慢化学反应速率
思路解析:催化剂可以改变化学反应速率,在生产上我们一般要求加快反应速率,在其他领域则需要用催化剂降低化学反应速率;如食品的防腐、橡胶的防老化等领域。
答案:C
1.工业上制取大量氧气的方法是 ( )
A.加热氯酸钾 B.加热高锰酸钾
C.分离液态空气 D.加热二氧化锰
思路解析:大量氧气的制备即工业制备氧气,一般采用分离液态空气法。A、B都是实验室制备少量氧气的方法;D无法得到氧气。
答案:C
3.燃烧、缓慢氧化、自燃的相同点是( )
A.反应都很剧烈
B.反应时都发光、放热
C.都属于氧化反应
D.都需要达到着火点
思路解析:燃烧、缓慢氧化、自燃,三者的共同点都是与氧气反应,都属于氧化还原反应。
答案:C
快乐时光
考试篇
老师说:“平时考是点心,百吃不厌;
段考是正餐,定时定量;
联考是满汉全席,一次就够。
你们为什么不好好用功呢?”
学生说:“报告老师,我们正在减肥!”
30分钟训练(巩固类训练,可用于课后)
2.某学生在实验室设计了五种制取氧气时使用药品的方案,其中可行的是( )
①用氯酸钾和二氧化锰混合加热②将氯酸钾加热③将高锰酸钾加热④将高锰酸钾和氯酸钾混合加热⑤将二氧化锰加热
A.①②③ B.③④⑤
C.①③④ D.②③⑤
思路解析:氯酸钾直接加热,很难分解;二氧化锰加热不分解,无法产生氧气。故②⑤不可能。
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com