
题目列表(包括答案和解析)
4.(2010山东课改区) 壹圆硬币的外观有银白色的金属光泽,同学们认为它可能是由铁制成的。在讨论时,有同学提出“我们可以先拿磁铁来吸一下”。就“拿磁铁来吸一下”这一过程而言,属于科学探究中的( )
A.假设 B.实验 C.观察 D.做出结论
思路解析:该题考查科学探究的一般方法,注意题目中的“这一过程而言”,题目问的是过程,所以应属于科学探究的实验而不是假设。
答案:B
3.化学变化常伴随能量的改变,这种能量的改变常常表现为___________、___________、___________的放出、吸收。
思路解析:人类研究化学的目的其一就是利用反应放出的能量,主要表现为热能、光能和电能。
答案:热能 光能 电能
2.硫酸铜溶液是__________色的,氧化镁固体是__________色的,氢氧化钠溶液能使__________色的酚酞试液变成__________色。
思路解析:实验时应注意观察现象,不仅是反应的现象,还要观察反应前后各物质的颜色状态等。
答案:蓝 白 无 红
1.下列有关生活常识的说法,正确的是 ( )
A.用完后的废电池应该集中回收处理
B.天然果汁中不含任何化学物质
C.“绿色食品”是指颜色一定为绿色的食品
D.“白色污染”是指白色粉尘造成的污染
思路解析:电池中含有镉等重金属元素,会大面积污染环境,所以应该集中回收处理。B中天然果汁中的水也是一种化学物质。
答案:A
11.(2010河北中考,38) 小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。
他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:
①可能是NaOH ②可能是Na2CO3 ③可能是NaOH与Na2CO3的混合物。
为了验证猜想,他们分别做了下面的实验:
(1)小刚取少量白色粉末,滴加稀盐酸,有气体生成。由此小刚认为白色粉末是Na2CO3。
请判断小刚所得结论是否正确,并简述理由。
_______________________________________________________________________________。
(2)小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色。由此小军认为白色粉末是NaOH。请判断小刚所得结论是否正确,并简述理由。
_______________________________________________________________________________。
(3)小红取少量白色粉末溶于水,向所得溶液中滴加BaCl2试液,有白色沉淀产生。由此判断白色粉末中含有____________。为了验证猜想③,小红继续向溶液中滴加BaCl2试液至不再产生沉淀,然后过滤。你认为她接下来还应进行的实验是______________________________。
在小红所做的实验中,若把BaCl2溶液换成Ba(OH)2溶液是否可行?请简述理由。
解析:(1)白色粉末滴加稀盐酸有气体生成,说明含有Na2CO3,但并不能证明只是Na2CO3,两者的混合物也可以产生气体。(2)向所得溶液中滴加酚酞试液,溶液变为红色,说明溶液是碱性溶液,但Na2CO3溶液也显碱性,故不能确定白色粉末就是NaOH。(3)滴加BaCl2试液,有白色沉淀产生,说明生成了Ba2CO3沉淀,可以判断白色粉末中含有Na2CO3,至沉淀不再产生后过滤出的滤液应滴酚酞(或石蕊)试液,如果滤液显碱性,说明白色粉末中还含有NaOH,不变色说明是纯净的Na2CO3粉末。
答案:(1)不正确,两者混合物也可
(2)不正确,碳酸钠也呈碱性
(3)碳酸钠 向滤液中滴酚酞(或石蕊)试液不可,生成氢氧化钠,影响对氢氧化钠的确定
快乐时光
今天
有一次化学实验课上,老师让学生们配制一定浓度的溶液,并强调标签上要写上是哪天完成的,过一周要用此溶液做实验。几天后,老师突然问一个叫汤姆的学生:“溶液是哪天配制的?”汤姆拿出那瓶已配好的溶液,上面写到:“今天。”
10.有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液,将其任意编号:A、B、C、D、E,进行两两混合实验,其现象如下:
|
实验 |
A+B |
A+E |
B+C |
B+E |
|
现象 |
产生沉淀 |
产生沉淀 |
产生沉淀 |
产生气泡 |
(1)试推断并写出五种溶液中溶质的化学式:
A____________,B____________,C____________,D____________,E____________。
(2)写出有关反应的化学方程式:
A+E________________________________________________________________________。
B+E________________________________________________________________________。
答案:(1)AgNO3 Na2CO3 Ca(NO3)2 KNO3 HCl
(2)AgNO3+HCl====AgCl↓+HNO3 Na2CO3+2HCl====2NaCl+H2O+CO2↑
9.物质A为常见的白色固体,A遇水后放出大量的热并生成微溶于水的白色粉末B;A、B与盐酸反应都能生成C;C溶液与一种钠盐溶液反应,生成难溶于水的D;D遇盐酸又生成C。
(1)写出A、B、C、D的化学式:
A____________,B____________,C____________,D____________。
(2)写出有关反应的化学方程式:
B→C_______________________________________________________________。
C→D_______________________________________________________________。
答案:(1)CaO Ca(OH)2 CaCl2 CaCO3 (2)Ca(OH)2+2HCl====CaCl2+2H2O
CaCl2+Na2CO3====CaCO3↓+2NaCl
8.小明发现一个盛有无色溶液(初中化学常用试剂)的试剂瓶,标签破损(如图所示)。请根据图示提供的信息,对该试剂作出猜想,并设计实验验证。
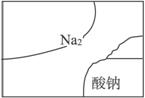
(1)猜想:这种试剂可能是____________。
(2)设计实验(简述步骤、现象和结论):_____________________________________________。
解析:从图中可知,该物质是一种“某酸钠”的盐溶液。也就是说未知的是酸根,可以猜想是碳酸钠或硫酸钠。当然,最好与你熟悉什么物质的鉴别结合起来猜想。
答案:(1)碳酸钠等
(2)取少量试样于试管中,滴加稀盐酸,如果产生能使澄清石灰水变浑浊的气体,说明该试剂确实是碳酸钠溶液
7.(2010江苏南通中考,24) 我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。下表是几种物质在不同温度时的溶解度:
(1)从表中数据可以看出,温度对____________的溶解度影响不大。
(2)要使NH4Cl饱和溶液中的NH4Cl结晶析出,在____________(填“较高”或“较低”)温度下进行比较合适。
|
|
0 ℃ |
20 ℃ |
40 ℃ |
60 ℃ |
|
NaHCO3 |
6.9 |
9.6 |
12.7 |
16.4 |
|
NaCl |
35.7 |
35.8 |
36.6 |
37.3 |
|
NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O====NaHCO3+NH4Cl,该反应能进行的原因是________________________________________________。
解析:从表中可以看出,温度对NaHCO3和NH4Cl的溶解度的影响都比较大,对NaCl的溶解度影响不大;随着温度的升高,水中可溶解的NH4Cl的质量变大,可以通过在较高温度下配置NH4Cl的饱和溶液,然后再降温结晶析出NH4Cl的办法将NH4Cl从溶液中分离出来;NaCl+CO2+NH3+H2O====NaHCO3+NH4Cl这个反应能够进行是因为NaHCO3在水中的溶解度较小,可以结晶析出。
答案:(1)NaCl (2)较低 (3)有溶解度较小的NaHCO3产生
6.有一种白色固体可能含有:BaCl2、NaCl、Na2CO3、Na2SO4和CuSO4中的一种或几种。对该固体进行如下实验。
①取样,加足量的水,充分搅拌,过滤。得到白色沉淀A和无色溶液B。
②在白色沉淀A中加入稀盐酸,沉淀全部溶解,放出能使石灰水变浑浊的无色气体。
③在无色溶液B中加入AgNO3溶液,得到白色沉淀,再加入稀盐酸,白色沉淀不溶解。
请完成下列问题:
(1)原白色固体中一定不含有____________;一定含有____________。
(2)实验①得到的无色溶液B中一定含有的溶质是____________________________________。
(3)原白色固体中可能含有________________________________________________________。
解析:①中过滤后剩下的是无色溶液,说明溶液中没有Cu2+,因此固体中肯定不含CuSO4;白色固体加水混合后生成了白色沉淀,说明含有Ba2+,故白色固体中肯定含有BaCl2;在白色沉淀A中加入稀盐酸,沉淀全部溶解,说明不含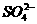 ,因此白色固体中肯定不含Na2SO4和CuSO4;沉淀加入稀盐酸放出能使石灰水变浑浊的无色气体,说明沉淀中含有
,因此白色固体中肯定不含Na2SO4和CuSO4;沉淀加入稀盐酸放出能使石灰水变浑浊的无色气体,说明沉淀中含有 ,而只有Na2CO3中含有
,而只有Na2CO3中含有 ,故白色固体中一定含有Na2CO3。
,故白色固体中一定含有Na2CO3。
答案:(1)CuSO4、Na2SO4 BaCl2、Na2CO3 (2)NaCl (3)NaCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com