
题目列表(包括答案和解析)
11.用如右图所示的装置制取氢气,在多孔塑料板上放锌粒,稀H2SO4由A中加入,若打开弹簧夹,酸液由A中流下与锌粒接触即发生反应,产生的氢气由支管导出,试完成下列问题:
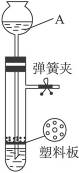
(1)仪器A的名称是_________。
(2)检查此装置的气密性时,关闭弹簧夹,从仪器A处注入适量的___________形成液封后,若看到仪器A内___________,则表明装置气密性良好。
(3)若关闭弹簧夹,容器内继续反应产生的氢气会使容器内___________,将酸液压回仪器A中,使酸液与锌粒___________,反应即自行停止。
(4)若氢气发生装置气密性良好,该同学用排水法收集一试管氢气,经检验不纯,你认为可能的原因是_____________________________________________________________________。
(5)若在塑料隔板上放小块大理石,A中放稀HCl,___________(填“能”或“否”)用弹簧夹控制CO2的发生和停止。
解析:本题考查实验室制H2的简易装置及装置的原理,并且对气密性检查的多样性进行考查。
答案:(1)长颈漏斗 (2)水 液面不变 (3)压强增大 脱离接触 (4)开始冒气泡就收集,氢气中混有了原试管中的空气 (5)能
10.推广使用含10%乙醇的汽油,目的是开发石油替代资源,改善汽车尾气排放。常温下乙醇是一种能溶于水和汽油的液体,能在空气中燃烧。制取乙醇的方法是将淀粉水解生成葡萄糖(化学式为C6H12O6),葡萄糖在酶的作用下发生分解反应转化为乙醇(化学式为C2H5OH)和二氧化碳。另查资料知,纸张等含纤维素的物质也可水解生成葡萄糖。请根据上述信息完成下列问题:
(1)总结乙醇的有关知识:
乙醇的物理性质:_______________________________________________________________,
乙醇的化学性质(用化学方程式表示):_____________________________________________。
(2)写出葡萄糖转化为乙醇的化学方程式:__________________________________________。
(3)若想利用身边的废弃物生产乙醇,你设想的生产过程是:__________________________。
解析:从材料提供的信息可知乙醇的物理和化学性质,乙醇的获取方法。纸张是常见废弃物,从信息可知它也可转为葡萄糖,再转变为乙醇。
答案:(1)乙醇是一种能溶于水和汽油的液体 C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
(2)C6H12O6 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
(3)废弃的淀粉类物质(或纤维素类物质) 葡萄糖
葡萄糖 酒精(如将废弃物写成具体的物品,如剩饭、废纸等也可)
酒精(如将废弃物写成具体的物品,如剩饭、废纸等也可)
9.一些家庭中使用的液化石油气的主要成分是丙烷(C3H8)和丁烷(C4H10),它们的组成、结构相似。根据下列所示的甲烷、乙烷的结构式,完成有关问题:
(1)推测丙烷的结构式:
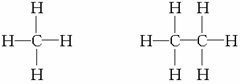
甲烷(CH4) 乙烷(C2H6)
丙烷(C3H8)_______________________________________________________。
(2)写出丁烷在空气中完全燃烧的化学方程式。
解析:由甲烷结构式联想,每个“C”可获取4个“-”来推测。C、H化合物完全燃烧一定生成水和CO2。
答案:(1)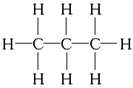
(2)C4H10+9O2 4CO2+5H2O
4CO2+5H2O
8.供选择的仪器装置如下图所示(图中A-G为装置代号,①-⑧为仪器的接口符号)。供选择的药品有:金属钠、铜片、锌粒、炭粉、硝酸、稀硫酸。
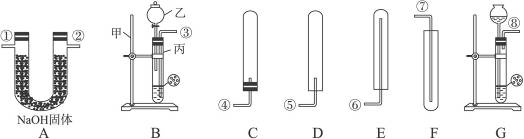
完成下列问题:
(1)写出B装置中的仪器名称:甲___________,乙___________,丙___________。
(2)实验室制取氢气时,常选用的药品是___________和___________;发生反应的化学方程式为________________________________________。
(3)若一个学生选用盐酸为原料之一,则制得的氢气中会含有少量盐酸的酸,如让氢气通过装置(写装置代号)___________,酸雾即可除去,化学反应方程式为________________________;制取和收集的装置是(写装置代号)___________和___________。
(4)请正确连接氢气的制取、除酸雾和收集氢气的装置(写接口符号)___________接___________,___________接___________。
解析:要掌握H2的实验室制法的原理装置、收集方法等,对装置的连接要了解一般的原则,发生装置→净化→干燥→收集装置,净化除杂要“长进短出”。
答案:(1)铁架台 分液漏斗 试管
(2)锌粒 稀硫酸 Zn+H2SO4====ZnSO4+H2↑
(3)A NaOH+HCl====NaCl+H2O G E
(4)⑧ ①(或②) ②(或①) ⑥
7.请回答:氢气作为一种优质能源,目前为什么不能广泛使用?
解析:一种能源,如果要推广使用,必须具备燃烧安全,充足;储存方便,价格低廉等特点。氢气为什么不能推广,应该从上述几个方面来回答。
答案:氢气难储存,生产成本高,这是制约氢气作为优质能源不能大力推广的关键因素。
6.利用自己所学知识或生活常识,解释或完成下列问题:
(1)在清洗沼气池时,能不能在池内点火吸烟?为什么?
(2)汽油是石油分馏的产物,它其中可能含有哪些元素,你能证明吗?
解析:结合沼气的成分来回答;证明物质的组成,对于有机物而言,常采用的方法是把有机物燃烧,根据燃烧产物来分析。
答案:(1)沼气的主要成分是甲烷,甲烷易于燃烧,所以在清理沼气池时不能吸烟,否则可能引发火灾,甚至爆炸
(2)分析有机物的组成,往往采用把有机物燃烧,根据产物及其质量分析该有机物的组成?成分。
具体方法:把石油气通过过量氧气,充分燃烧后,气体通过浓硫酸吸收,测定生成的水的质量(或通过无水氯化钙),然后通过碱石灰,测定产生的二氧化碳的质量。结合有机物的总质量,判断有机物中是否含有氧元素。并能确定各元素的原子个数比
5.2003年4月,我国登山运动员再次登上世界屋脊--珠穆朗玛峰。登山运动员登山时所带的能源是氢化钙(CaH2),它能与水剧烈反应生成氢气和氢氧化钙,该反应的化学方程式为:_____________________________________________________________________________。

当登山运动员需要热量时,将上述反应中生成的氢气点燃,该过程中实现了能量转化,即___________能转化为___________能。
解析:书写化学方程式主要是先分析反应物(CaH2与H2O)和生成物(H2和Ca(OH)2),并能正确地配平即可完成。
答案:CaH2+2H2O====Ca(OH)2+2H2↑ 化学 热(内)
4.2010黑龙江中考,2 6月5日是“世界环境日”。我国的环保主题是“人人参与,创建绿色家园”。下列有关能源的开发和利用不符合该主题的是( )
A.氢能是理想的新型能源,它具有资源丰富、燃烧放热多、产物不污染环境等优点
B.为减少空气污染,应提倡使用乙醇汽油
C.开发和利用太阳能、水能、风能等能源
D.煤、石油、天然气等化石燃料为不可再生能源,应禁止使用
解析:化石燃料依然是现代社会的主要能源物质,只能改造、限制利用传统燃料,同时,去开发并使用新型能源物质。
答案:D
3.手机中使用的锂(Li)电池是新型的高能电池,某种锂电池的总反应可表示为Li+MnO2====LiMnO2。此反应中锂元素的化合价变化为0→+1,下列对锰元素的化合价变化判断正确的是( )
A.+4→+3 B.+2→+3
C.0→+2 C.-4→-2
解析:本题可利用化合物中化合价代数和为0的原则对MnO2、LiMnO2两种物质中Mn的化合价分别计算得出。(也可利用化合价升降相等,化合价升高1价,必定也会降低1价判断)
答案:A
2.煤矿井下禁止吸烟,以防点燃坑道内的可燃性气体而引起爆炸,这种可燃性的气体主要是( )
A.氨气 B.甲烷
C.氢气 D.液化石油气
解析:坑道气、天然气、沼气等的主要成分均为甲烷。
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com