
题目列表(包括答案和解析)
3.向密闭的容器中通入氧气(含a个氧气分子)和一氧化氮(含有b个一氧化氮分子)气体,已知:2NO+O2====2NO2,则最终容器内氧原子和氮原子个数之比为( )
A.2(a+b)/b ?B.2a/b? C.(2a+b)/b ? D.b/a?
思路解析:此题为质量守恒定律的运用题。质量守恒定律不仅体现在宏观上总质量相等、元素的质量相等,还体现在微观上原子个数相等。NO和O2发生反应,反应前后氮原子和氧原子个数保持不变,即氮原子数为b个,氧原子数为(2a+b)个。
答案:C
2.利用化学方程式进行计算的依据是( )
A.化学方程式表示了一种化学反应的过程
B.化学方程式表示了反应物、生成物和反应条件
C.化学方程式表示了反应前后反应物和生成物的质量关系
D.化学方程式中,各反应物质量比等于各生成物质量比
思路解析:化学方程式的计算理论依据是化学方程式的量的意义(质量比、粒子数目比)。
答案:C
1.6 g 4.4 g x?
(1)11/4.4 g=9/x x=3.6 g
(2)根据质量守恒定律:Y的质量为:4.4 g+3.6 g-1.6 g=6.4 g
Y与M的质量之比是:6.4 g∶3.6 g=16∶9。
答案:B
1.在反应X+2Y====R+2M中,当1.6 g X与Y完全反应后,生成4.4 g R,且反应生成的R和M的质量之比为11∶9,则在此反应中Y和M的质量之比为( )
A.23∶9 B.16∶9 C.32∶9 D.46∶9
思路解析:此题考查的知识是物质之间发生的反应按一定的质量比进行,反应物和生成物的质量总和相等(即质量守恒)。
X+2Y====R + 2M
质量之比: 11 9
15.在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,使之充分反应后有下列情况:
(1)若反应后锌有剩余,则溶液中所含溶质为________。
(2)若反应后,将溶液过滤,所得固体物质加盐酸没有气体产生,则固体物质中一定有________,可能有________。
(3)若反应后,将析出的金属过滤,向滤液中滴加NaCl溶液,有不溶于稀HNO3的白色沉淀生成,则此时溶液中含有的溶质为________。
解析:(1)根据金属活动性Zn>Cu>Ag,若Zn剩余,则Cu2+、Ag+全部置换出,溶质为Zn(NO3)2。
(2)固体加盐酸,无气体产生,则Zn完全反应,则可能Cu2+未完全置换,所以固体中一定有Ag,可能有Cu。
(3)根据题意,滤液中有AgNO3,则一定有Cu(NO3)2和Zn(NO3)2。
答案:(1)Zn(NO3)2 (2)Ag Cu (3)AgNO3、Cu(NO3)2、Zn(NO3)2
快乐时光
绿色食品
秘书小张回乡探亲,带回一箱家乡特产--芦笋罐头。
傍晚,小张亲自送到厂长府上,说是绿色食品,能抗癌防衰老,请厂长品尝。厂长甚是高兴,执意挽留小张共进晚餐,并让夫人开一瓶芦笋罐头上桌。
片刻,菜上齐了,小张给厂长夹了一块芦笋说:“厂长,你尝尝。”
厂长揉揉眼睛,瞅了瞅说:“小张!这明明是白的,你怎么说是绿色食品呢?我才知道:原来你是色盲啊!”
14.(2010福建福州) 某蔬菜基地在种植蔬菜时,常采用下列方法。
(1)施用适量的氮肥可以使种植的蔬菜叶色浓绿。
①下列化肥中,属于氮肥的是___________。(填字母)
A.碳酸氢按(NH4HCO3) B.草木灰(主要成分K2CO3) C.磷矿粉(Ca3(PO4)2)
②草木灰呈碱性,你认为它___________(填“能”或“不能”)与所选的氮肥混合施用。
理由是________________________________________________________________________。
(2)用大棚种植蔬菜时,常向大棚中补充气体肥料CO2。
①目的是促进绿色植物的___________作用。
②若提供的气体肥料CO2中混有少量的SO2,为了除去SO2,现设计以下两种方法。
甲方法:将气体通过足量的碳酸氢钠溶液。
乙方法:将气体通过足量的氢氧化钠溶液。
[提供资料] CO2与NaHCO3不会发生反应;SO2+2NaHCO3====NaSO3+H2O+2CO2;SO2+2NaOH====Na2SO3+H2O。
请你利用提供的资料和所学的知识分析:上述___________方法(填“甲方法”或“乙方法”)可行,理由是________________________________________________________________________。
答案:(1)①A ②不能 二者混合使用会生成氨气,降低肥效
(2)①光合 ②甲方法 CO2与NaHCO3不会发生反应,SO2与NaHCO3能反应,不但能除去SO2,而且还能增加CO2的含量
13.右图所示是一个现代化植物生产车间(温室),植物生长所需要的气态肥料可以通过调节二氧化碳来补充。
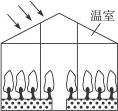
(1)在这个温室中,以人工配制的营养液无土栽培蔬菜满足了植物对温度及矿物质元素的要求,要实现通过补充二氧化碳使作物增产,所需要的另一条件是________,若栽培的的作物是叶菜类,营养液中应该适当增加___________肥。
(2)此温室可视为一个小型的生态系统,构成该系统的生产者是_________________________。
(3)碳酸氢铵是一种常用的化肥,俗称碳铵。请你简述一点使用时的注意事项:_____________
______________________________________________________________________________。
解析:植物的光合作用可用下列文字表达式表示:
水+二氧化碳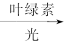 有机物+氧气,从这个反应中我们可以知道,植物进行光合作用的生产者是植物的叶绿体,原料是水和二氧化碳,生产条件是光照。
有机物+氧气,从这个反应中我们可以知道,植物进行光合作用的生产者是植物的叶绿体,原料是水和二氧化碳,生产条件是光照。
答案:(1)光照 氮 (2)植物(叶绿体) (3)密封贮存在阴凉处(或不能与碱性物质混合施用等)
12.小红参加化学课外小组的活动,活动的内容是在实验室练习配制农药波尔多液。其配制过程是:称取1 g胆矾放入A容器中,再加90 mL水搅拌,完全溶解制成硫酸铜溶液;称取1 g生石灰放入B容器中,先加少量水搅拌,使生石灰变成熟石灰,再加入10 mL水搅拌,制成石灰乳。将硫酸铜溶液慢慢地倒入石灰乳中,同时不断搅拌,即成波尔多液。请完成:
(1)写出配制过程中有关反应的化学方程式:
①________________________________________________________________,
②________________________________________________________________。
(2)小红用的A容器能否选用铁制容器?___________,理由是________________________。
(3)配制过程中,小红需用到哪些主要化学仪器?请写出仪器的名称:___________、___________、___________、___________。
解析:在配制农药波尔多液的过程中主要发生了两个化学反应:一个是生石灰与水的反应,另一个是硫酸铜与氢氧化钙的反应。铁的金属活动性比铜强,能置换硫酸铜溶液中的铜。需要哪些仪器可根据每一步的操作来填写:称取需托盘天平、量取体积可用量筒、盛水可用烧杯、搅拌可用玻璃棒。
答案:(1)CaO+H2O====Ca(OH)2 CuSO4+Ca(OH)2====Cu(OH)2↓+CaSO4
(2)不能 因为铁会与硫酸铜溶液发生反应,导致铁制容器腐蚀和农药失效
(3)托盘天平 量筒 烧杯 玻璃棒
11.A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物,鉴别方法见右图所示。(所加溶液均过量,使反应完全)
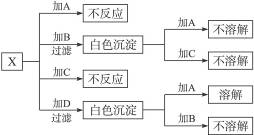
完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A___________,B________,C________,D________,X________。
(2)写出下列有关反应的化学方程式:
X和B:________________________________________________________。
X和D:________________________________________________________。
解答:(1)由于X含Mg2+,能将Mg2+沉淀的有OH-,而条件中产生两种沉淀,因此X含有的阴离子必然能将Ba2+沉淀,则阴离子可能为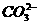 、
、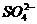 ,但BaSO4不溶于水也不溶于酸,而BaCO3易溶于酸,由于A、C与X不反应,则应为盐酸或NaCl,X与B产生的沉淀不溶于A、C,则沉淀应为BaSO4,X为MgSO4,B为Ba(NO3)2,A为盐酸,D为氢氧化钠,C为NaCl。
,但BaSO4不溶于水也不溶于酸,而BaCO3易溶于酸,由于A、C与X不反应,则应为盐酸或NaCl,X与B产生的沉淀不溶于A、C,则沉淀应为BaSO4,X为MgSO4,B为Ba(NO3)2,A为盐酸,D为氢氧化钠,C为NaCl。
(2)MgSO4+Ba(NO3)2====Mg(NO3)2+BaSO4↑
MgSO4+2NaOH====Na2SO4+Mg(OH)2↓
10.请你参加某中学初三学生识别化肥的探究活动。他们从家中拿来了四种化肥,分别是硫酸钾、氯化钾、碳酸铵和硝酸铵。
第一步:称取化肥各10 g,进行研细。
第二步:取上述化肥各少量于研钵中,分别加入少量熟石灰粉末,混合研磨,能嗅到剌激性气味的是两种铵盐。请将下列硝酸铵与熟石灰反应的化学方程式填写完整:
2NH4NO3+_________====________+2NH3↑+2H2O。
第三步:另取两种铵盐各少量于试管中,都滴入少量稀盐酸,无明显现象的是氯化铵和硝酸铵,有气泡产生的是碳酸铵,写出反应的化学方程式:________________________________。
第四步:另取两种钾盐,分别在试管中配成溶液,各滴入几滴氯化钡溶液,根据盐的溶解情况判断:有白色沉淀产生的是___________,无明显现象的是___________。写出生成白色沉淀时发生反应的化学方程式:____________________________________________________。
解析:此题主要考查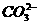 和
和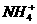 的检验方法,运用这两种离子检验方法的化学反应、实验现象进行解题。第四步的解题关键要知道硫酸钡(BaSO4)是不溶的白色沉淀。
的检验方法,运用这两种离子检验方法的化学反应、实验现象进行解题。第四步的解题关键要知道硫酸钡(BaSO4)是不溶的白色沉淀。
答案:第二步:Ca(OH)2 Ca(NO3)2
第三步:(NH4)2CO3+2HCl====2NH4Cl+H2O+CO2↑
第四步:硫酸钾(K2SO4) 氯化钾(KCl) K2SO4+BaCl2====BaSO4↓+2KCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com