
题目列表(包括答案和解析)
1.许多城市都禁止燃放烟花爆竹,原因是燃放烟花爆竹时( )
①产生有毒气体 ②产生噪声 ③产生粉尘 ④易引起火灾
A.①②③④ B.①③④ C.②④ D.②③④
思路解析:本题联系生活实际,燃放烟花爆竹时除了产生噪声、粉尘,易引起火灾之外,还会产生二氧化硫等有毒的气体。
答案:A
8.工业上用电解氧化铝的方法制取单质铝的化学方程式为:2Al2O3 4Al+3O2。对“电解10 kg氧化铝最多可生产多少千克铝?”一题,小明和小亮两位同学分别采用了两种不同的计算方法。
4Al+3O2。对“电解10 kg氧化铝最多可生产多少千克铝?”一题,小明和小亮两位同学分别采用了两种不同的计算方法。
|
小明同学的解法 |
小亮同学的解法 |
|
解:设铝的质量为X。 2Al2O3  4Al+3O2 4Al+3O2204 108 10 kg ?X? 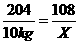 X=5.3 kg 答:最多可生产5.3 kg铝。 |
解:氧化铝中铝元素的质量分数: ×100% ×100%=  ×100% ×100%=53% 铝的质量为:10 kg×53%=5.3 kg 答:最多可生产5.3 kg铝。 |
请你完成下列下列问题:
(1)你认为他们的解题思路和方法都正确吗?
(2)对“34 kg过氧化氢完全分解可产生多少克氧气?”一题,你认为也能用上述两种方法解答吗?试试看,请把你用的解法过程写出来。
思路解析:小明同学是根据化学方程式进行计算的,小亮同学是根据在化学反应前后氧元素的质量相等来做的,所以他们的解题思路是正确的。对“34 kg过氧化氢完全分解可产生1多少克氧气?”一题,可以用小明同学的做法根据化学方程式的计算来做,但不能用小亮同学的做法,因为过氧化氢中的氧元素并没有全部转变成氧气。
答案:(1)他们的解题思路和方法都正确。
(2)16 kg
7.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的含量,取来了一些矿石样品,并取稀盐酸200 g,平均分成4份,进行实验。
|
实验 |
1 |
2 |
3 |
4 |
|
加入样品的质量/g |
5 |
10 |
15 |
20 |
|
生成CO2的质量/g |
1.76 |
3.25 |
4.4 |
M |
(1)哪几次反应矿石有剩余?_______________。
(2)上表中M的数值是____________。
(3)试计算这种石灰石中碳酸钙的质量分数。
思路解析:第一次实验中样品全部反应,盐酸有剩余,第二次实验中样品也全部反应,盐酸仍有剩余,因为反应的样品质量与生成二氧化碳的质量对应成比例,在第三次实验中如果15 g样品全部参加反应,会生成1.76 g×3=5.28 g二氧化碳,实际上只生成了4.4 g。这说明样品没有全部反应,有剩余,则盐酸全部反应生成4.4 g二氧化碳。在第四次实验中,盐酸也全部反应,生成4.4 g二氧化碳。
解:设5 g石灰石中碳酸钙的质量为X。
CaCO3+2HCl====CaCl2+H2O+CO2
100 44
X ?1.76 g
 X=4 g
4 g÷5 g=80%
X=4 g
4 g÷5 g=80%
答案:(1)第一、二次 (2)4.4 g (3)80%
我创新 我超越
6.图5-3是分析一种化合物组成的实验装置。

图5-3
实验结果如下:
|
|
实验前 |
实验后 |
|
铜的氧化物+玻璃管 |
137.8 g |
131.4 g |
|
氯化钙+U形管 |
100.8 g |
108.0 g |
注:玻璃管质量为80.2 g。
试根据实验数据求:
(1)完全反应后生成水的质量为_______g。
(2)生成的水中氧元素的质量为_______g。
(3)铜的氧化物中铜元素的质量为_______g。
(4)铜的氧化物中铜元素和氧元素的质量比为_______。
(5)铜的氧化物中铜、氧原子个数的最简整数比为_______(已知铜和氧的相对原子质量分别为64和16);
(6)写出铜的氧化物的化学式:____________________________。
思路解析:(1)完全反应后生成的水的质量为:108.0 g-100.8 g=7.2 g。
(2)生成的水中氧元素的质量为:137.8 g-131.4 g=6.4 g。
(3)铜的氧化物中铜元素的质量为:137.8 g-80.2 g-6.4 g=51.2 g。
(4)铜的氧化物中铜元素和氧元素的质量比为:51.2 g∶6.4 g=8∶1。
(5)铜的氧化物中铜、氧原子个数的最简整数比为:(8∶1)/(64∶16)=2∶1。
(6)铜的氧化物的化学式:Cu2O。
答案:(1)7.2 (2)6.4 (3)51.2 (4)8∶1 (5)2∶1 (6)Cu2O
5.在反应2A+B====2C中,1.6 g的A完全反应生成2 g C,又知B的相对分子质量为32,则C的相对分子质量为( )
A.28 B.64 C.44 D.80
思路解析:本题是将质量守恒定律的具体内容应用于利用化学方程式计算中的综合题。在列比例式关系时一定要明确质量守恒定律的具体内容与化学方程式中化学式前的化学计量数无关,即参加反应的B物质的质量不等于2×2 g-2×1.6 g;而物质的相对分子质量总和却与化学方程式中化学式前的化学计量数有关。
答案:D
我综合 我发展
4.将A、B、C三种物质各16 g混合加热,充分反应后混合物中有12 g A、27 g C和一定质量的D,已知B完全反应。若A、B、C、D的相对分子质量分别为16、32、44、18,则该反应的化学方程式可表示为( )
A.2A+B====C+2D B.A+2B====C+2D C.2A+B====2C+D D.A+B====C+D
思路解析:此题由反应物、生成物间反应的质量比去确定化学方程式中各物质前的化学计量数。解题的关键是理解反应各物质的质量、相对分子质量与化学计量数三者间的关系。解题时首先根据质量守恒定律确定A、B、C、D的质量。
答案:B
3.向密闭的容器中通入氧气(含a个氧气分子)和一氧化氮(含有b个一氧化氮分子)气体,已知:2NO+O2====2NO2,则最终容器内氧原子和氮原子个数之比为( )
A.2(a+b)/b ?B.2a/b? C.(2a+b)/b ? D.b/a?
思路解析:此题为质量守恒定律的运用题。质量守恒定律不仅体现在宏观上总质量相等、元素的质量相等,还体现在微观上原子个数相等。NO和O2发生反应,反应前后氮原子和氧原子个数保持不变,即氮原子数为b个,氧原子数为(2a+b)个。
答案:C
2.利用化学方程式进行计算的依据是( )
A.化学方程式表示了一种化学反应的过程
B.化学方程式表示了反应物、生成物和反应条件
C.化学方程式表示了反应前后反应物和生成物的质量关系
D.化学方程式中,各反应物质量比等于各生成物质量比
思路解析:化学方程式的计算理论依据是化学方程式的量的意义(质量比、粒子数目比)。
答案:C
1. 6 g 4.4 g x?
(1)11/4.4 g=9/x x=3.6 g
(2)根据质量守恒定律:Y的质量为:4.4 g+3.6 g-1.6 g=6.4 g
Y与M的质量之比是:6.4 g∶3.6 g=16∶9。
答案:B
1.在反应X+2Y====R+2M中,当1.6 g X与Y完全反应后,生成4.4 g R,且反应生成的R和M的质量之比为11∶9,则在此反应中Y和M的质量之比为( )
A.23∶9 B.16∶9 C.32∶9 D.46∶9
思路解析:此题考查的知识是物质之间发生的反应按一定的质量比进行,反应物和生成物的质量总和相等(即质量守恒)。
X+2Y====R + 2M
质量之比: 11 9
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com