
题目列表(包括答案和解析)
8.(2010江苏徐州中考,25) 小明在学习金属活动性顺序时,对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”这句话产生了好奇。为什么用“一般”这个词呢?难道还有例外吗?
[查阅资料]Na性质活泼,常温下,与氧气反应,也可以与水反应放出氢气。
[实验与分析]①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投入蒸馏水中,发现钠块立刻熔化成银白色小球,在水面上到处游动,滴入酚酞试液后溶液变成红色;③往硫酸铜溶液中,投入一小块钠,又出现蓝色沉淀,但没有红色物质析出。
(1)金属钠保存在煤油中的原因________________________。
(2)从实验②中,你能得出哪些信息?(任写三条)____________; ____________;____________。
(3)写出钠与硫酸铜溶液反应的化学方程式______________________;____________________。
[结论]活动性较强的金属不一定将位于其后面的金属从它们的盐溶液中置换出来,而是置换出H2。
解析:本题为信息给予题,根据金属钠的相关资料,分析金属钠的性质,判断金属钠的保存方法、活泼性、与水反应的产物等,并能写出反应的方程式。金属钠与水反应生成氢气和碱,碱与铜离子反应生成沉淀氢氧化铜,为蓝色沉淀。
答案:(1)防止钠与水、氧气反应
(2)钠为银白色金属、密度比水小、质软、熔点低、反应放热、与水反应的生成物中有碱性物质等合理答案均可
(3)2Na+2H2O====2NaOH+H2↑ 2NaOH+CuSO4====Na2SO4+Cu(OH)2↓
快乐时光
化学课上,老师提问一学生:“如果我把这枚银圆投入稀硫酸中,可以溶解吗?”
学生:“当然不会!”
老师:“为什么呢?”
学生:“如果能够溶解的话,你是舍不得投进去的!
7.镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源。
(1)占地球表面积70%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中的MgCl2 Mg(OH)2
Mg(OH)2 MgCl2·6H2OMgCl2Mg
MgCl2·6H2OMgCl2Mg
①在实验室进行过滤操作时需要用到玻璃棒,其作用是________________________。
②电解熔融氯化镁的过程中,____________能转化为____________能。
(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为2Mg+CO2====C+2MgO,此反应类型属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为-3。据此写出
氮化镁的化学式____________________________________。
解析:金属镁从海水中用碱液沉淀得到,经过过滤、溶解、结晶,得到MgCl2·6H2O,除去结晶水,经过电解即可得到该金属元素镁。本题以信息为载体,把金属镁、镁盐等的性质总结起来。
答案:(1)①引流 ②电 化学 (2)①C ②Mg3N2
6.含有硝酸锌、硝酸镁、硝酸铜、硝酸银四种溶质的溶液中加入一定量的铁粉,充分反应后过滤,滤纸上一定有________________________,滤液中一定有____________;如果滤纸上有铜,则滤纸上一定也有________________________,滤液中一定有____________,滤液中一定没有____________;如果滤纸上有铁,则滤纸上一定同时还有____________,滤液中一定有____________________________________。
解析:活泼金属可以置换出不活泼的金属单质。故充分反应后溶液中存在的是最不活泼的金属银单质;滤液中一定存在硝酸亚铁和没有反应的硝酸锌和硝酸镁;如果铜被置换出来,那么银也一定被置换出来了;滤液中一定存在硝酸亚铁和没有参加反应的硝酸锌和硝酸镁;滤液中一定没有硝酸银和硝酸铜。
答案:银 硝酸亚铁、硝酸镁、硝酸锌 银 硝酸亚铁、硝酸镁、硝酸锌 硝酸银 银和铜 硝酸亚铁、硝酸镁、硝酸锌
5.写出下列变化的化学反应方程式。
(1)用砂纸打磨过的铝片放置在空气中______________________________________________。
(2)铁钉在稀硫酸溶液中__________________________________________________________。
(3)铁丝浸泡在硫酸铜溶液中______________________________________________________。
解析:本题考查几种金属的基本性质。砂纸打磨过的铝片,暴露在空气中的是金属铝,被空气中的氧气氧化生成氧化铝。铁钉在稀硫酸中反应,生成硫酸亚铁放出氢气。铁丝浸泡在硫酸铜溶液中,与硫酸铜发生置换反应,生成硫酸亚铁。
答案:(1)4Al+3O2====2Al2O3 (2)Fe+H2SO4====FeSO4+H2↑ (3)CuSO4+Fe====FeSO4+Cu
4.日常生活中使用铁锅炒菜,并加入适量的食醋,就会增加人体对的摄入量,从而达到预防缺铁性贫血病的目的。已知醋酸在水溶液中能电离出H+和CH3COO-,并具有酸的一切通性。请用化学方程式表示用铁锅炒菜加醋能预防贫血病的原理:____________________________。
解析:这是一道化学与生物知识渗透的跨学科试题。旨在要求学生用化学知识解释缺铁性贫血病的原因。缺铁性贫血实质上是人体内含铁血红蛋白的含量减少。用铁锅炒菜会有少量单质铁随菜进入人体,在胃酸的作用下生成人体可吸收的亚铁离子(Fe2+)。炒菜时若放点食醋,少量单质铁在醋酸的作用下也可转化为人体可吸收的铁。所以用铁锅炒菜加食醋能预防缺铁性贫血病。
答案:Fe2+或铁元素 Fe+2CH3COOH====(CH3COO)2Fe+H2↑
3.在日常生活中,用于铁栏杆外层涂料的“银粉”大多是金属____________;家用热水瓶内胆壁的银白色金属是____________;温度计中填充的金属是____________;灯泡里作灯丝的金属是____________;铝器表面有一层致密而结实的薄膜,其主要成分是____________。
解析:用于铁栏杆外层涂料的“银粉”,主要成分是铝粉,铝可以形成一层致密的氧化物保护膜,有利于保护内部金属;白银具有很好的金属光泽,可以反射热量,使保温瓶保温;温度计中填入了金属汞,金属汞熔点低,膨胀系数变化小;金属钨熔点高,难以熔化;铝可以形成一层致密的氧化膜,难以被氧化腐蚀。
答案:铝 银 汞 钨 氧化铝
2.铜和铝是日常生活和生产中重要的金属。钛(Ti)有许多神奇的性能,越来越引起人们的关注,是21世纪的重要金属之一。依据三种金属的性质和用途,判断下列说法错误的是( )
A.钛或钛合金放到海水中数年,取出后仍光亮如初,这说明金属钛具有很强的抗腐蚀性
B.将大小、厚薄相等的铜、铝、钛分别放入盛有稀盐酸的试管中,观察到盛钛的试管放出气泡缓慢,盛铝的试管放出气泡快,盛铜的试管无现象,由此可推测三种金属的活动性顺序为Al>Cu>Ti
C.某同学的铜制眼镜框表面出现了绿色物质(主要成分Cu2(OH)2CO3),可用稀盐酸除去
D.高层建筑常采用铝合金门窗而不采用铁门窗,主要原因是铝的密度小且易形成一层致密的氧化物薄膜
解析:本题主要考查金属铜、铝、铁的性质和用途。钛是一种新型的金属,它熔点较高、密度较小、机械强度高、易加工成形、有耐腐蚀性能等,所以常用来制海轮和舰艇的外壳。它的金属活动性比铝弱,比铜强。铝的密度小,且易在表面形成一层致密的氧化物薄膜,因此高层建筑常用铝合金门窗而不用铁门窗。铜在空气中也能生锈,其主要成分是Cu2(OH)2CO3,俗称铜绿,属于碱类物质,故铜制眼镜框上出现了铜绿,可用稀盐酸清洗。综上所述,可知B说法错误。
答案:B
1.除去铜粉中少量铁粉,不可采用的方法是( )
A.用磁铁吸引 B.加入足量稀盐酸再过滤
C.加适量CuSO4溶液 D.在空气中灼热
解析:在空气中灼烧,铁粉和铜粉都被氧化生成金属氧化物。
答案:D
7.(2010山东滨州中考,15) 下列四个化学反应中,符合图中漫画情景的是( )
A.Zn+CuCl2====ZnCl2+Cu B.Fe2O3+3CO====2Fe+3CO2
C.2CuO+C====2Cu+CO2↑ D.Fe+H2SO4====FeSO4+H2↑
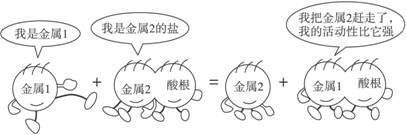
解析:根据漫画,应该属于活泼金属与不活泼金属的盐反应,生成新的金属和新的盐,属于置换反应。
答案:A
30分钟训练(巩固类训练,可用于课后)
6.将过量的铁粉投入硫酸和硫酸铜的混合溶液中,充分反应后过滤,滤出剩余的铁和生成的铜,在滤液里含有的物质是( )
A.FeSO4 B.CuSO4 C.Fe2(SO4)3 D.H2SO4
解析:铁粉和硫酸反应,生成硫酸亚铁和氢气,硫酸铜也和单质铁发生置换反应生成硫酸亚铁和单质铜。故最后溶液中的溶质只有硫酸亚铁。
答案:A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com