
题目列表(包括答案和解析)
5.诺贝尔化学奖获得者哈迈德泽维尔,开创了“飞秒化学”的新领域,使运用激光光谱技术观察进行化学反应分子中原子的运动成为可能。你认为该技术不能观察到的是( )
A.化学变化中反应物分子的分解 B.反应中原子的运动
C.化学反应中生成物分子的形成 D.原子核的内部结构
思路解析:运用激光光谱技术观察化学反应中原子的运动,原子核体积只占原子体积的几千亿分之一,因此此技术无法观察到原子核的内部结构。
答案:D
4.在一个玻璃容器中,加入约60 mL水,向水中加入一小块糖块,在容器外壁用铅笔沿液面画一条水平线,当糖块溶解后,液面与水平线哪一个高,并解释这一现象。
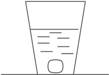
图3-5
思路解析:这是考查粒子之间有间隔的一道题。
答案:当糖块溶解后,液面降低;因为糖的粒子扩散到水的粒子中间去了,粒子间有间隔。
3.氧气降温加压变成液氧,氧分子的主要变化是( )
A.分子间的间隔 B.分子的质量 C.分子的体积 D.分子的性质
思路解析:由氧气变成液氧,没有新物质生成,则分子本身没有改变,那么分子的质量、体积、性质都不变。加压时只是氧分子之间的间隔缩小。
答案:A
2.下列物质含有氧分子的是( )
A.过氧化氢 B.氧化铜 C.空气 D.二氧化碳
思路解析:过氧化氢、氧化铜、二氧化碳这三种纯净物都是由各自的分子构成的,不含氧分子。空气是由氮气、氧气等物质组成的,氧气是由氧分子构成的,则空气中含氧分子。
答案:C
1.某同学在电脑上绘制的表示气体粒子的示意图,图中“ ”和“
”和“ ”分别表示两种不同的原子。其中表示混合物的是( )
”分别表示两种不同的原子。其中表示混合物的是( )

图3-4
思路解析:纯净物和混合物的概念从宏观角度理解为“一物”与“多物”;从微观角度来看,由分子构成的物质,含一种分子的是纯净物,含多种分子的是混合物。本题各图直观地反映了物质的微观构成,因此要从微观角度去认识。选项B、D是由同种分子构成的,为纯净物;选项A是由不同种原子直接构成的,选项C是由不同种分子构成的,是混合物。
答案:AC
9.根据质量守恒定律,6 g镁和8 g氧气充分反应后,可能生成14 g氧化镁。这种说法是否正确?为什么?如不正确,请加以改正。
思路解析:在化学反应中,各反应物之间是按照一定的质量比相互作用的。因此,质量守恒定律中“参加化学反应的各物质的质量总和”就不是任意比例的反应物的质量的简单加和,而应是按一定的质量比进行反应的各反应物的质量总和。所以本题简单地用:6 g + 8 g=14 g的计算方法就得出生成物氧化镁的质量是错误的。
答案:2Mg +
O2 2MgO
2MgO
2×24 32
6 g 8 g
由于 ,所以氧气过量。
,所以氧气过量。
设6 g镁能与氧气反应的质量为x
2Mg +
O2 2MgO
2MgO
48 32
6 g x

x=4 g
生成氧化镁的质量:6 g+4 g=10 g
所以上述说法可以这样改正:根据质量守恒定律,6 g镁和4 g氧气恰好完全反应后,可以生成10 g氧化镁。
8.早在17世纪,质量守恒定律发现之前,英国化学家玻义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于玻义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律。
答案:(1)金属燃烧是金属和氧气发生化合反应,生成金属氧化物。根据质量守恒定律可知,参加反应的金属与氧气的质量之和等于生成的金属氧化物的质量。生成的金属灰是金属氧化物,所以金属灰的质量比原来金属的质量增加了。
(2)分别称量反应前后密闭容器的质量。
13.6 g÷85%=16克
答案:(1)12.5 (2)16
0.8x 6.4 g y

x=12.5克

y=13.6克
7.火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式为:2CaCO3(粉末) + 2SO2+ O2====2CaSO4+2CO2
(1)若100克废气中含6.4克二氧化硫,则处理100克这种废气需含碳酸钙(CaCO3)80%的石灰石___________克。
(2)处理上述100克废气,可得到含CaSO4 85%的粗产品_________克。
思路解析:题中给出的化学方程式,即为计算的依据。
设需含CaCO3 80%的石灰石的质量为x,生成纯CaSO4的质量为y。
2CaCO3+2SO2+O2====2CaSO4+2CO2
200 128 272
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com