
题目列表(包括答案和解析)
19.纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:Zn +2OH- →Zn(OH)2 +2e-; Ag2O +H2O +2e- →2Ag +2OH-。下列说法中,正确的是( )
A. 锌发生还原反应,氧化银发生氧化反应 B. 锌是负极,氧化银是正极
C.溶液中OH-向正极移动,K+、H+ 向负极移动
D.在电极放电过程中,电解质溶液的酸碱性基本保持不变
18. 元素A和B的原子序数都小于18,已知A元素的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a-b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有 ( )
A、能与水反应 B、能与硫酸反应 C、能与NaOH反应 D、能与碳酸钠反应
17. 向恒温、恒容(2L)的密闭容器中充入2 mol SO2和一定量的O2,发生反应:2SO2(g)+O2(g) 2SO3(g);△H= -197.74 kJ·mol-1,4min后达到平衡,这时c(SO2)=0.2mol
L-1,且SO2和O2的转化率相等。下列说法中,不正确的是( )
2SO3(g);△H= -197.74 kJ·mol-1,4min后达到平衡,这时c(SO2)=0.2mol
L-1,且SO2和O2的转化率相等。下列说法中,不正确的是( )
A.2min时,c(SO2)=0.6mol L-1
B.用O2表示4min内的反应速率为0.1mol·(L·min) -1
C.再向容器中充入1mol SO3,达到新平衡,n(SO2):n(SO3)=2:1
D.4min后,若升高温度,平衡向逆方向移动,平衡常数K增大
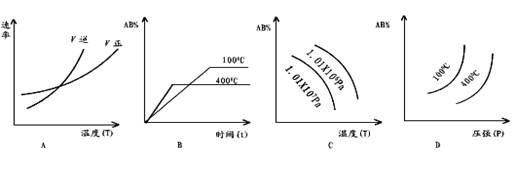
13、对于可逆反应,2AB3(g)  A2(g)
+3B2(g) ΔH > 0,下列图像正确的是( )
A2(g)
+3B2(g) ΔH > 0,下列图像正确的是( )

A.2H2(g)+O2(g)====2H2O(g) ΔH=-Q1 2H2(g)+O2(g)====2H2O(l) ΔH=-Q2
B.S(g)+O2(g)====SO2(g) ΔH=-Q1 S(s)+O2(g)====SO2(g) ΔH=-Q2
C.C(s)+ O2(g)====CO(g) ΔH=-Q1 C(s)+O2(g)====CO2(g) ΔH=-Q2
O2(g)====CO(g) ΔH=-Q1 C(s)+O2(g)====CO2(g) ΔH=-Q2
D.H2(g)+Cl2(g)====2HCl(g) ΔH=-Q1  H2(g)+
H2(g)+  Cl2(g)====HCl(g) ΔH=-Q2
Cl2(g)====HCl(g) ΔH=-Q2
12.发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知:N2(g) + 2O2(g) = 2NO2(g); △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g); △H = – 534kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是( )
A.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(l);△H = – 1135.7kJ/mol
B.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = – 1000.3kJ/mol
C.N2H4(g) + NO2(g) =3/2N2(g) + 2H2O(l);△H = – 1135.7kJ/mol
D.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = – 1135.7kJ/mol
11.镍氢电池是近年来开发出来的可充电电池,它可以取代会产生镉污染的镍镉电池。电池的总反应式是:1/2 H2+NiO(OH) Ni(OH)2。根据此反应式判断,下列叙述中正确的是
( )
Ni(OH)2。根据此反应式判断,下列叙述中正确的是
( )
A.电池放电时,电池负极周围溶液的pH不断增大 B.电池放电时,镍元素被氧化 C.电池充电时,氢元素被还原 D.电池放电时,氢气是负极
7.下列事实不能用电化学理论解释的是( )
A、轮船水线以下的船壳上镶嵌有一定量的锌块 B、镀锌的铁制品比镀锡的铁制品耐用
C、铝片不用特殊方法保存 D、锌跟稀硫酸反应时,滴入少量硫酸铜溶液后,反应速率加快
6.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极:Pb + SO42- → PbSO4 + 2e 正极:PbO2 + 4H+ + SO42- + 2e → PbSO4 + 2H2O若为电解池提供0.1mol电子,这时电池内消耗的H2SO4的物质的量至少是( )
A、0.025mol B、0.050mol C、0.10mol D、0.20mol
4. 如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是 ( )
A.④>②>①>③
B.②>①>③>④ C.④>②>③>①
D.③>②>④>① 

3. 下列反应过程中,同时有离子键、极性键和非极性键的断裂和形成的反应是 ( )
A、NH4Cl NH3↑+HCl↑
B、NH3+CO2+H2O=NH4HCO3
NH3↑+HCl↑
B、NH3+CO2+H2O=NH4HCO3
C、2NaOH+Cl2=NaCl+NaClO+H2O D、2Na2O2+2CO2=2Na2CO3+O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com