
题目列表(包括答案和解析)
24.已知:SO2+2H2S=3S+2H2O,其中氧化产物和还原产物的质量比为2:1。25℃时,向体积为 V L的真空容器内通人 n mol SO2和 m mol H2S。
(1)若n=2,则当m = 时,反应后容器内气体的密度最小。
(2)若2n>m时,则反应后氧化产物和还原产物的质量差为 g。
(3)若 5n=m,且反应后氧化产物和还原产物的质量和为48g时,则 n+ m= 。
23.取一定量的Na2SO4和Na2CO3的混合物溶于水后配成1L溶液,取出100mL,加入足量的氯化钡溶液,滤出沉淀,加入足量的盐酸,沉淀部分溶解且放出标况下的气体1.12L;将剩余沉淀滤出,洗涤,干燥,得沉淀 2.33g,求原溶液中钠离子的物质的量浓度。
22. ( 6 分)浓硫酸与铜的反应用了下图所示的装置,请回答下列问题。

( l )若试管乙中装的是石蕊试液,则反应过程中观察到乙中的现象是 ; 若试管乙中装的是品红溶液,则反应过程中观察到乙中的现象是 。
( 2 )反应结束后在试管甲的底部常可见到一些白色固体,该固体可能是 (填化学式)。待试管甲内液体冷却后,将试管中的液体慢慢倒人另一支盛有少量水的试管中,观察溶液的颜色。这一步操作的目的是要证实 。
( 3 )写出上述试管甲中发生反应的化学方程式
若收集到标准状况下气体 0.56L ,则反应中转移电子的物质的量为
21.(11分)实验室有一瓶长久放置的亚硫酸钠,为了检验此瓶亚硫酸钠是否部分被氧化及测定亚硫酸钠的质量分数,有学生设计了下面实验,根据实验步骤填写下列空格。
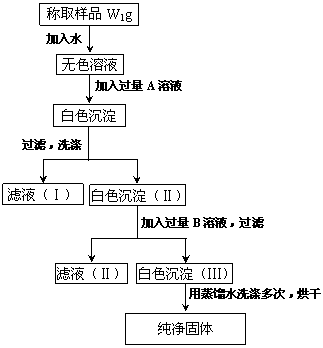
(l)加入的A是 ,应该加入过量的A的理由是
;检验A是否过量的方法是
加入A发生反应的离子方程式是 。
(2)加入的 B是 ,应稍过量的理由是 ;加入B发生反应的离子方程式是 。
(3)为了检验沉淀(Ⅲ)是否洗净,在最后几滴洗涤液中加人 ,
若 ;表示沉淀已经洗净。
(4)含亚硫酸钠的质量分数计算式为 。
(5)当W1与W2的关系式为 时,表明亚硫酸钠已被全部氧化。
20、(7分)、甲、乙、丙是由短周期元素形成的常见单质,丙在常温下为无色气体,且乙、丙两元素同主族,其余为常见化合物,它们在一定条件下有如下转化关系:(反应中生成的水已略去)
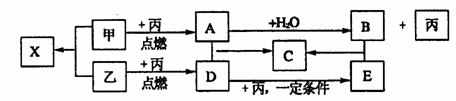
(1)、甲、乙、丙三种单质的名称分别为,甲 乙 丙
(2)、写出下列反应的化学方程式,D+丙→E
A + D → C 。
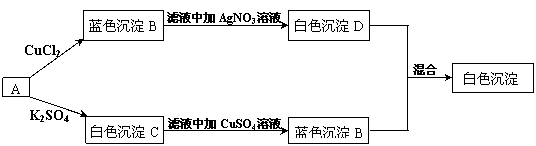
19.(8分)有一学生取两份A溶液做实验,实验步骤和实验现象如下所示(C不考虑是微溶物)。
|
|
(1)写出化学式:A. 、B. 、C. 、D. 。
(2)写出下列反应的离子方程式。
 A B
A B
 A C
A C
18.(4分)用浓硫酸吸收三氧化硫可得到发烟硫酸(H2SO4·SO3),某化工厂用1.5t质量分数为 98%的浓硫酸吸收三氧化硫制成发烟硫酸,再与水混合可得密度为1.84g/cm3、质量分数为98 %的H2SO4 t。
17. (4分)有 K2SO4、H2SO4、NaOH三瓶未贴标签的溶液,如何只用酚酚一种试剂加以鉴别?
16.(3分)用铁槽车盛装浓硫酸,是利用浓硫酸的 性;将含水蒸气的氯气通过盛浓硫酸的洗气瓶,是利用浓硫酸的 性;除掉铁皮表面的铁锈,是利用浓硫酸的
性。
15.设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A. NA个CO分子和NA个N2分子的质量相等 B. 18gD2O含有的电子数为10NA
C. 25℃、1.01×105Pa时,NA个氢分子的体积约是22.4L
D. 同温、同压下,相同体积的氟气和氩气所含的原子数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com