
题目列表(包括答案和解析)
3.取标准状况下CH4 和过量O2的混合气体840mL,点燃,将Q燃烧后的气体用过量碱石灰吸收,碱石灰增重0.600g。计算:
(1)碱石灰吸收后所剩气体的体积(标准状况下)。
(2)原混合气体中CH4 和O2 的体积比。
答案:(1)336mL (2)1∶4
2.在一定条件下PbO2与Cr3+反应,产物是Cr2O72-和pb2+,则与1mol Cr3+反应所需PbO2的物质的量为……………………………………………………………………( B )
A.3.0mol B.1.5mol C.1.0mol D.0.75mol
1.用足量的CO还原32.0g某种氧化物,将所生成的气体通入足量澄清石灰水中,得到的沉淀为60g,则该氧化物是………………………………………………………( B )
A.FeO B.Fe2O3 C.CuO D.Cu2O
5.把100g铁片插入500mL 2 mol·L-1的CuSO4溶液中,反应一段时间后,取出铁片,洗净、干燥、称量,铁片的质量为104g。计算:
(1)析出铜多少克?
(2)混合液中FeSO4 的物质的量浓度是多少?
解析:CuSO4 + Fe= Cu + FeSO4 △m增
64g 1mol 8g
m(Cu) n(FeSO4 ) 104g - 100g
得m(Cu)=32g
n(FeSO4 ) = 0.5mol
所以c(FeSO4)
= 
答案:(1)32g (2)1 mol·L-1
高考真题
7.8g, n(NaOH)
得n(NaOH) = 0.2mol
所以c(NaOH)
= 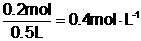
答案:(1)1.12L (2)0.4 mol·L-1’
7.8g V(O2 )
得V(O2 ) = 1.12L
(2) 2 Na2O2 + 2H2O == 4NaOH + O2↑
2×78g 4mol
4.7.8g Na2O2 投入水中,充分反应后,计算:
(1)在标准状况下放出O2的体积是多少升?
(2)把反应的溶液加水稀释至500Ml,NaOH的物质的量浓度是多少?
解析:(1) 2 Na2O2 + 2H2O == 4NaOH + O2↑
2×78g 22.4L
3.某温度下,将Cl2通入NaOH溶液中,反应得到NaCI、NaCIO、NaClO3 的混合液,经测定CIO-与CIO3-的浓度之比为1∶3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为…………………………………………………( D )
A.21∶5 B.11∶3 C.3∶1 D.4∶1
2.有一未知浓度的盐酸25mL,在加入0.5 mol·L-1的AgNO3 溶液25mL后,改加NaOH溶液,结果用去1.0 mol·L-1NaOH溶液25mL恰好完全中和,则盐酸的物质的量浓度为………………………………………………………………………………( B )
A.0 .5 mol·L-1 B.1.0 mol·L-1 C.1.5 mol·L-1 D.2.0 mol·L-1
1.将NaCI和NaBr的混合物m g溶于足量的水配成500mL溶液A,再向其中通入足量的Cl2,充分反应后蒸干得干燥晶体(m - 2) g,则A溶液中的Na+、Br-、CI-的物质的量之比不可能是…………………………………………………………………( D )
A.3∶2∶1 B.3∶1∶2 C.4∶3∶1 D.3∶1∶4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com