
题目列表(包括答案和解析)
43.在氢气还原氧化铜的实验中
A.氧化铜发生还原反应 B.氢气发生还原反应
C.铜发生还原反应 D.水发生还原反应
42.下列变化属于还原反应的是
A.CO2在高压、低温下变成雪状固体 B.CO2通人澄清的石灰水,石灰水变浑浊
C.CO2通人紫色石蕊试夜,试液变红色 D.CO2通过赤热的炭变成CO
41.氧化还原反应的实质是
A.氧元素的得与失 B.化合价的升降
C.电子的得失或偏移 D.分子中原子重新组合
40.下列各组变化中,后者一定包括前者的是
A.物理变化、化学变化 B.氧化还原反应、分解分应
C.氧化还原反应、化合反应 D.中和反应、复分解反应
35.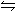 可逆反应:2NO2 2NO+O2在定容密闭容器中反应,达到平衡状态的标志是( )
可逆反应:2NO2 2NO+O2在定容密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2 n molNO2
②单位时间内生成n molO2的同时生成2 nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
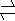 A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
*36.将2molSO2, 1molO2充入带活塞的密闭容器中,发生反应2SO2(g)+ O2(g) 2 SO3(g),达到平衡后,改变下列条件,SO3的平衡浓度不改变的是( )
A.保持温度和容器的压强不变,充入1mol SO3(g)
B.保持温度和容器的容积不变,充入1mol SO2(g)
C.保持温度和容器的压强不变,充入1mol O2(g)
D.保持温度和容器的压强不变,充入1mol Ar(g)
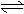 *37.在体积、温度都相同的条件下有如下反应:2A(气)+2B(气) C(气)+3D(气)。现分别从两条途径建立平衡:(Ⅰ)A、B的起始物质的量均为2mol;(Ⅱ)C、D的起始物质的量分别为2mol和6mol。以下叙述正确的是(
)
*37.在体积、温度都相同的条件下有如下反应:2A(气)+2B(气) C(气)+3D(气)。现分别从两条途径建立平衡:(Ⅰ)A、B的起始物质的量均为2mol;(Ⅱ)C、D的起始物质的量分别为2mol和6mol。以下叙述正确的是(
)
A.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同
B.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同
C.达到平衡时,Ⅰ途径的反应速率VA等于Ⅱ途径的反应速率VD
D.达到平衡时,Ⅰ途径所得混合气体的密度为Ⅱ途径所得混合气体密度的1/2
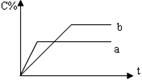
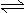 *38.右图表示可逆反应A(g)+B(g) nC(g) ΔH<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线,有关叙述一定正确的是( )
*38.右图表示可逆反应A(g)+B(g) nC(g) ΔH<0,在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线,有关叙述一定正确的是( )
A.a表示有催化剂,而b无催化剂
B.若其他条件相同,a比b的温度高
C.若其他条件相同,a比b的压强大,n>2
D.反应由逆反应方向开始
*39.在一恒定的容器中充入2 mol A和1 mol B发生反应:
 2A(g)+B(g) x C(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6 mol、B:0.3 mol、C:1.4 mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为(
)
2A(g)+B(g) x C(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6 mol、B:0.3 mol、C:1.4 mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为(
)
A.只能为2 B.只能为3
C.可能是2,也可能是3 D.无法确定
34. 反应N2(g)+3H2(g) 2NH3(g)在密闭容器中进行,分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率V(N2)、V(H2)、V(NH3),则三者之间的关系正确的是( )
反应N2(g)+3H2(g) 2NH3(g)在密闭容器中进行,分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率V(N2)、V(H2)、V(NH3),则三者之间的关系正确的是( )
A.V(N2)=V(NH3) B.3V(H2)=2V(NH3) C.V(NH3)=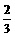 V(H2) D.V(H2)=3V(N2)
V(H2) D.V(H2)=3V(N2)
32.某FeCl2 溶液中混有FeI2 杂质,根据已知反应:①2FeCl3+2KI=2FeCl2+2KCl+I2↓;②2FeCl2+Cl2=2FeCl3;③F2+2KI(固)=2KF+I2中的有关事实,要除去其中的FeI2,应选用的试剂是( )
A.F2 B.过量Cl2 C.FeCl3 D.FeCl2
*33.羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00ml 0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65ml 0.020mol/L的KMnO4酸性溶液完全作用(已知:FeSO4+ KMnO4+ H2SO4 → Fe2(SO4)3 + K2SO4+ MnSO4+ H2O(未配平)),则在上述反应中,羟胺的氧化产物是( )
A.N2 B.N2O C.NO D.NO2
31.向某溶液A中逐滴加入或通入B物质至过量, 反应过程中加入或通入B的量(用横坐标表示)与生成沉淀的量(用纵坐标表示)的关系如图所示, 则符合图象的物质A与B为
|
|
A |
B |
C |
D |
|
溶液A |
澄清石灰水 |
AlCl3溶液 |
H2S |
Na2SiO3 |
|
过量B |
CO2 |
KOH |
SO2 |
H2SO4 |
30.已知 I-、Fe2+、SO 2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序Cl-< Fe 2+< H2O 2 < I-< SO 2,则下列反应不能发生的是( )
A.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ B.I2+SO2+2H2O=H2SO4+2HI
C.H2O2+H2SO4=SO2+O2+2H2O D.2Fe2++I2=2Fe3++2I-
29.常温下,在溶液中可以发生反应:X+2Y3+=2Y2++X2+,则下列叙述①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性比X2+的氧化性强。以下叙述中正确的是( )
A.②④⑥ B.①③④ C.①③⑤⑥ D.②⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com