
题目列表(包括答案和解析)
22.(6分)一固体混和物,可能有氯化钙、碳酸铵、烧碱、硫酸铵,将它溶解于水得到无色澄清溶液,无其它明显现象,向溶液中加入硝酸钡溶液,产生白色沉淀,再加入硝酸,沉淀部分消失,原混和物中肯定有 ,肯定没有 。
21.(5分)纳米材料的特殊性质的原因之一是由于它具有很大的比表面积(S/V)即相同体积的纳米材料比一般材料的表面积大很多。假定某种原子直径为0.2nm,则可推算在边长1nm的小立方体中,共有 个原子,其表面有 个原子,内部有______个原子。由于处于表面的原子数目较多,其化学性质应 (填“很活泼”或“较活泼”或“不活泼”)。利用某些纳米材料与特殊气体的反应可以制造气敏元件,用以测定在某些环境中指定气体的含量,这种气敏元件是利用了纳米材料具有的 作用。
20.下列离子方程式书写错误的是
A 氨气通入醋酸溶液:CH3COOH+NH3=CH3COONH4
B 氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
C 过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2
D 澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-=CaCO3↓+H2O
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
19.有一金属钠和过氧化钠的混和物,与过量水充分反应后,产生2.24L气体(标准状况),用电火花点燃后,恢复到标准状况,体积减少了1.12L,则原混和物中钠与过氧化钠的物质的量之比为
A 1︰3 B 5︰1 C 1︰1 D 1︰2
18.在周期表主族元素中,甲元素与乙、丙、丁三元素紧密相邻。甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断中正确的是
A 原子半径:丙>乙>甲>丁 B 乙和甲或乙和丁所能形成的化合物都是大气污染物
C 气态氢化物的稳定性:甲>丙 D 最高价氧化物对应水化物的酸性:丁>甲
17.1999年曾报道合成和分离了含高能量的正离子N5+化合物N5AsF6,下列叙述错误的是
A N5+共有34个核外电子 B N5+中氮-氮原子间以共用电子对结合
C 化合物N5AsF6中As化合价为+1 D 化合物N5AsF6中F化合价为-1
16.氡(Rn)是放射性元素,某些建筑材料中若含有氡,将对人体健康造成危害。222Rn来自镭而称之为镭射气,220Rn来自钍而称之为钍射气,219Rn来自锕而称之为锕射气。下列有关氡的说法正确的是
A 氡气是双原子分子 B 氡元素有222Rn、220Rn、219Rn三种同素异形体
C 氡气因其化学性质活泼而对人体有害 D 氡的原子核外有6个电子层,最外层有8个电子
15.如果假设12C的相对原子质量为24,且以0.024kg 12C所含有的原子数为阿伏伽德罗常数,则下列数值中肯定不会因此而改变的是
A 标准状况下氧气的密度 B 气体摩尔体积
C 一个Cl原子的质量 D 一定质量硫酸中氧原子的物质的量
14.某溶液中含有HCO3-、SO32-、CO32-、CH3COO-等4种阴离子。向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A CH3COO- B SO32- C CO32- D HCO3-
13.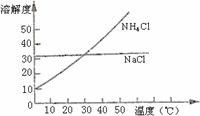 把NH4Cl从几乎饱和NaHCO3溶液中分离出来是联合制碱法中的关键。为此,应向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不含NaHCO3的NH4Cl。NH4Cl和NaCl共同存在时的溶解度曲线如右图所示,下列操作正确的是
把NH4Cl从几乎饱和NaHCO3溶液中分离出来是联合制碱法中的关键。为此,应向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不含NaHCO3的NH4Cl。NH4Cl和NaCl共同存在时的溶解度曲线如右图所示,下列操作正确的是
|
组别 |
通入气体 |
控制温度 |
|
A |
CO2 |
30℃-40℃ |
|
B |
CO2 |
0℃-10℃ |
|
C |
NH3 |
30℃-40℃ |
|
D |
NH3 |
0℃-10℃ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com