
题目列表(包括答案和解析)
5.下列气体不能用H2SO4干燥的是
A.CO2 B.NH3 C.SO2 D.HC1
4.漂白粉的有效成分是
A.次氯酸钙 B.氯化钙 C.次氯酸 D.次氯酸钙与氯化钙
3.新制氯水与久置的氯水相比较,下列结论不正确的是
A.颜色相同 B.前者能使有色布条褪色
C.都含有H+ D.加AgNO3溶液都能生成白色沉淀
2.将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
A.稀硝酸 B.稀盐酸 C.浓硝酸 D.氢氧化钠
1.下表是某城市空气质量每周公报的部分内容。对表中三个空气质量指标不会产生影响的是
|
项目 |
空气污染指数(API) |
空气质量级别 |
空气质量描述 |
|
总悬浮颗粒 |
52 |
Ⅱ |
良 |
|
二氧化硫 |
7 |
I |
优 |
|
二氧化氮 |
24 |
I |
优 |
A.焚烧垃圾 B.使用含磷洗衣粉
C.汽车排放的尾气 D.用煤和石油产品作燃料
26. (13分)化学定量分析常涉及溶液的配制和溶液浓度的计算。例如,通过溶液中的反应测定物质的组成时,首先需配制一定物质的量浓度的标准溶液,再将标准溶液与待分析物质进行反应或进行比较,最后通过对实验数据的处理,确定物质的组成。
某甲、乙、丙三个化学学习小组为探究碳酸钠溶液和盐酸的反应并测定盐酸的浓度,做了以下实验:
(1)甲组的同学打算配制标准碳酸钠溶液,用所配制的标准溶液与盐酸反应来进行测定盐酸的浓度,该小组在配制标准溶液的过程中应该用到的玻璃仪器有
。
(2)乙组同学准确量取一定体积的盐酸,然后将甲组配制的、一定体积的标准溶液逐滴滴入盐酸中,产生的现象是 。
(3)丙组同学准确量取一定体积的标准碳酸钠溶液,然后慢慢向碳酸钠溶液中滴入过量的盐酸,边滴边及时混合均匀,产生的现象是 。
(4)假设乙、丙两组的同学的操作都准确无误,并都使用合适的指示剂使反应恰好完全进行,他们所测得的盐酸的浓度 (填“相同”或“不相同”)。
如果甲组同学称取的碳酸钠中含有少量水分,最后配制的标准溶液的浓度将 (填“偏高”或“偏低”),而乙、丙两组的同学的操作都准确无误,他们按上述方法测定得到的盐酸的浓度 (填“相同”或“不相同”)。
(5)如果乙、丙两组同学所量取的碳酸钠溶液和盐酸的体积分别相等,请你写出它们在实验过程中得到的二氧化碳气体的体积关系(相同状况下):
。
徐州市2005--2006学年度年第一学期期末考试
25. (4分)氯气通入石灰乳制得漂白粉,其主要成分是Ca(OH)2·3CaCl(ClO)·nH2O[其相对分子质量为(455+18n)],一定质量的漂白粉和一定浓度的盐酸完全反应,生成氯气的质量与参加的漂白粉质量之比可标志“有效氯”的多少。如果某漂白粉的“有效氯”的质量分数为35%,且该漂白粉的组成和上述化学式相符时,请计算出化学式中的n值。
(已知反应:CaCl(ClO)+2HCl=CaCl2+Cl2↑+H2O)
24. (3分)某小型钢铁厂以含Fe2O3 65%的赤铁矿(杂质中不含铁元素)为原料炼铁。若在生产过程中氧化铁损失5.0%,则用1000 t这样的铁矿石能生产多少吨含碳2.0%的生铁?(计算结果保留一位小数)
23. (11分)为了探究铁与氯气的反应,某同学甲设计了如下的实验方案。
其实验装置为:
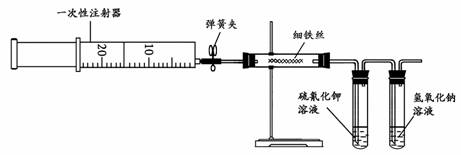
其实验步骤为:
(1)用注射器吸取20 mL左右的氯气。
(2)在硬质玻璃管内加入一定量的细铁丝,一支试管内加入硫氰化钾溶液,另一支试管中加入氢氧化钠溶液。按图所示连接实验装置,并固定在铁架台上。经检验装置不漏气。
(3)加热硬质玻璃管内铁丝约1 min,然后把注射器中的氯气注入到硬质玻璃管内,观察实验现象。可观察到的主要现象是 ,
。
(4)请写出试管中所发生反应的离子方程式:
。其中,氢氧化钠溶液的作用是 。
(5)某同学乙猜测铁与氯气反应可能还会生成氯化亚铁,其为了探究生成物中是否含有氯化亚铁(假设铁已完全反应),设计了实验步骤如下的实验方案,但其只写出了实验的第1步。现只有H2O2溶液、酸性KMnO4溶液和KSCN溶液,而没有其他试剂,请你利用这三种试剂中的合适试剂和中学化学实验常用仪器,补充同学乙的实验步骤、完善其实验方案:
第1步:取出甲实验后的玻璃管中的固体少量,放入小烧杯中加适量蒸馏水,搅拌、溶解。
。
22.(8分)在进行某实验探究过程中,一些学生发现等质量的铜片分别与等体积(均过量)的浓硝酸和稀硝酸反应,所得溶液前者为绿色,后者为蓝色。
针对这种现象,学生们进行了讨论后,出现了以下两种观点:
一种认为,这可能是Cu2+浓度的差异引起的。你同意这种看法吗? (填“同意”或“不同意”),原因是 。
另一种认为,呈“绿色”是Cu2+与NO2混合的结果。请你设计出一个实验方案证明之,你设计的实验方案是
。
请写出铜与稀硝酸反应的离子方程式,并标出电子转移的方向和数目:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com