

题目列表(包括答案和解析)
6、( )下列关于氯水的叙述,正确的是
A、新制的氯水中只含Cl2和H2O
B、新制的氯水可使兰色的石蕊试纸先变红后褪色
C、光照氯水有气泡逸出,该气体是Cl2
D、氯水放置数天后酸性将增强
5、( )设NA表示阿伏加德罗常数,下列说法正确的是:
A、标准状况下,5.6 L氧气含有n个O2,则NA为4n
B、常温常压下,1 mol氦气含有的原子数为2NA
C、常温下,1 mol氯气与足量的烧碱反应,转移的电子数为2 NA
D、18 g水中所含的电子数为8 NA
4、( )下列气体中,不能用浓硫酸干燥的是:(1)O2(2)CO2(3)Cl2(4)NH3
A、只有(4) B、(1)和(4) C、(3)和(4) D、(1)(2)(4)
3、( )下列物质在空气中久置变质,并且在变质过程中,既有氧化还原反应发生,又
有非氧化还原反应发生的是:
A、苛性钠溶液 B、漂白粉 C、碳酸钠 D、稀硫酸
2、( )不能通过单质直接化合得到的是:
A、FeCl3 B、Na2S C、FeCl2 D、NaCl
1、( )下列物质为纯净物的是:
A、液氯 B、纯净的盐酸 C、浓硫酸 D、漂白粉
28.取6.60克NaHCO3和Na2O2的固体混合物,在密闭容器中加热到250℃经充分反应排出气体,冷却后称得固体质量为5.30克,计算原混合物中Na2O2的质量分数。
27. Na2CO3和NaHCO3混合物9.5g加入稀盐酸,到不再产生气体为止,恰好用去50克稀盐酸,将生成的气体通入过量的石灰水中,得到沉淀10g,求①混合物中Na2CO3与NaHCO3各多少克?②所用稀盐酸的溶质质量分数。③所得溶液溶质质量分数。
25.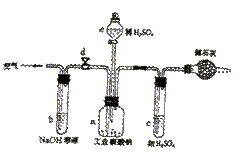 工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如下图的装置:
工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如下图的装置:
操作程序是:1.准确称取盛有碱石灰的干燥管的质量(m1g),再准确称取一定质量纯碱mg并全部放入a中;2.组装全部反应装置并检查气密性,关闭d;由e逐滴加入稀硫酸至不再产生气泡为止;3.打开d,慢慢鼓入空气10min;4.再称干燥管的总质量为m2g。
①必须鼓入空气的理由是______________________________。
②不设置装置C将使测定结果______(填偏大、偏小或不变),原因是____________________________。
③不设置b 将使测定结果______(填偏大、偏小或不变),原因是_____________________________。
④Na2CO3质量分数的计算式为__________________________。
24.按要求写出下列反应的方程式,是氧化还原反应的,标出电子转移的方向和数目。
①Na与FeCl3溶液反应:(写化学方程式)
②Na2O2与CO2反应(写化学方程式)
③Ba(OH)2溶液与CuSO4溶液(写离子方程式)
④Ca(HCO3)2溶液与NaOH溶液(适量和过量)(写离子方程式)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com