
题目列表(包括答案和解析)
1、在通常状况下,下列气体在水中的溶解度最大的是
A.氯气 B.氯化氢 C.二氧化硫 D.硫化氢
21.(8分)归纳整理是科学学习的重要方法之一。在学习了氧族元素的各种性质后,可归纳整理出如下表所示的表格(部分)。
|
性质/元素 |
8O |
16S |
34Se |
52Te |
|
单质熔点(℃) |
– 218.4 |
113 |
|
452 |
|
单质沸点(℃) |
– 183 |
444.6 |
685 |
1390 |
|
主要化合价 |
– 2 |
– 2、+ 4、+ 6 |
– 2、+ 4、+ 6 |
|
|
原子半径 |
逐渐增大 |
|||
|
单质与H2反应情况 |
点燃时易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
请根据上表回答下列问题:
(1) 硒的熔点范围可能是______________________;
(2) 碲的化合价可能有__________________;
(3) 硫、硒、碲的氢化物的稳定性由强至弱的顺序是_______________(填化学式)。
(4) 氢硒酸有较强的还原性,因此放在空气中长期保存易变质,其可能发生反应的化学方程式为________________________ 。
20.(4分)下列分子结构图中的大黑点表示原子序数小于10的元素的“原子实”(指原子除去最外层电子的剩余部分),小黑点表示没形成共价键的最外层电子,短线表示共价键。 示例如下:(4分)
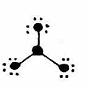

代表的分子是 。
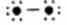 代表的分子是 。(写化学式)
代表的分子是 。(写化学式)
19.(6分)在原子序数为 1 - 18 号的元素中, 用适当的化学符号填写下列空白(稀有气体除外):
(1)原子半径最大的是 _______ , 简单离子中, 离子半径最大的是 _____
(2)气态氢化物最稳定的是 ___ , 气态氢化物中含有H 元素质量分数最大的氢化物是___
(3)酸性最强的含氧酸是 _________,属于两性氢氧化物的物质是___________.
18.(10分)实验室合成SO3的装置如下图所示;试回答:
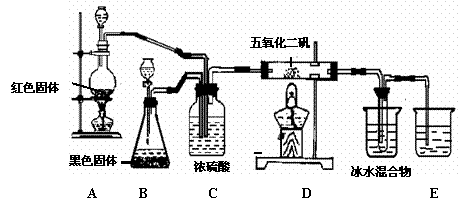
(1)装置B中的黑色固体是 ;
(2)装置C的作用: ① ;② ;
(3)D处反应的化学方程式 ;
(4)E中冰水混合物的作用是
17.已知由NaHS、MgSO4、NaHSO4组成的混合物,硫元素的质量分数为a%,则混合物中氧元素的质量分数为
A.a% B.2a% C.1-1.75a% D.1-0.75a%
第Ⅱ卷 (非选择题 共49分)
16.以NA表示阿伏加德罗常数,下列说法正确的是:
A.常温常压下,11.2L氧气所含的原子数为NA
B.2.3g金属钠变为钠离子时失去的电子数为0.1NA
C.1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA
D.标准状况下,22.4L水所含分子数为NA
15. 向50mL18mol/LH2SO4溶液中加入足量的铜粉并加热,充分反应后被还原的硫酸的我物质的量:
A、小于0.45mol B、等于0.45mol
C、在0.45mol和0.90mol之间 C、大于0.90mol
14.下列实验方案能达到预定目的的是
A、将SO2通入石蕊溶液中证明SO2有漂白性
B、用绿豆大小的钠和钾分别与冷水反应说明钠、钾金属性的强弱
C、向某未知溶液中加入BaCl2溶液后再加入稀硝酸,检验是否含SO42-
D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
13.根据元素在周期表中的位置判断,下列说法正确的是
A. 在元素周期表中金属和非金属的交界处可以找到半导体材料
B. Be(OH)2(氢氧化铍)易溶于水
C.Tl(OH)3(氢氧化铊)一定是两性氢氧化物
D.RaCO3(碳酸镭)是易溶于水的盐
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com