
题目列表(包括答案和解析)
32、用含FeS275%的硫铁矿制取硫酸,若反应过程中损失5%的硫,求制取1000kg98%的浓硫酸需这种硫铁矿多少kg。(要求写出所有反应的化学方程式)
[答案]
31、下图是实验室中某学生设计用来制取干燥纯净氯气的装置,由于有错误而不能在D集气瓶中收集到氯气。请指出装置中的错误,加以改正,并回答下列问题:(A中试剂为二氧化锰和稀盐酸,B中为食盐饱和溶液,C中为浓硫酸)
(1)装置中的错误并改正:

‚
ƒ
„
…
(2)写出A中反应的化学方程式 ,此反应中氧化剂是 ,被氧化的元素是 ;
(3)B瓶中盛饱和食盐水的目的是 ;
(4)C瓶中盛浓硫酸的作用是 ,利用浓硫酸的 性。
(5)若在D瓶中放有湿润的淀粉KI试纸,现象是 ,反应方程式为
。
30、将Na2S、Na2SO3、Na2SO4按一定比例混合配成溶液,做如下实验:
(1)混合溶液与过量的某无氧酸甲反应,得浅黄色沉淀A和无色溶液B;
(2)无色溶液B与某硝酸盐溶液乙反应,得白色沉淀C和溶液D;
(3)在溶液D中加入某硝酸盐溶液丙,得黄色沉淀E,再加入少量稀硝酸,E不溶解。
写出下列物质的化学式:甲: 乙: A: C: E:
写出以上三步实验中反应的离子方程式:
(1) (2) (3)
29、写出或配平下列化学方程式:
(1)铜片浓硫酸共热
(2) K2Cr2O7 + HCl = + KCl + CrCl3 + Cl2+ H2O
28、某溶液中含有Na2SO4、Na2CO3、NaOH、NaCl四种溶质,如果只允许取一次该溶液,分别将这四种物质电离出的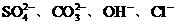 检验出来(允许使用必要的实验操作如过滤),那么应:
检验出来(允许使用必要的实验操作如过滤),那么应:
(1)先检验 ,加入试剂为
(2)然后检验 ,加入试剂为
(3)再检验 ,加入试剂为
(4)最后检验 ,加入试剂为
27、实验室中常用36.5%的浓盐酸,密度为1.2g/cm3,其物质的量浓度为 mol/L,现要配制3mol/L的稀盐酸100mL,需这种浓盐酸 mL。从所配好的稀盐酸100mL中取出15mL,加入2mol/L的NaOH溶液 mL,才能恰好中和。
26、有一瓶无色气体,可能含有CO2、H2S、HCl、SO2和HBr中的一种或几种,现实验如下:
(1)加入适量氯水,振荡、静置得无色透明溶液,然后分为两份;
(2)向一份中加入用盐酸酸化的BaCl2溶液,出现白色沉淀物,另一份中加入硝酸酸化的硝酸银溶液,也产生白色沉淀物。由此可得出正确的推论是
A.可能含有HBr和CO2 B.一定有HCl和SO2
C.一定无H2S和CO2 D.一定无HBr和H2S
24、在质量为Gg的坩埚中,放入BaCl2·nH2O晶体后称重为W1g。加热使结晶水全部失去,冷却后,称得剩余物与坩埚的质量为W2g。则n值为
A.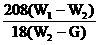 B.
B.  C.
C.  D.
D. 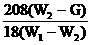
25、在反应 中,当有11mol电子转移时,反应前后固体物质减少的质量为
中,当有11mol电子转移时,反应前后固体物质减少的质量为
A.160g B.80g C.128g D.40g
23、VL硫酸铁溶液中含Fe3+ag,则溶液中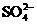 物质的量浓度为
物质的量浓度为
A. B.
B. 
C. 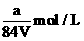 D.
D. 
22、既能使品红溶液褪色,又能使溴水褪色的是
A.SO2 B.H2S C.Cl2 D.HI
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com