
题目列表(包括答案和解析)
6. X、Y、Z都是金属,把X投入Z的硝酸盐溶液中,X的表面有Z析出, X 与Y组成原电池时,Y为电池的负极,X、Y、Z三种金属的活泼性顺序为: ( )
A X>Y>Z B X>Z>Y C Y>X>Z D Y>Z>X
5.下列叙述中正确的是 ( )
A.金属阳离子被还原一定得到金属的单质
B.在氧化还原反应中,非金属单质一定是氧化剂
C.某元素从化合态变为游离态时,该元素一定被还原
D.含金属元素的离子不一定都是阳离子
4.设NA为阿伏伽德罗常数的值,下列有关说法不正确的是
A.45g水中含有的水分子数是2.5NA
B.标准状况下,33.6LCO中含有的原子数是3NA
C.0.5L0.2mol/L的NaCl (aq)中含有的Na+数是0.1NA
D.1molCH3+(碳正离子)中含电子数目为10NA
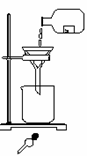
3.某学生发现滴瓶中溶液里有悬浊物,拟用右图所示操作进行过滤,错误的操作有( )
A.4处 B.3处
C.2处 D.1处
2. 在m A + n B 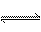 p C的反应中,m、n、p为各物质的计量数。现测得C每分钟
p C的反应中,m、n、p为各物质的计量数。现测得C每分钟
增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
A、2:3:2 B、2:3:3 C、1:3:2 D、3:1:2
1.下列说法正确的是
A. 煤的干馏是物理变化
B. 石油裂解的主要目的是制备更多的汽油
C. 石油分馏能得到不同沸点范围的产物, 每一种馏分都是多种烃的混合物
D. 煤中含有苯、甲苯等,可以用干馏后再分馏的方法把它们分离出来
26.(4分)某软锰矿石中MnO2 的质量分数为87%,如果其他成分不与浓盐酸反应,则150 g此矿石与足量浓盐酸反应,制得的氯气在标准状况下的体积是多少?
答案:33.61
25.(4分)将一定体积的密度为1.19 g·cm-3 、HCl的质量分数为36.5%的浓盐酸稀释至100mL时,溶液中的Cl-浓度为1.02 mol·L-1。计算所用浓盐酸的体积。
答案:8.57ml。
24.(6分)某固体混合物可能由KNO3、K2SO4、KI、NaCl、CuCl2、CaCl2和Na2CO3中的一种或几种组成。依次进行下列五步实验,观察到的现象记录如下:
①取一定量混合物加水溶解得无色透明溶液:
②向上述溶液中滴加BaCl2溶液,有白色沉淀生成,将该沉淀滤出,并将滤液分成两份:
③上述白色沉淀可完全溶解于稀盐酸中:
④往一份滤液中滴加氯水后振荡,溶液颜色无明显变化;
⑤往另一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸。
根据以上实验现象,可以判断出混合物中肯定含有 Na2CO3 ;肯定不含有的物质是 CuCl2 、K2SO4 、CaCl2、KI ;不能判断混合物中是否含有的物质是 KNO3 、NaCl
23.(13分)实验室用下列装置先制取干燥、纯净的Cl2,然后进行有关性质实验,试根据下列装置回答问题:
(1)按气体从左到右流向,上述各装置的连接顺序为(以图中字母A-G表示):A→ E→ F → C → D → B → G
(2)A装置的反应中氧化剂是 MnO2 ,还原剂是 浓HCl (均填化学式),制得的Cl2 中所含的杂质气体为 HCl和水蒸气 ;E装置的作用是 除HCl ;D装置中的现象为 布条褪色 ;反应结束后,振荡B装置,静置后出现的现象是下层液为紫红色 。
(3)写出下列装置中反应的离子方程式:
①B装置中: Cl2 + 2I- =I 2 + 2Cl- 。
②G装置中:Cl2 + 2OH-=Cl- + ClO- + H2O 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com