
题目列表(包括答案和解析)
25(6分)、为了比较硫与碳的非金属性的强弱,某同学想通过比较两种元素的最高价氧化物对应的水化物的酸性强弱来验证硫与碳的非金属性的强弱,采用了下图中的甲、乙装置:
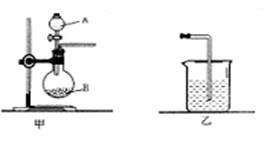
①.仪器A的名称是___________,仪器B中应盛放的药品是________,装置乙中应盛放的药品是___________。
②.B中发生反应的离子方程式为:______________________________;
在装置乙中观察到的现象是:_______________________________。
26.(7分)有同学用铜丝代替铜片改进教科书中浓硫酸与铜反应的实验,以便随时从反应液中抽出铜丝停止反应(如图):
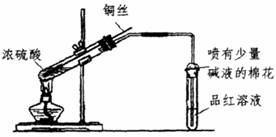
⑴浓硫酸与铜反应的化学方程式为: 。
⑵试管乙中装的是品红溶液,其反应过程中观察到的现象是: ;
若试管乙中装的是石蕊溶液,则反应过程中观察到的现象是: 。
若试管乙中装的是溴水,则反应的离子方程式为: 。
⑶反应结束后在试管甲的底部常可见到-些白色固体,该固体可能是 (填化学式)。
(4)装置中喷有少量碱液的棉花的作用是 。
24.(13分)已知A-F是中学化学中常见物质,其中A、D为气体,且A是一种具有刺激性气味的、易溶于水的无色气体,C、E分别为两种酸,E的浓溶液与F共热通常用于实验室制备D,F是一种黑色粉末。(反应中部分生成物已略去)
另外作图
试回答下列问题:
(1)写出反应③的离子方程式: ;
(2)根据图中信息判断,A、D、F氧化性从强到弱的顺序是
(3)H2O2的电子式为 ;H2O2既具有氧化性又具有还原性,已知H2O2的氧化性介于A和D之间,请写出A、D分别与H2O2溶液反应的化学方程式:
、
(4) C能与水反应生成一种强酸和一种弱酸,此弱酸的酸性比碳酸 (填“强”或“弱”),能证明此结论的化学方程式为 。
23. (11分) A、B、C、D四种短周期元素,原子序数D>C>B>A,且A、B、D同周期,A、D同主族,B的最外层只有1个电子,C的原子结构示意图为: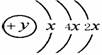 , D在同周期主族元素中原子半径最小,据此填空:
, D在同周期主族元素中原子半径最小,据此填空:
(1)C的元素名称为 ,其气态氢化物的化学式为 ;
A元素在周期表中的位置是 。
(2)A、B、C、D四种元素的原子半径由大到小的顺序为(用化学式填写) ;
比较A-与B+的离子半径(用化学式填写) 。
(3)B和D最高价氧化物的水化物化学式分别为 和 。
(4)A、B、C、D四种元素中某些元素的化合物具有漂白性,试任写出其中两种具有该性质的化合物的化学式 、
(5)写出D的单质与B的最高价氧化物的水化物溶液反应的离子方程式:
22.(8分)根据要求完成下列问题。
⑴写出氯气与消石灰反应制取漂粉精的化学方程式:_ 。
⑵用电子式表示NaCl 的形成过程:_ _ 。
⑶写出炭和浓硫酸在加热条件下反应的化学方程式:_ _。
(4)二氧化硅与炭在高温下反应制硅的化学方程式:_ _。
21.(5分)(1)工业上制造普通玻璃的原料是 、 、
(2)高岭石的组成为Al2(Si2O5)(OH)4,若改用氧化物的形式表示其组成为
20、硒是一种保健元素,含有硒元素的保健品现已进入市场。硒为第4周期第ⅥA族元素,根据它在元素周期表中的位置推测,硒元素不可能具有的性质是B
A.其单质在通常状况下是固体 B、H2Se比HBr稳定
C.硒的最高价氧化物的化学式为SeO3 D、硒元素常见化合价有-2、+4、+6三种
19.下列说法中,不正确的是( A )
A.双原子分子中的共价键,一定是非极性键
B.非极性键也可能存在于离子化合物中
C. HCl溶解于水时化学键没有被破坏
D.共价化合物在液态时不能导电
18.同周期的X、Y、Z三种元素,已知最高价氧化物对应的水化物的酸性强弱顺序是:
HXO 4>H2YO4>H3ZO4,则下列各判断中正确的是 ( B )
A.原子半径:X>Y>Z B.原子序数:X<Y<Z
C.气态氢化物稳定性:X<Y<Z D.元素的非金属性:X>Y>Z
17.A、B、C为短周期中相邻三元素,A、B同周期,B、C同主族,已知此三种元素原子的最外层电子数之和为13,而其质子数之和为27,则此A、B、C三元素为( )
A.P、Si、C B.N、C、Si C.B、C、Si D.Al、Si、C
16.以NA表示阿伏加德罗常数,下列说法中正确的是 ( )
A.标准状况下,11.2 L三氧化硫中含有的分子数为0.5NA
B.2.8g Si完全溶解于足量KOH溶液中失去电子的数为0.2NA
C.1mol氟气与足量H2O反应生成的氧分子数为0.5NA
D.常温、常压下,11.2 L氯气所含原子数为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com