
题目列表(包括答案和解析)
21.已知硫酸溶液的浓度越大,密度也越大,40%的硫酸和50%的硫酸等质量混合后,所得溶液的质量分数 (大于、小于、等于)45%;若等体积混合,所得溶液的质量分数 (大于、小于、等于)45%。
20.已知反应10AgF+5Cl2+5H2O=9AgCl+AgClO3+10HF+O2,则被1mol水还原的Cl2的物质的量是 ( )
A.0.2mol B.0.4mol
C.0.8mol D.1.0mol
19.某学生配制100mL 1mol/L的硫酸溶液,进行下列操作,然后对溶液浓度作精确测定,发现真实浓度小于1mol/L。他的下列操作中使浓度偏低的原因是 ( )
|
A.②③④ B.③④
C.①②③ D.①②③④
18.取相同体积的KI、Na2S、FeBr2溶液,分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温、同压条件下),则KI、Na2S、FeBr2溶液的物质的量浓度之比是(注:Na2S+Cl-NaCl+S↓)
A.1:1:2 B.2:1:3
C.6:3:2 D.3:2:1
16.被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑
下列说法中正确的是(NaBH4中H元素为-1价) ( )
A.NaBH4既是氧化剂又是还原剂
B.NaBH4是还原剂,H2O是氧化剂
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素质量比为2:1
|
A.2NaSCN+MnO2+2H2SO4(浓) Na2SO4+(SCN)2↑+MnSO4+2H2O
B.(CN)2+2KI=2KCN+I2
|
D.2AgCN 2Ag+(CN)2
15.碱金属元素随核电荷数的增加,下列变化中与卤素变化一般趋势不一致的是 ( )
A.单质的熔、沸点 B.单质的密度
C.原子的电子层数 D.原子半径
14.将过量Cl2通入到250mLNaI溶液中,充分反应后,用小火把溶液蒸干,冷却后得到固体12g,其中25%的碘,则原NaI溶液的物质的量浓度是 ( )
A.0.62mol/L B.0.09mol/L
C.0.047mol/L D.0.1mol/L
12.在Vml硫酸铁的溶液中,含Fe3+的质量为Ag,取0.5Vml溶液加水稀释到2Vml,溶液中SO42-物质的量浓度为 ( )
A.3A/112V mOL/l B.375A/14V mol/L
C.375A/56V mol/L D.75A/56V mol/L
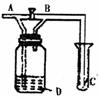 13.如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,当打开B阀后,C处红布条逐渐褪色,则D中装的是 ( )
13.如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,当打开B阀后,C处红布条逐渐褪色,则D中装的是 ( )
A.浓H2SO4
B.CaCl2溶液
C.H2O
D.饱和NaCl溶液
11.某金属氧化物的相对分子质量为A,相同价态金属硫酸盐的相对分子质量为B,则该金属化合价应表示为 ( )
A.(A-B)/20 B.(B-A)/20
C.(B-A)/30 D.(B-A)/80
10.某种混合气体,可能含有N2、HCl、CO,把混合气体依次通过足量的 NaHCO3溶液和灼热的CuO,气体体积都没有变化,在通过足量的Na2O2固体,气体体积减小。最后通过灼热的铜网,经充分反应后气体体积又减少,但还有剩余气体,以下对混合气体组分的判断正确的是 ( )
A.一定没有N2;CO和HCl中至少有一种
B.一定有N2、HCl和CO
C.一定有N2;CO和HCl中至少有一种
D.一定有N2和HCl没有CO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com