
题目列表(包括答案和解析)
4.已知A元素的原子序数为W,B元素的阳离子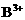 和A元素的阴离子
和A元素的阴离子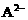 具有相同的电子层结构,则B原子的核外电子数为
( )
具有相同的电子层结构,则B原子的核外电子数为
( )
A.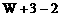 B.
B.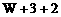 C.
C.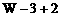 D.
D.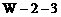
3.将SO2通入BaCl2溶液中至饱和,未见沉淀,继续通入另一种气体至过量仍无沉淀,则通入的气体可能是 ( )
A.CO2 B.NH3 C.H2S D.SO3
2.由下列实验事实得出结论正确的是 ( )
A.蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性
B.室温下,浓硫酸可以用铝槽车装运,说明室温下浓硫酸与铝不反应
C.SO2既可以与NaOH反应又可以与HNO3反应,说明SO2是两性氧化物
D.Na2SO4中硫元素处于最高价,说明Na2SO4溶液具有强氧化性
1. 1998年5月20日,中央电视台第一套节目《新闻联播》播放了一则新闻:近年来我国重点保护文物“云岗石窟”严重腐蚀风化,急剧损坏。其主要原因是在它的旁边新修了一条高速公路。我国不惜花费二亿元资金另修一条路,让公路绕道而行来保护这一珍贵的文物。通过这则新闻你认为造成腐蚀损坏的主要原因是 ( )
A.车辆排放大量尾气 B.居民燃 C.车辆尘埃 D.风吹日晒
23.臭氧(O3)能与KI溶液反应生成氧气等.向反应后的溶液中滴入酚酞,溶液变为红色,若滴入淀粉,溶液则变为蓝色.为测定环境中空气的臭氧含量,将0℃、1.01×105Pa的空气33.6m3通过KI溶液,使反应完全,在所得溶液中用0.100mol·L-1的Na2SO3溶液60.0mL恰好滴定达终点,反应为:2 Na2SO3+I2=Na2S4O6+2NaI
(1)臭氧通入KI溶液中的化学反应方程式是________________________________.
(2)计算大气中臭氧的体积分数.
信阳市十一高2005-2006学年下期期中考试高一化学试题
22.某元素A,它的最高价氧化物的化学式是A2O5,气态氢化物中氢的质量分数为8.82﹪,且A原子中质子数比中子数少1,A是________元素,它在元素周期表位于第______周期第______族.
21.(10分)分别处于第三和第四两个周期的主族元素A和B,它们形成的离子相差两个电子层,已知A元素位于周期表中的m主族:B元素位于周期表中的n主族,B单质的分子中含有共价键。试回答:
(1)A原子的核外电子数可用关系式(含m的式子)___________表示,它的离子符号为__________。
(2)B原子的质子数可用关系式(含n的式子)___________表示,它的离子的符号为__________。
(3)若A和B形成化合物的化学式为AB2,用电子式表示AB2形成过程_____________。
20.有X、Y、Z是原子序数相连的三种元素。元素X获得电子成为的离子;元素Z失去电子成为稳定的离子下列说法:
①元素Y的原子中电子数较X原子多一个,但比Z原子少一个;
②元素X的原子与氢反应能形成HX;
③元素Z为活泼的金属,跟水反应放出氢气生成物的水溶液显碱性;
④元素Y和Z、X可以反应
其中正确的是_______________(填序号)
19.O3、H2O2、SO2均可用于漂白,其中_________的漂白原理不同于其他二者,从化合价、氧化还原反应角度考虑,O3和SO2的水溶液______(填“能”或“不能”)发生反应,若能反应,SO2被__________(填“氧化”或“还原”)的产物是____________.
18.A、B、C三种元素为短周期元素,A元素的阴离子不被任何氧化剂氧化,则A离子的结构示意图为___________;1molB的单质能从盐酸中置换出3gH2,此时B转化为与Ne原子具有相同电子层结构的离子,则B元素是________,B的最高价氧化物对应的水化物的化学式为________,该化合物中的化学键属___________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com