
题目列表(包括答案和解析)
2.当不慎有大量Cl2逸到周围空气里时,可用浸有一定浓度的下列物质溶液的毛巾捂住鼻子,该物质是( )
A.NaOH B.NaCl C.KBr D.Na2CO3
1.下列关于氯水的叙述正确的是( )
A.新制氯水中只含Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出该气体是Cl2
D.氯水放置数天后PH变小
27.(6分)密闭容器中将3.62 gNaOH、Na2S、Na2SO3的混合物溶于50 mL某浓度的稀 H2SO4
中,不放出任何气体,再加入100 mL 0.1mol·L-1的Ba(OH)2溶液,正好中和过量的
H2SO4。将反应所得沉淀分离、洗净、烘干、称重,其质量为3.29 g 。求:
(1)原混合物中各物质的物质的量之比;
(2)原稀H2SO4的物质的量浓度。
26.(5分)23.第四主族元素R,在它的化合物R(OH)n中,其质量分数为0.778,在它的另一种化合物R(OH)m中,其质量分数为0.636。
(1)试求n和m的值。
(2)试求R的相对原子质量。
25.(8分)用石灰石和酸反应制取CO2气体,往往含有水蒸气、硫化氢、氯化氢、少量氧气等。为了得到干燥和较纯净的CO2,某学生设计了如下图的实验装置。所选用的试剂有浓硫酸、饱和碳酸氢钠溶液、硫酸铜溶液、铜网等。A是石灰石,G是收集干燥纯净的CO2的装置。
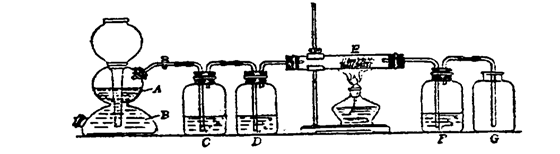
根据上述实验条件和要求回答下列各问:
(1)B物质是 ,E中盛放的是 。
(2)D洗气瓶中盛的是CuSO4溶液,除去杂质反应的离子方程式是
(3)C中盛的是 ,该装置反应的化学方程式 。
(4)F装置的作用是 ,所盛试剂是 。
(5)启普发生器中A与B反应产生CO2气体的离子方程式为 。
24.(9分)要分离一氧化碳、二氧化碳并分别得到干燥的气
体,某学生设计如右图装置,其中a、b是玻璃活塞。
(1)甲容器中盛______溶液;乙容器中盛_____溶液;
丙容器中盛_______溶液。
(2)实验时关闭_____(a、b),打开______(a、b),发
生反应的化学方程式是________________________,
这样得到的气体是__________________。
(3)当分离完一种气体后,关闭___,打开_____, 发
生反应的化学方程式是________________________________________,这样得到的气体是______________。
23.(6分)短周期元素A、B、C、D,它们的原子序数依次增大。其中A、C与B、D分别是同主族元素。又知B、D两元素的原子核中质子数之和是A、C两元素原子核中质子 数和的2倍。这四种元素的单质中有2种气体,2种固体。 (1)写出元素符号:A ;D ;
(2)写出两种均含有A、B、C、D四种元素的化合物相互作用逸出气体的离子方程
式 。
(3)A、C组成的化合物,常作为野外考察的取氢(H2)剂。试写出该化合物的电子式 ;该化合物中加入适量的水,即可形成氢气。写出制氢化学方程式 ;经研究发现,该化合物中加入某些单质(如:Si、Al),再加水,可以成倍地产生氢气。现取1mol该化合物中加入适量的单质硅,产生氢气 ____________mol。
22.(6分)不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。
下面是某些短周期元素的x值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x值 |
0.98 |
1.57 |
2.04 |
2.25 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
(1)通过分析x值变化规律,确定Mg、N的x值范围:
<x(Mg)< , <x(N)< 。
(2)推测x值与原子半径的关系是 。据据短周期元素的x值变化特点,体现了元素性质的 变化规律。
21.(4分)(1)常用的农药石硫合剂是硫粉和石灰乳拌合而成的一种浊液。其反应很复杂,其中反应的主要产物为CaS2O3、CaS•Sx和H2O。写出该反应的化学方程式___________
_ ;在此反应中硫单质_______(填“是”或“否”)发生了氧化还原反应。
(2)工业上制CuSO4时,不是直接用铜跟浓硫酸在加热条件下反应,而是将铜丝浸入稀H2SO4中,再不断地从容器下部吹入细小的空气泡,这样做的好处是①__________ _ ,②____________ _。
20.(3分)原硅酸通过分子间缩水聚合可形成不同的多硅酸(多聚体),如:
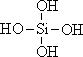
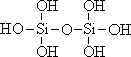
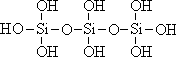
原硅酸 二聚体 三聚体
按上述规律,n个原硅酸聚合而成的链状多酸分子的通式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com