
题目列表(包括答案和解析)
24.(5分) 12 , 10 , ;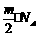 。
。
23.(3分) AgI , AgBr ; NaHCO3 。
32.(5分)加热38.0g Na2CO3和NaHCO3混合物至质量不再变化,剩余固体的质量为31.8g。计算:
求:⑴原混合物中NaHCO3的质量;
⑵求原混合物Na2CO3与NaHCO3的物质的量之比。
化 学
1-5 CDDBD 6-10 DACDB 11-15 ABBCB 16-20 ACBAD 21-22 CD
31.(5分)现有浓硫酸与铜反应生成二氧化硫气体的体积为2.24L(标准状况),
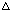 已知Cu+2H2SO4(浓)=== CuSO4+SO2↑+2H2O
已知Cu+2H2SO4(浓)=== CuSO4+SO2↑+2H2O
试计算:⑴反应后生成硫酸铜的物质的量
⑵若将生成的硫酸铜配制成500mL溶液,则该溶液的物质的量浓度是多少?
30.请利用下列装置及试剂组装一套装置。其流程是,先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性。试回答:
⑴按气体从左向右流动,请将各装置依次连接起来(填接口标号):a接 , 接
, 接e,d接 , 接h。
⑵烧瓶中发生反应的化学方程式是 。
⑶E装置的作用是 ,化学方程式 ,F装置的作用是 。
29.有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、NaCl等物质组成,为鉴定它们,做了如下实验:
①将固体混合物溶于水,搅拌后得无色溶液;
②向此溶液中滴入氯化钡,有白色沉淀产生;
③过滤,然后在白色沉淀中加入足量的稀HNO3,沉淀完全消失。由此推断:
固体混合物中肯定有 ,肯定没有 ,可能有 ,如果要进一步确定可能存在的物质,可采用①中取少量溶液滴加 溶液的方法来检查。
27.(2分)一定量Na2CO3和NaHCO3的混合物,溶于水中配成100mL溶液,Na+的浓度为0.5mol·L-1,若将等量的固体混合物加热最后得到固体 g。
|
①2NaCl+2H2O === 2NaOH+H2↑+Cl2↑ 氧化剂 还原剂
②KClO3+6HCl(浓) === KCl+3Cl2+3H2O 氧化剂 还原剂
⑵(6分)写出下列反应的离子方程式:
①大理石与稀盐酸反应制二氧化碳
②氢氧化钡溶液与硫酸铜溶液反应
③氯气与水反应
26.(4分)某学生往一支试管里按一定次序分别加入下列几种物质:A、KI溶液;B、淀粉溶液;C、氯水。发现溶液颜色按下面次序变化:①无色→ ②棕黄色→③蓝色。依据溶液颜色的变化回答下列问题:⑴加入以上药品的顺序是 ,⑵写出①→②的化学反应方程式
25.(4分)除去下列混合物中的杂质需要的试剂或操作方法:
CO2(HCl) , NaHCO3溶液(Na2CO3)
NaCl(BaCl2) , NaCl固体(碘)
24.(5分)已知粒子X2+的质量数为24,中子数为12,则X2+的核电荷数为 ,核外电子数为 ,该离子的结构示意图 ;mg该粒子的氧化物XO中含有中子数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com