
题目列表(包括答案和解析)
8、原子序数大于4的主族元素X、Y的离子 、
、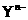 核外电子层结构相同,则关于X、Y两元素的叙述正确的是( )
核外电子层结构相同,则关于X、Y两元素的叙述正确的是( )
A.X的原子序数小于Y的原子序数 B. X、Y的核电荷数之差是(m-n)
C.Y元素的族序数与X元素的族序数之差是8-(m+n)
D.X和Y处于同一周期
7、下列叙述中正确的是( )
A.含有共价键的化合物一定是共价化合物
B.含有离子键的化合物一定是离子化合物
C.含非极性键的纯净物一定是单质
D.原子最外层2个电子的元素一定在ⅡA族
6、元素周期表中ⅠA元素R,有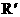 和
和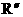 两种同位素,
两种同位素,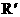 和
和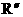 的相对原子质量分别为a和b,R元素中
的相对原子质量分别为a和b,R元素中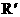 和
和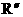 原子的百分比分别为x和y,则R元素的碳酸盐的式质量是( )
原子的百分比分别为x和y,则R元素的碳酸盐的式质量是( )
A.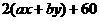 B.
B.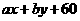 C.
C. D.
D.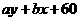
5、第四周期某主族元素的原子,它的最外电子层上有两个电子,下列关于此元素的叙述正确的是( )
A.原子半径比钾的原子半径大 B.氯化物难溶于水
C.原子半径比镁的原子半径大 D.碳酸盐难溶于水
4、已知a为ⅡA族元素,b为ⅢA族元素,它们的原子序数分别为m和n,且a、b为同一周期元素,下列关系式错误的是( )
A.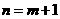 B.
B.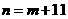 C.
C. D.
D.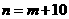
3、甲、乙是周期表中相邻两个主族的两种元素,若甲的原子序数为 ,则以下有可能是乙的原子序数是(
)
,则以下有可能是乙的原子序数是(
)
A.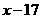 B.
B.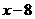 C.
C.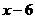
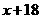
2、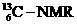 (核磁共振)可以用于含碳化合物的结构分析,
(核磁共振)可以用于含碳化合物的结构分析,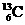 表示的碳原子( )
表示的碳原子( )
A.核外有13个电子,其中6个能参与成键 B.核内有6个质子,核外有7个电子
C.质量数为13,原子序数为6,核内有7个质子
D.质量数为13,原子序数为6,核内有7个中子
1、下列各组元素性质递变情况错误的是( )
A.Li、B、Be原子最外层电子数依次增多 B.P、S、Cl元素最高正化合价依次升高
C.N、O、F原子半径依次增大 D.Na、K、Rb的金属性依次增强
22.取5.4g由碱金属R及其氧化物R2O组成的混合物,使之与足量的水反应,蒸发反应后溶液得到8.0g无水晶体。
(1)判断该金属是哪一种碱金属?
(2)原混合物中R及R2O的质量各是多少?
21.将Na2CO3、NaHCO3的混合物1.9g,强热至无气体出现为止,恢复至原来状态,称量剩余物的质量减轻了0.31g,求原混合物中NaHCO3质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com