
题目列表(包括答案和解析)
33、400mL某浓度的NaOH溶液恰好与5.6LCl2(标准状况)完全反应,计算:(不用写过程)
(1)生成的NaClO的物质的量__________。 (2)反应物NaOH溶液的物质的量浓度________。
32、实验室是用二氧化锰和浓盐酸反应制氯气,写出该反应的离子方程式_____________________,
如果把干燥的氯气通入干燥的有色布条中,布条_____褪色,多余的氯气要用氢氧化钠溶液吸收,
写出该反应的离子方程式:_________________________________________________________,
指出该反应的还原剂:_________,氧化剂_________。
31、进行化学实验必须注意安全,下列说法正确的是(填写编号)___________________
A、制取硫化氢(有毒)气体时,必须在通风橱中进行。
B、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在不断搅拌下慢慢加入浓硫酸。
C、做实验时不能用手直接拿取金属钠。
D、让鼻孔靠近集气瓶口闻氯气的气味。
30、重铬酸钾(K2Cr2O7)是一种强氧化剂,重铬酸钾和浓盐酸反应生成氯化钾、三氯化铬、一种气体单质X和水。在下图的装置中,当重铬酸钾与浓盐酸共热时产生的气态单质X经过A、B两瓶后,在C处与加热的白色晶体反应,最后在D瓶底有紫黑色晶体状物质生成。
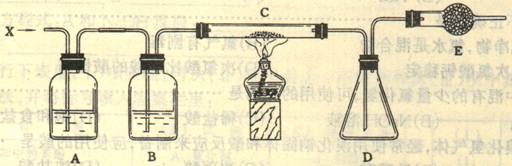
(1)重铬酸钾和浓盐酸反应的反应式(不用配平)_______________________________________
(2)要得到纯净的X气体,A瓶应盛_______________,其作用是_____________________。B瓶
应盛___________________,其作用是___________________。E瓶装置的作用是_____________,
为达到此目的,E装置中应盛放______________________________。
(3)在C处加热可以加快反应的速率,还能___________________,C处反应的化学反应方程式
是_______________________________________________________________________。
29、在9.5克某二价金属的氯化物中含有0.2摩Cl-,此氯化物的摩尔质量为_______________,该
金属元素的相对原子质量为_________________。
28、把加到红热的铜丝放入氯气瓶中,可观察的现象:_______________________________,再往瓶
中加入少量的水,振荡,溶液呈____色。上述反应的化学方程式:___________________________,
该反应是氧化还原反应,氧化剂是______________,电子转移数目为_________。
27、按要求用化学式回答:可用于人工降雨的物质是_________;涂于照相感光片上的是_________;
漂白粉的有效成分是______________。
26、卤族元素包括______、______、______、_______等元素(填元素符号),它们结构的共同点是
___________________,因此在化学反应中一般易_________个电子,变成______离子。
25、常温常压下,将40L氢气和氧气的混合气体引爆后冷却到原状态时剩余气体4L,则原混合气体中H2的体积可能是( )
A、12L B、16L C、24L D、28L
高一第一学期期末考试题
化学试卷
第二卷 非选择题(占50分)
班别________ 姓名__________学号__________ 成绩__________
原子量: H-1 N-14 C-12 O-16 S-32 Cl-35.5 Fe-56 F-19 Na-23
Mg-24 Al-27 Cu-64 Zn-65 Mn-55 Ag-108
24、在下列各组物质中,所含分子数相同,原子数也相同的是( )
A、1克氢气和16克氧气 B、1摩氩气和1摩氟气
C、1摩二氧化碳和标准状况下22.4L氨气 D、1摩二氧化碳和34克硫化氢
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com