
题目列表(包括答案和解析)
23.向a mol KAl(SO4)2的溶液中逐滴加入Ba(OH)2溶液。(1)反应的化学方程式 。
(2)若已加入Ba(OH)2溶液中含b mol溶质,试讨论:当a和b的比值为何值时,产生的沉淀的成分及其物质的量各是多少?将计算结果填入下表:
|
a与b之比 |
产生的沉淀 |
|
|
分子式 |
物质的量(mol) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
22.用重结晶法测定胆矾中结晶水的实验中,下面是某学生的实验记录:
干燥坩埚重:A g;W坩埚+晶体=B g;W坩埚+CuSO4=C g
(1)结晶水x的计算公式为 。
(2)若A=5.4 g,W坩埚+晶体=7.9 g;W坩埚+CuSO4=6.8 g,则该生测定的胆矾中结晶水的百分含量是 ,结果 (填偏大、偏小)
(3)从下列分析中指出发生误差的原因可能是 。
A.加热前称量容器时未完全干燥
B.最后两次加热后的质量相差较大(大于0.1 g)
C.加热后容器未放入干燥器中冷却
D.加热过程中晶体有少量溅失
21.实验室配制500 mL 0.5 mol·L-1的NaCl溶液,有如下操作步骤:①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;②把①所得溶液小心转入500mL容量瓶中;③继续向容量瓶中加蒸馏水至液面距离刻度2-3厘米处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部,与刻度线相切;④用少量蒸馏水洗涤烧杯和玻璃棒2-3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
请填写下列空白:
A.实验操作步骤的正确顺序为(填序号) 。
B.本实验用到的基本仪器有: 。
C.若出现如下情况,对所配溶液浓度将有何影响?没有进行操作④ ;加蒸馏水时不慎超过了刻度 。
D.若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度 ;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面 。
20.常温下A和B两种气体组成混合气体(A的分子量大于B的分子量),经分析混合气体中只含有氮和氢两种元素,而且不论A和B以何种比例混合,氮和氢的质量比总大于14/3,由此可确定A为 ,B为 ,其理由是 ;若上述混合气体中氮和氢的质量比为7∶1,则在混合气体中A和B的物质的量之比为 ;A在混合气体中的体积百分数为 。
19.由A、B两气体组成的混合气体8.6 g,在标准状况下占有体积为8.96 L,已知A和B的物质的量之比为3∶1,摩尔质量之比为14∶1,则A可能是 、 、 ;B 。
18.化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10 mL A气体能分解生成15 mL O2和10 mL F2(同温同压)。
(1)A的化学式是 ,推断理由是 。
(2)已知A分子中x个氧原子呈…O-O-O…链状排列,则A分子的电子式是 ,A分子的结构式是 。
17.1个12C的质量是A kg,1个Na的质量是B kg,Na的摩尔质量是 。
16.某温度下,向一未饱和的Na2CO3溶液中加入20 g无水Na2CO3,或加入50 g Na2CO3·7H2O晶体,都恰好使溶液达到饱和,则Na2SO3在此温度时的溶解度为
A.25 g B.75 g C.50 g D.20 g
15.用1 L 1.0 mol·L-1 NaOH溶液吸收0.8 mol CO2,所得溶液中的CO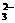 和HCO
和HCO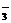 的物质的量浓度之比约为
的物质的量浓度之比约为
A.1∶3 B.2∶1 C.2∶3 D.3∶2
14.某14%的KOH溶液加热蒸发掉100 g水后,得到28%的苛性钾溶液80 mL,则后来溶液的物质的量浓度为
A.6.25 mol·L-1 B.4.25 mol·L-1
C.5 mol·L-1 D.7.5 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com