
题目列表(包括答案和解析)
5.为方便某些化学计算,有人将98%的浓H2SO4表示成下列形式,其中合理的是( )
A. H2SO4· H2O
B. H2SO4·H2O
H2O
B. H2SO4·H2O
C. H2SO4·SO3
D. SO3·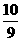 H2O
H2O
4.下列比较正确的是( )
A.原子半径:Na>K B.价电子数:P>S>Cl
C.最高正价:Se<Te D.离子半径:S2->Cl->K+
3.某Na2SO3样品已部分被氧化为Na2SO4,经测定该混和物中含硫25%,则混和物中Na2SO3与Na2SO4的物质的量之比为( )
A.7:6 B.6:7 C. 7:1 D. 1:7
2.下列反应中,不能产生黑色固体的是( )
A.铜在硫蒸气中燃烧 B.铁丝在氧气中燃烧
C.氯气与硫化氢气体混和 D.氯化锌溶液与硫化钠溶液混和
1. 某元素的原子最外层有 2 个电子, 该元素( )
A.一定是金属元素 B.最高化合价一定为 +2 价
C.一定是 ⅡA 族元素或是 He D.无法确定属于哪类元素
21. (8分)含FeS286%的黄铁矿燃烧时损失硫5%,由SO2转化为SO3时转化率为99%,问生产98 %的硫酸1吨,需黄铁矿多少吨
乙卷(50分)
20. 实验室乙醇与浓硫酸反应制乙烯,常因温度过高而使烧瓶中液体变黑。为了验证被硫酸氧化确实有二氧化碳气体生成,某同学设计如图所示的A、B、C三个装置进行实验(乙醇与浓硫酸的反应装置省略,并假设装置C中的反应完全)。请回答:

(1)装置B的作用是_______;(2分)
(2)三个装置之间的连接顺序是(填写导管口序号a、b、c、d、e、f)(3分):
气体发生装置导管口接_______,然后_______接_______,_______接______;
(3)装置A、B、C中各有什么现象?(3分)
A中______,B中_______,C中_______;
19. A、B、C、D都是短周期的元素。A元素的原子核外有2个电子层,最外层已达到饱和。B元素位于A元素的下一周期,最外层的电子数是A元素最外层电子数的1/2。C元素的离子带有两个单位正电荷,它的核外电子排布与A原子相同。D元素与C元素属同一周期,D元素原子的最外层电子数比A的最外电子数少1。
根椐上述事实判断:
C是 D是 (填元素符号)
B元素在周期表中的位置中 ,
18. 元素的种类决定于________________ , 元素的化学性质主要决定于_________________________.在原子序数为 1 - 18 号的元素中酸性最强的含氧酸是 _________,气态氢化物最稳定的是 __________。
17. 汽车尾气(含有碳氢化合物、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(铂、钯合金作催化剂)。它的特点是使CO和NO反应,生成可参与大气生态循环的无毒气体,并促使碳氢化合物充分燃烧用SO2的转化。
(1)写出CO和NO反应的化学方程式_______________________________。
(2)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因是_______________。
(3)控制城市空气的污染源的方法可以有______
A.开发氢能源 B.使用电动车 C.植树造林 D.戴上呼吸面具
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com