
题目列表(包括答案和解析)
2.X和Y两元素的原子,在化学反应中都容易失去电子形成稳定结构,已知X的原子半径小于Y的原子半径,下列说法正确的是( )
A.两种原子失去电子的能力相同
B.两种原子的核外具有相同的电子层数
C.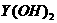 的碱性比
的碱性比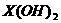 的碱性强
的碱性强
D.Y的金属性比X的金属性强
1.由H、D、T与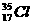 和
和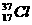 形成的氯化氢分子,其相对分子质量的数值是( )
形成的氯化氢分子,其相对分子质量的数值是( )
A.2种 B.5种
C.6种 D.9种
6.A元素的原子序数为13,它的最高价氧化物的水化物是 _________性;当其与强酸反应的现象是___________________,离子方程式为______________;当其与强碱反应时的现象是______________,离子方程式为____________________。
[综合题]
5.在第三周期中置换H能力最强的是________________元素(符号),化学性质最稳定的元素符号是__________________,最高价氧化物对应的水化物酸性最强的分子式为__________________,碱性最强的分子式为______________,显两性的分子式为_________________________,原子半径最大的金属元素的符号是________________,离子半径最小的金属离子结构示意图________________。
4.X、Y、Z三种元素的原子,其核外电子排布分别为:X原子最外层有一个电子,Y原子的第一、二、三层电子数分别为2、8、3,Z原子第一、二层电子数为2、6,由这三种元素组成的化合物的化学式可能是( )
A.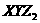
B.
C.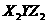
D.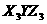
3.已知某元素R的气态氢化物的化学式为 ,下列叙述中不正确的是( )
,下列叙述中不正确的是( )
A.该元素的原子最外电子层上有6个电子
B.该元素最高正价氧化物的化学式为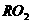
C.该元素一定是非金属元素
D.该元素最高价氧化物对应水化物的化学式为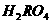
2.能说明Cl的非金属性比S的非金属性强的事实是( )
A.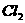 与
与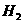 反应生成HCl,而S与
反应生成HCl,而S与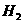 反应生成
反应生成
B.向 的水溶液中通入
的水溶液中通入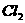 可得到淡黄色的固体S
可得到淡黄色的固体S
C.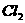 能与水反应,而S不与水反应
能与水反应,而S不与水反应
D.Cl原子最外电子层上有7个电子,而S原子最外电子层上有6个电子
1.元素性质呈周期性变化的原因是( )
A.相对原子质量逐渐增大
B.核电荷数逐渐增大
C.核外电子排布呈周期性变化
D.元素的化合价呈周期性变化
26.短周期元素A、B,A原子最外层电子数为a个,次外层电子数为b个;B原子M层电子数为(a-b)个,L层为(a+b)个,则A为_________,B为__________。
25.R元素的单质4.5g,跟足量的硫酸反应生成R2(SO4)3并放出5.6L的H2(标态)。
试求:⑴R的原子量⑵若R原子中质子数比中子数少1则R是什么元素?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com