
题目列表(包括答案和解析)
21.运用物质结构和元素周期律的知识解释下列事实
(1)元素的相对原子质量绝大多数和都不是整数解释为
。
(2)Be(OH)2+2NaOH=Na2BeO2+H2O解释为
。
(3)氟没有正化合价,解释为 。
20.由IIIA族元素A和VIA族元素的B组成的三种阴离子的结构如下图:


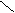
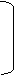

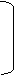


 B
X-
Y-
B
B
Z-
B
X-
Y-
B
B
Z-
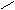
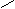
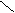
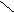 A-B
B
A-B
B
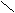
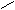
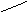

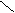

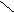 B
A-B B-A A-B
A A
B
A-B B-A A-B
A A
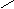
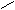 A-B B
B
B B
A-B B
B
B B
B 、 、
所带电荷数分别为X= ,Y= ,Z= 。
19.A、B、C、D四种短周期元素,A、D同族,B、C同族,C、D同周期,A形成的单质是气体中密度最小的气体,B元素的原子最外层电子数是总电子数的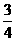 ;
;
①写出这四种元素的元素符号A B C D 。
②X和Y都是由这四种元素所形成的化合物,写出X和Y溶液反应的离子反应方程式
。
18.下列说法中错误的是
A Na2SO3与BaCl2溶液作用有白色沉淀生成加HNO3后沉淀消失
B将SO2气体通入Ba(OH)2溶液中有白色沉淀生成
C将SO2气体通入用硝酸酸化的BaCl2中有白色沉淀生成
D将硝酸酸化后的BaCl2试液加入某种溶液中,有白色沉淀生成,不能判断该溶液中一定含有SO42-离子
17.FeCl3溶液呈黄色,FeCl2溶液呈浅绿色,向BaCl2溶液中通入SO2气体无现象,但向FeCl3和BaCl2的混合液中通入SO2气体,则出现白色沉淀,过滤得浅绿色溶液,根据该现象,下列说法正确的是
A SO2被氧化,FeCl3被还原 B SO2被还原,FeCl3被氧化
C白色沉淀是BaSO3和S的混合物 D白色沉淀是BaSO4
16.有相同电子层结构的三种微粒An+、Bn-、C,下列分析正确的是
A原子层数关系C>B>A B粒子的半径关系Bn->An+
C C一定是稀有气体元素的一种原子 D原子半径的关系是A<C<B
15.X、Y均为短周期元素,已知aXn-比bYm+多两个电子层,则下列说法中正确的是
A b<5 B X只能位于第三周期 C a+n-b+m=10或16 D Y不可能位于第二周期
14.已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对较弱是HXO4>H2YO4>H2ZO4,则下列说法正确的是
A气态氢化物的稳定性HX>H2Y>ZH3 B金属性Y<X<Z
C原子半径X>Y>Z
D原子最外电子层上电子数关系Y=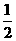 (X+Z)
(X+Z)
13.运用元素周期律分析下列判断中错误的是
A铍(Be)的氧化物的水化物可能有酸性
B砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸
C硫酸锶(SrSO4)是难溶于水的白色固体
D硒化氢(H2Se)是无色、有毒,比H2S稳定的气体
12.设某元素中某原子原子核内的质子数为m,中子数为n,则下列判断正确的是
A不能由此确定该元素相对原子质量 B这种元素的相对原子质量为m+n
C若碳-12的原子质量为Wg,此原子的质量为(m+n)Wg
D核内中子的总质量小于质子总质量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com