
题目列表(包括答案和解析)
元素周期律是元素性质随核外电子排布的周期性变化而呈周期性变化的规律,周期表是周期律的表现形式。
1、元素周期表的结构


|
电子层数 |
1 |
2 |
3 |
4 |
…… |
N |
|
电子层符号 |
K |
L |
M |
N |
…… |
|
|
最多容纳电子数 |
2 |
8 |
18 |
32 |
…… |
2n2 |
注意:不管有多少电子层,最外层电子数不超过8个(K为最外层不超过2个),次外层不超过18个(L为次处层不超过8个),倒数第三层不超过32个。
电子层排布可用原子结构示意图表示。
24.(7分)在1.00L1.00mo1·L-1NaOH溶液中通入0.750mol的CO2。
(1)计算所得溶液中含有的NaHCO3和Na2CO3的物质的量。
(2)将上述溶液蒸于、灼烧,可以得到Na2CO3多少克?
23.(6分)将标准状况下13.44L氯化氢气体溶解于水后配成50.0mL溶液,得到密度为1.19g·cm-3的盐酸。试计算:
(1)所得盐酸的物质的量浓度。
(2)该盐酸中溶质的质量分数。
22.(8分)根据下列反应框图填空。已知B、D、E、L常温下均为密度比空气大的气体,D呈黄绿色,其他无色,D、E为单质,其他为化合物。A是一种淡黄色固体,C在水中的溶解度随温度的升高而减小,G难溶于水,L能使湿润的蓝色石蕊试纸变红。
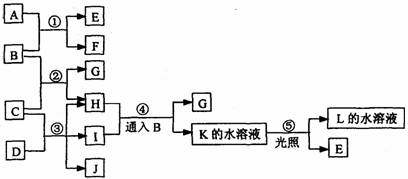
(1)F的俗名是 。
(2)反应①的用途是 。
(3)反应②在实验室常被用来 。
(4)工业上利用反应③生产 。
(5)A与H反应生成E,另有一种物质也能与H反应生成E,写出这两个反应的化学方程式:
21.(4分)某固体混合物可能由KNO3、K2SO4、CaCl2、NaCl、CuCl2、Na2CO3中的一种或几种组成,依次进行如下实验,观察到的实验现象记录如下:
①用干净的铂丝蘸取混合物在酒精灯火焰上灼烧,透过蓝色的钴玻璃,可以观察到火焰呈紫色;
②混合物加水得到无色溶液;
③向上述溶液中滴加过量BaCl2溶液,有白色沉淀生成,将该沉淀滤出,此沉淀可完全溶于稀硝酸;
④向③的滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸。
据此,可判断混合物中肯定含有 ,不能肯定是否含有 (均用化学式填写)。
20.(9分)为探究氯水中除H2O分子外还含有哪些粒子,某化学兴趣小组做了如下实验:
(1)观察氯水颜色,发现氯水呈黄绿色,说明氯水中肯定含有的粒子是(填化学式,下同) ;
(2)取少量氯水于试管中,滴入硝酸酸化的AgNO3溶液,有白色沉淀生成,说明氯水中含有的粒子是 ;
(3)另取少量氯水于表面皿中,将一块蓝色石蕊试纸置于其中,发现试纸先变红然后褪色,说明氯水中含有的粒子是 和 ;
(4)以上实验不能说明溶液中是否有 存在;
(5)通过以上实验说明氯气与过量的水的反应是 (填“完全”、“不完全”)的,因此氯气与水的反应是一个 (填“可逆”、“不可逆”)反应,该反应的离子方程式是
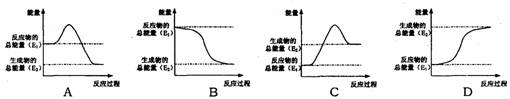
19.(4分)人们常利用化学反应中的能量变化为人类服务。
(1)煤是一种重要的燃料,在点燃条件下燃烧,放出大量的热。其在燃烧过程中能量的变化与下列示意图中的 (填字母代号)最相符。
(2)将一定量的碳酸钠晶体与硝酸铵晶体密封于一塑料袋中,用线绳绑住塑料袋中间部分,使两种晶体隔开,做成“冰袋”。使用时将线绳解下,用手使袋内两种固体粉末充分混合,便立即产生低温,这种“冰袋”可用于短时间保鲜食物。则碳酸钠与硝酸铵的总能量 (填“高于”或“低于”)反应后生成产物的总能量。
(3)化学反应中的能量变化不仅仅表现为热能的变化,有时还可以表现为其它形式的能量变化。比如,停电时,人们一般点蜡烛来照明,这是将化学能转化为 ;人们普遍使用的干电池,是将化学能转化为 。
18.(10分)某校化学兴趣小组拟用浓盐酸与二氧化锰加热反应,制取并收集2瓶干燥、纯净的氯气。为防止换集气瓶时生成的氯气污染空气,设计了如下装置: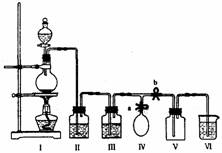
(1)写出该反应的化学方程式并标出电子转移的方向和数目。
(2)装置Ⅲ中盛放的药品是 ,其作用是
(3)装置Ⅵ中盛放的药品是 ,其作用是 。
(4)实验开始后, (用“打开”或“关闭”等简洁的语言叙述对弹簧夹a和b的操作,下同);当集满一瓶氯气时, ,使氯气储存在气球中;换好集气瓶后, ,继续收集氯气。
17.(4分)要配制浓度为2.0 mo1·L-1的NaOH溶液100 mL,下面的操作不正确的是 (填代号)。
A.称取8.0gNaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解
B.称取8.0gNaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
C.称取8.0gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
D.称取8.0gNaOH固体,放入100mL烧杯中,加少量蒸馏水同时不断搅拌,待固体完全溶解后,趁热将烧杯中的溶液倒入100mL容量瓶中。然后加入蒸馏水到刻度,盖好瓶塞,反复摇匀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com