
题目列表(包括答案和解析)
3、1999年新发现的114号元素的同位素,其中子数为184,该同位素原子的质量数为
A.70 B.114 C.228 D.298
2、IBr属于卤素互化物,它的化学性质活泼,其性质与卤素单质相似。它与水反应的化学方程式为:IBr + H2O = HBr + HIO 则下列关于IBr的叙述不正确的是A、固态的IBr是共价化合物
B、在许多反应中,IBr是强氧化剂 C、在IBr与H2O反应中,IBr既是氧化剂,又是还原剂
D、IBr与NaOH溶液反应,生成NaBr、NaIO和H2O
1、潮湿的氯气、新制的氯水、次氯酸钠及漂白粉的水溶液均能使有色布条褪色,是因为它们均含有A、氯气 B、次氯酸 C、次氯酸根 D、氯化氢
30. (1)略(2)NaOH>Mg(OH)2
`(3)NH3+H2O≒NH3·H2O≒NH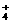 +OH- (4)分子晶体
+OH- (4)分子晶体
29.(1)Kr (2)NaOH (3)K+;Ca2+;Mg2+
(4)H2O;2H2O+2K=2KOH + H2 ↑;H2O + Cl2=HClO + HCl
(5)NaOH;HBRO4;NaBr;黄;2NaBr+ Cl2=2NaCl+ Br2
(6)NaOH+ Al(OH)3=NaAlO2+ 2H2O;OH-+Al(OH)3=AlO2- + 2H2O
(7)CCl4;橙红
(8)18。
28. 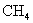 ;
;
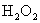 ;
;
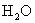 ;
;
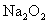 ;
;
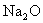 ;
;

19.D 20.C、D 21.A 22AB 23.A 24.B 25.B、C 26.B 27.B、C
10.C 11.B 12.A 13.B 14.D 15.C 16.D 17.D 18.A、C
1.C 2.D 3.B 4.C、D 5.B 6.B 7.A、D 8.B 9.B、C
30.a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
|
微粒代码 |
a |
b |
c |
d |
e |
f |
g |
|
原子核数 |
单核 |
单核 |
双核 |
多核 |
单核 |
多核 |
多核 |
|
带电荷数 (单位电荷) |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可形成两个共价型g分子。试写出:(1)a微粒的核外电子排布式
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为 > (用化学式表示) (3)d溶于水的电离方程式
(4)g微粒所构成的晶体类型属 (5)c微粒是 ,f微粒是
(用化学式表示)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com