
题目列表(包括答案和解析)
3.据报道,科学家发现了一种新元素,它的原子核内有161个中子,质量数272该元素的质子数为 ( )
A.111 B. 161 C.272 D .433
2.下列微粒中,既含有离子键又含有共价键的是 ( )
A.Ca(OH)2 B.H2O2 C.Na2O D.MgCl2
1.下列物质中,既能与强酸反应又能与强碱反应的是 ( )
①Na2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3
A. ①②③④ B. ①②③ C. ①②④ D. ②③④
28.某元素的同位素原子ZAX,其氯化物XCl21.11g配成溶液后,需用1mol/L的AgNO3溶液20mL,才能把氯离子完全沉淀下来。已知同位素中有20个中子。
(1)计算X的质量数是多少。
(2)指出X元素在周期表中的位置(周期、族)。
(3)把X的单质放入水中,有何反应现象?滴入的酚酞呈现什么颜色?写出有关的化学方程式。
27.A元素最高价离子0.5mol被还原成中性原子时得到6.02×1023 个电子,当A的单质与盐酸充分反应放出0.02g氢气,消耗A单质0.4g,B元素的原子核外电子层数与A原子相同,B元素形成的单质为深红棕色的液体。
(1). A、B两元素为A ,B .
(2). 用电子式表示A、B形成化合物的过程 .
(3). 这种化合物所含的化学键为 .
26.(8分)A、B、C、D、E为原子序数逐渐增大的主族元素,已知A、B、E三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3,回答:
(1)写出下列元素符号:A______________,E______________,D______________。
(2)写出A、B两元素最高价氧化物的水化物相互反应的化学方程式:_____________
A、E两元素最高价氧化物的水化物相互反应的化学方程式:
______________________。
(3)比较D、E最高价氧化物对应水化物的酸性: 。
25.(共6分) Li3N是离子化合物,它与水作用可生成NH3,试回答
(1) 写出Li3N的电子式________
(2)写出Li3N与水反应的化学方程式________
(3)微粒半径关系,Li+________N3-,Li________N(填>、<、=)
24.(16分)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,0.1molE单质与足量酸作用,在标准状况下能产生3.36LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
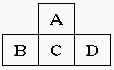
(1)五种元素的名称:A__________,B______________,C____________,D_____________,E______________。
(2)画出C原子、A离子的结构示意图:______________。
(3)B单质在D单质中燃烧,反应现象是______________,生成物的化学式为__________
(4)A与E形成的化合物的化学式是______________,它的性质决定了它在物质的分类中应属于______________。
(5)向D与E形成的化合物的水溶液中滴入烧碱溶液直至再无明显现象发生时,观察到的现象是___________________________,有关反应的离子方程式为________________。
23.(7分)A、B两种离子具有相同的电子层,A、B两元素的单质都能与水剧烈反应,在反应中A单质为氧化剂,B单质为还原剂。则:
(1)A元素位于______________周期______________族。新发现A的一种含氧酸的化学式为HAO,其中A的化合价为______________。
(2)A单质与水反应的化学方程式为______________。
(3)B单质与水反应的离子方程式为______________。
22. (6分)等质量的H2O和D2O,所含氧原子的个数比为 . 它们与足量金属钠完全反应放出气体的体积比(同温同压)为 ,质量比为 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com