
题目列表(包括答案和解析)
6、下列物质中的氮元素不能被还原的是
A.HNO3 B.NaNO2 C.N2 D.(NH4)2SO4
5、关于2g氢气,下列叙述正确的是
①体积约为22.4L②约含有6.02×1023个分子③含有1molH2④含有2molH
A.全对 B.只③对 C.③④对 D.②③④对
4、下列关系正确的是
A. 还原性: Na>K B. 离子半径:Na+>K+
C. 热稳定性: Na2CO3>NaHCO3 D. 熔点: Na<K
3、各取0.1mol钠、镁、铝、铁分别跟足量的盐酸反应,生成的氢气在标准状况下,体积最大的是
A.铁 B.铝 C.镁 D.钠
2、下列物质属于强电解质的是
A.Cl2 B.醋酸 C.NaNO3 D.H2O
1、医生建议患甲状腺肿大的病人多食海带,这是由于海带含有较丰富的
A.碘元素 B.氯元素 C.溴元素 D.氟元素
(6分)24.配制250 mL 0.2 mol/L的KCl溶液时,需要用天平称量_____g KCl。所需仪器有托盘天平、量筒、烧杯、玻璃棒、 、 。并分析下列操作可能导致的最终溶液的物质的量浓度误差:(填“偏大”、“偏小”、“无影响”)
(1)移液时容量瓶尚未干燥 ;(2)定容时俯视 ;(3)定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线 。
(5分)25.现用CO2气体和NaOH固体制取较纯的Na2CO3固体。简述操作过程。
要求:①不能用NaHCO3受热分解;②方法要最简单;③由于Na2CO3固体要“较纯”,必须考虑反应物的用量。
(2分)17.充分加热碳酸钠和碳酸氢钠混合粉末,产生的气体分别通过足量的Na2O2、浓硫酸,最终得到的气体是_____(用化学式填写),其电子式为_________。
(4分)18.在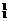 H,
H,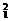 H,
H,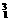 H,
H, 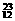 Mg,
Mg,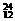 Mg,
Mg,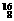 O,
O,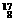 O,
O,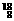 O中共有_______种元素,______种原子,中子数最多的是__________。D218O的相对分子质量为_________。
O中共有_______种元素,______种原子,中子数最多的是__________。D218O的相对分子质量为_________。
(4分)19.实验室制取有毒的氯气时,常用氢氧化钠溶液来吸收多余的氯气,其反应的化学方程式为:Cl2+2NaOH==NaCl+NaClO(次氯酸钠)+H2O。写出其离子方程式______________________,并在化学方程式上用“双桥法”标出电子转移的方向和数目。
(15分)20.(1)8 g某物质含有3.01×1022个分子,该物质的相对分子质量为 。(2)标准状况下,1.12 L氯化氢气体溶于水中配成250 mL溶液,此溶液中盐酸的物质的量浓度为 ,取出10mL此溶液,其中含氯化氢的质量为 。(3)3.2 g XO2中含有0.1 mol的氧原子,则X的摩尔质量为 。(4)V L Al2(SO4)3溶液中含有A g Al3+ 离子,则此溶液中SO42-的物质的量浓度是 _______________。
(9分)21.标准状况下,a L HCl气体溶于10 g水中,得到的盐酸的密度为b g·cm-3,则该盐酸的物质的量浓度为____________________ mol/L;溶质质量分数为c%,密度为d g/cm3的硫酸溶液V mL加水稀释到5 V mL,所得溶液的物质的量浓度为_______________ mol/L;相对分子质量为A的某物质在室温下的溶解度为B g,此饱和溶液物质的量浓度为D mol/L,则该饱和溶液密度为________________ g/cm3。
(4分)22. 已知:Na2O+CO2==Na2CO3,根据同主族元素性质相似,完成下列反应的化学方程式: Na2S+ As2S5==________________。欧洲核子研究中心于1995年9至10月间制成了世界上第一批反原子--共9个反氢原子,揭开了人类制取、利用反物质的新篇章。请用离子方程式表示出反物质酸碱中和反应的实质________________________。
(3分)23.用1000 g溶剂中所含溶质的物质的量来表示溶液的浓度叫做质量物质的量浓度,其单位是mol/Kg。10 mol/Kg的硫酸的密度是d g/cm3,则其物质的量浓度为 ________________mol/L。
16. 某KOH溶液,蒸发掉63 g水后,溶质质量分数恰好增大一倍,体积变为500 mL,则浓缩后溶液的物质的量浓度可能为 ( )
A.4 mol/L B.3 mol/L C.2.5 mol/L D. 0.63 mol/L
第Ⅱ卷(非选择题,共52分)
15.两种短周期元素组成的化合物中原子数比为1:3,若两种元素的原子序数分别为a和b,则a和b的关系可能为 ( )
① a==b+5;②a+b==8;③a+b==30;④a==b+8
A.②③ B.①②④ C. ②③④ D.①②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com