
题目列表(包括答案和解析)
26.(1)(2分)已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色的溶液,其化学方程式是:
PbSO4+2CH3COONH4 =(CH3COO)2Pb+(NH4)2SO4。当醋酸铅溶液中通入H2S时,有黑色沉淀PbS和CH3COOH生成。表示这个反应离子方程式是
(2)(4分)已知4℃时四种化合物在水中和液氨中的溶解度如下表:
|
|
AgNO3 |
Ba (NO3)2 |
AgCl |
BaCl2 |
|
H2O(l) |
170g |
9.20g |
1.50×10-4g |
33.3g |
|
NH3(l) |
86.0g |
97.2g |
0.80g |
0.00g |
①上述四种物质能在水中发生的复分解反应为_________________________________;
②能在液氨中发生的复分解反应为_____________________________________。
(3)(4分)请把下面一些常用危险化学药品的标志贴在对应的化学药品瓶子上(在横线上写上编号即可)。
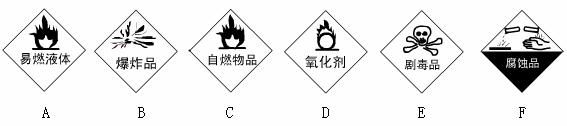
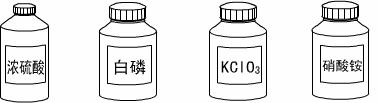
______ ______ ______ ______
(4)(8分)现有碳酸盐矿石(主要成分为CaCO3、BaCO3)需分离出BaCO3,并尽可能除去Ca2+,为完成此分离查得有关溶解度(克/100克水)数据如下:
 温度
温度物质 |
0℃ |
50℃ |
80℃ |
|
Ca(OH)2 Ba(OH)2 |
0.173 1.64 |
0.130 13.1 |
0.004 101.5 |
分离要求:(1)原料只有矿石、焦炭、空气和水,不用其它化学原料;(2)Ca2+含量越低越好。下图是分离的实验步骤,在箭头上方注明反应所需条件、方法和所需的物质,在方框里写上各步产物的分子式或化学式。

(5)(6分)实验室欲配制6mol/L的硫酸溶液.现在三种不同浓度的硫酸:①240mL、1mol/L的硫酸 ②150mL25%(ρ=1.18g/cm3)的硫酸③18mol/L的H2SO4足量.还有三种规格的容量瓶:250mL、500mL、1000mL.配制要求:①②两种H2SO4全部用完,不足部分由③补充.问需选用哪种容量瓶?需用18mol/L浓H2SO4多少毫升?
25. (6分)将5.0LNaCl溶液和3.0LBaCl2溶液混和,设混和后总体积为8.0L,并测得NaCl物质的量浓度为0.50mol·L-1,BaCl2物质的量浓度为0.30mol·L-1。问:
(1)混合溶液中则Cl-物质的量浓度为多少?
(2)混和前NaCl溶液中NaCl的物质的量浓度为多少?
(3)混和前BaCl2溶液中BaCl2的物质的量浓度为多少?
24.(4分)将下列离子方程式改写成化学方程式
(1)Fe3++3OH-==== Fe(OH)3↓
(2)Ba2++SO42-==== Ba SO4↓
(3 ) CO32-+2H+====CO2↑+H2O
(4)Fe2O3+6H+====2Fe3++3H2O
23.(4分)写出下列反应的离子方程式:
(1)MgSO4(aq)与Ba(OH)2(aq)反应
(2)Fe(OH)3溶于稀硫酸
(3)CO2通入澄清的石灰水
(4)K2CO3(aq)与AgNO3(aq)反应
22.(8分)H2SO4的摩尔质量为 ,1.204×1024个H2SO4分子物质的量为 ,所含电子物质的量为 ,共含 个氧原子
21.(5分)现有mg某气体,它由四原子分子构成,它的摩尔质量为M g·mol-1。则:
(1)该气体的物质的量为__________________mol。
(2)该气体所含原子总数为________________个。
(3)该气体在标准状况下的体积为_____________L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______________。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_______________g·mol-1。
20.(13分)实验室用碳酸钠晶体配制1.00 mol/L的Na2CO3溶液100mL,回答下列问题:
(1)所需主要仪器为:药匙、 、 、 、 、
和 。
(2)本实验须称量碳酸钠晶体(Na2CO3•10H2O) g。
(3)容量瓶上标有 、 、 。
(4)某同学将称量好的碳酸钠晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进所选的且经检查不漏水的容量瓶中,洗涤烧杯2--3次,洗涤液也移至容量瓶中,然后加水至离刻度线2cm处,用滴管加水至刻度线。请指出上述操作中的3处错误:
①
②
③
19.(12分)(1)对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、洗气、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用 的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
②除去H2中的CO2,可用 的方法除去。
③除去乙醇中溶解的微量食盐可采用 的方法。
④粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再 ;然后将溶液调成中性并
就可以得到较为纯净的氯化钠。
⑤除去氧化钙中的碳酸钙可用 的方法。
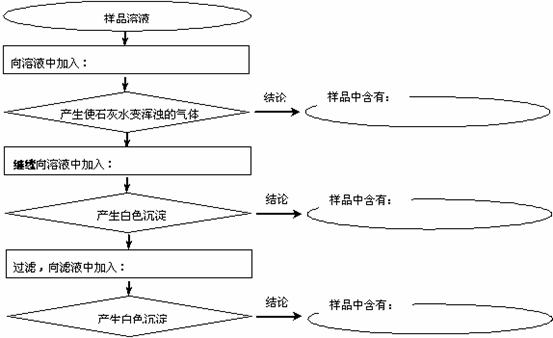 (2)某样品中含有碳酸钠及少量的硫酸钠和氯化钠。某学生为了检验其成分,按照下图所示步骤进行实验,请将所加试剂及有关结论填写在相应的空格中。
(2)某样品中含有碳酸钠及少量的硫酸钠和氯化钠。某学生为了检验其成分,按照下图所示步骤进行实验,请将所加试剂及有关结论填写在相应的空格中。
18.某实验室用下列溶质配制一种混合溶液,已知溶液中c(K+)=c(Cl-)=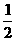 c(Na+)=
c(Na+)=
c(SO42-)(c表示物质的量浓度),则其溶质可能是
A.KCl、Na2SO4 B.KCl、Na2SO4、NaCl
C.NaCl、Na2SO4、K2SO4 D.KCl、K2SO4、Na2SO4
第Ⅱ卷(非选择题 共76分)
17.能正确表示下列化学反应的离子方程式的是
A.澄清的石灰水与盐酸的反应 OH-+H+ = H2O
B.氧化铜与硝酸(aq)反应 O2- + 2H+ = H2O
C.硫酸镁(aq)与氢氧化钡(aq)混合 Ba2++SO42-=BaSO4↓
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com