
题目列表(包括答案和解析)
1、 下列叙述中,通常不能作为判定两种元素得电子能力强弱的依据是
A. 其气态氢化物稳定性的强弱
B. 元素氧化性的强弱
C. 其最高价氧化物的水化物酸性的强弱
D. 单质熔点的高低
22、(8分)将一定量氯气通人250ml KBr溶液中,反应后将溶液蒸干,测知所得固体
中含溴元素10克,且K+和Cl-的物质的量之比为2:1,试求:
(1)标况下通人氯气的体积?
(2)原溴化钾溶液物质的量浓度?
21、(6分)钠、过氧化钠的混合物加入足量的水中生成的混合气体点火爆炸,恰好完
全反应,则原混合物中Na、Na2O2的物质的质量比是多少?
 19、(14分)实验室用右图所示装置制备氯气,并
19、(14分)实验室用右图所示装置制备氯气,并
进行氯气性质实验,请回答下列问题:
(1)A中加入二氧化锰,B中盛有浓盐酸,则烧
瓶中发生反应的离子方程式为____________________________________________________;
(2)C中盛有紫色石蕊溶液,则C中的现象是__________________________________;
(3)D中盛有KI淀粉的混合溶液,现象是______________________________,反应化学方程式__________________________________;
(4)E中是AgNO3溶液,现象是______________________________________,反应化学方程式_____________________________,_____________________________。
(5)F中一般应盛有__________________________________溶液,其作用是_________________发生反应的离子方程式__________________________________。
20、(9分)现有溶质的质量分数为36.5%,密度为1.19g/cm3的盐酸,若配制2mol·L-1的盐酸250mL,需量取该浓盐酸____________ml。该实验所需要的仪器有_____________
____________、___________________、________________、___________、__________。
下列操作使配得溶液浓度偏高的是(填序号)_____________________ 。
A、洗净的容量瓶底部残留蒸馏水
B、把溶液从烧杯转移到容量瓶里时,不慎流到瓶外数滴
C、稀择浓盐酸的烧杯没有用蒸馏水
D、定容时俯视液面使之与刻度线相切
18、(6分)有A、B、C、D、E、F、G七种气体,它们分别是CO、O2、H2、C02、C12、HBr、HCl中的一种,通过下列事实回答问题:
①A、B、C均难溶于水,D、E能溶于水,F、G易溶于水;
②A和C都能在B中燃烧,火焰呈蓝色,且C在B中的燃烧产物是D;
③A也能在E中燃烧,火焰为苍白色,生成物为F。
据以上事实,生成下列反应的化学方程式:
(1)C在B中燃烧_______________________________________________;
(2)气体D通入足量澄清石灰水中__________________________________________;
(3)少量E气体通入足量G的水溶液中____________________________________________;
17、(6分)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为
XY2(液)+3O2(气)=XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积为672mL,密度为2.56g·L-1。则:
①反应前在标准状况下O2的体积是--mL;
②化合物XY2的摩尔质量是____________;
③若XY2分子中X、Y两元素的质量比为3:16,则X、Y两元素的符号分别是______
和__________ 。
16、(6分)现有下列三个氧化还原反应。 ①2FeCl 3十2KI一2FeCl2+12+2KCI
②2FeCI2+C12-2FeCl3 ③2KMnO4+16HCl-2KCl+2MnCI 2+5C1 2+8H20在强酸
性溶液中,将MnO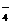 、Fe2+、Fe3+、I-和四种离子的溶液混在一起,充分反应后:
、Fe2+、Fe3+、I-和四种离子的溶液混在一起,充分反应后:
①若溶液中有l-剩余,则溶液中还可能有_______________,一定无____________;
②若Fe3+有剩余,则溶液中可能还有_________________,一定无_____________;
③若溶液中有Mn0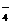 剩余,则还可能有_________,一定无_______________。
剩余,则还可能有_________,一定无_______________。
15、在甲、乙、丙三种溶液中各含有一种离子:CI-、Br-、I-向甲溶液中加入淀粉溶液
和氯水时,溶液变为橙色;再加入丙溶液,溶液颜色无明显变化。则乙溶液中含有的离子
A、Cl- B、Br- C、I- D、无法判断
第Ⅱ卷 (非选择题 共55分)
14、由CO2、H2和CO组成的混合气在同温同压下与氮气的密度相同,则该混合气体
中CO2、H2和CO的体积比为
A、29:8:13 B、22:1:14 C、13:8:100 D、16:26:57
13、下列各组中的两种物质相互作用时,当反应条件(温度、反应物用量比)改变,不会
引起产物的种类改变的是
A、Na和O2 B、Fe和盐酸 C、NaOH和C02 D、红磷和Cl2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com