
题目列表(包括答案和解析)
25、向NaHSO4溶液中,逐滴加入Ba(OH)2溶液直至溶液呈中性,请写出反应的离子方程式______________________________________ ,在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式__________________________ 。
24、下表是元素周期表的主族和零族部分,请用相应的化学用语回答有关问题:(用相应化学符号填写,下同)
|
主族 周期 |
|
|
ⅢA |
|
|
|
|
0 |
|
1 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
A |
|
B |
|
|
|
C |
D |
|
|
|
E |
|
|
|
|
F |
|
|
|
G |
|
H |
|
|
5 |
|
|
|
|
|
|
|
J |
⑴A、B的气态氢化物的稳定性是 > 。
⑵A、B、C、D的离子半径由大到小的顺序
⑶若E的原子序数为m,则A的原子序数是 ,H的原子序数是 。
⑷C、D、F的最高价氧化物的水化物的碱性强弱顺序是 。
⑸E、G的最高价氧化物的水化物的酸性强弱顺序是 。
⑹C在空气中燃烧产物的电子式是 。
⑺A-J所有元素中,两两相互结合成原子个数比为1∶2的离子化合物的化学式是 。
23、A~H 八种物质相互反应或转化的关系如图,其中A为非金属固体单质,火药中含有A元素。C、E、F、G、H均为含A元素的化合物,F可转化为H,常温下D为液态,F、H为气态,透过蓝色的钴玻璃观察B的焰色反应呈紫色。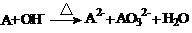

(1)A在周期表中的位置: 周期 族
(2)写出下列物质的电子式:
B D
(3)写出F和H反应的化学方程式
(4)写出下列反应的离子方程式
A + B:
H+Cl2(水):
22、为了除去粗盐中含有的Ca2+、Mg2+、SO42-及泥沙,可将粗食盐溶于水,然后进行下列操作:①过滤,②加稍过量的NaOH,③加适量盐酸,④加稍过量的Na2CO3溶液,⑤加稍过量的BaCl2溶液。正确的操作顺序为__________________。
21、图虚线框中的装置用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物。填写下列空白
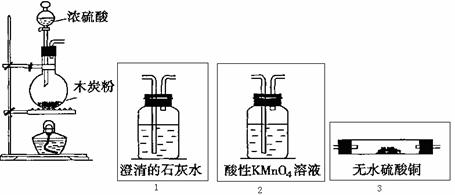
(1)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是_____________,不能检出的物质是____________。
(2)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是___________,不能检出的物质是_____________。
(3)如果将仪器的连接顺序变为②、③、①,则可检出的物质是___________,不能检出的物质是_____________。
20.下列说法正确的是 ( )
A.非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
B.只有非金属能形成含氧酸或含氧酸盐
C.除稀有气体外的非金属元素都能生成不同价态的含氧酸
D.非金属的最高价含氧酸都具有强氧化性
第II卷
19、某短周期元素的最外层有2 个电子,则这种元素是 ( )
A.金属元素
B.稀有气体元素
C.非金属元素
D.无法确定为哪一类元素
18、mgCu与足量浓H2SO4完全反应,在标准状况下得到nLSO2,则被还原的H2SO4的量不正确的是( )
A、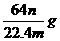 B、
B、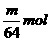
C、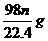 D、
D、
17、在50mlAl2(SO4)3溶液中,加入Cl-离子浓度为0.8mol·L-1的BaCl2溶液75ml,恰好使SO42-离子完全变成沉淀,则Al2(SO4)3溶液中Al3+离子的物质的量浓度为( )
A、0.6mol·L-1 B、0.4mol·L-1
C、0.3mol·L-1 D、0.2mol/L
16、下列各组溶液,只有组内溶液相互反应就能鉴别的是 ( )
A、Na2SO4、BaCl2、KNO3、NaCl
B、Na2SO4、Na2CO3、BaCl2、HCl
C、NaCl、Na2SO3、NaNO3、HCl
D、HCl、Na2CO3、Na2S、BaCl2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com